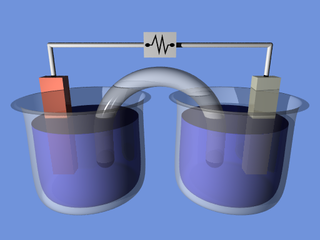
Электро́лиз — физико-химический процесс, состоящий в выделении на электродах составных частей растворённых веществ или других веществ, являющихся результатом вторичных реакций на электродах, который возникает при прохождении электрического тока через раствор либо расплав электролита.

Электрический аккумулятор — вторичный химический источник тока многоразового действия, который может быть вновь заряжен после разряда. Для заряда аккумулятора электрический ток пропускается в направлении, обратном направлению тока при разряде.

Никель-цинковый аккумулятор — это химический источник тока, в котором анодом является цинк, электролитом — гидроксид калия с добавкой гидроксида лития, а катодом — оксид никеля. Часто сокращается аббревиатурой NiZn.
Лантан-фторидный аккумулятор — очень мощный химический источник тока с твёрдым электролитом. Анод — металлический лантан или церий, электролит — фторид лантана с добавкой фторида бария или, в случае цериевого анода, фторид церия(III) с добавкой фторида стронция, катод — фторид висмута или свинца с добавкой фторида калия. Добавки фторидов калия и щелочноземельных металлов способствуют разупорядочению в анионной подрешетке фторидов лантана/церия, что в конечном счете приводит к 6-8-кратному увеличению удельной проводимости твердого электролита.

Никель-ка́дмиевый аккумуля́тор (NiCd) — вторичный химический источник тока, в котором катодом является гидрат закиси никеля Ni(OH)2 с графитовым порошком (около 5–8%), электролитом — гидроксид калия KOH плотностью 1,19–1,21 с добавкой гидроксида лития LiOH (для образования никелатов лития и увеличения ёмкости на 21–25%), анодом — гидрат закиси кадмия Cd(OH)2 или металлический кадмий Cd (в виде порошка). ЭДС никель-кадмиевого аккумулятора — около 1,37 В, удельная энергия — порядка 45–65 Вт·ч/кг. В зависимости от конструкции, режима работы (длительные или короткие разряды) и чистоты применяемых материалов, срок службы составляет от 100 до 9000 циклов заряда-разряда. Современные (ламельные) промышленные никель-кадмиевые батареи могут служить до 20–25 лет. Никель-кадмиевые аккумуляторы (NiCd) наряду с Никель-Солевыми аккумуляторами могут храниться разряженными, в отличие от никель-металл-гидридных (NiMH) и литий-ионных аккумуляторов (Li-ion), которые нужно хранить полностью заряженными.

Желе́зо-ни́келевый аккумуля́тор — это вторичный химический источник тока, в котором железо — анод, электролитом является водный раствор гидроксида натрия или калия, катод — гидрат окиси никеля(III).

Никель-металлогидридный аккумулятор — вторичный химический источник тока, в котором анодом является водородный металлогидридный электрод, электролитом — гидроксид калия, катодом — оксид никеля.

Марганцево-цинковый элемент, солевой элемент питания, также известный как элемент Лекланше — это первичный химический источник тока, в котором катодом является диоксид марганца MnO2 (пиролюзит) в смеси с графитом (около 9,5 %), электролитом — раствор хлорида аммония NH4Cl, анодом — металлический цинк Zn.

Литий-ионный аккумулятор (Li-ion) — тип электрического аккумулятора, который широко распространён в современной бытовой электронной технике и находит своё применение в качестве источника энергии в электромобилях и накопителях энергии в энергетических системах. Это самый популярный тип аккумуляторов в таких устройствах как сотовые телефоны, ноутбуки, цифровые фотоаппараты, видеокамеры и электромобили. В 2019 году Уиттингем, Гуденаф и Ёсино получили Нобелевскую премию по химии с формулировкой «За развитие литий-ионных аккумуляторов».

Литий-серный аккумулятор — вторичный химический источник тока, в котором катод жидкий с содержанием серы отделён от электролита специальной мембраной.

Суха́я батаре́я — необслуживаемая батарея, содержащая элементы, в которых электролит малоподвижен или не растекается за счет наличия адсорбирующего вещества, впитывающего влагу, или загустителя. В отличие от элементов, содержащих жидкий электролит, сухие элементы содержат электролит в виде пасты или геля, увлажненных лишь до состояния, которое необходимо для прохождения через них электрического тока, что предотвращает возможность утечки электролита и является, наряду с компактностью, главным достоинством сухих батарей. В конструкциях сухих батарей могут быть использованы химические источники тока разных типов. К сухим батареям так же иногда относят металл-воздушные топливные элементы.
Литий-титанатный аккумулятор (LTO) — вариант литий-ионных аккумуляторов, использующий пентатитанат лития (Li4Ti5O12) в качестве анода вместо графита, применяемого в большинстве других вариантов. Для увеличения площади анод имеет нанокристаллическое строение. Такое решение позволяет обеспечить площадь поверхности анода до 100 м²/г по сравнению с 3 м²/г для углерода, что позволяет значительно увеличить скорость перезарядки и обеспечить высокую плотность тока. По состоянию на 2017 год литий-титанатные батареи способны обеспечить плотность энергии до 177 Вт*ч/л. Кроме того, эти аккумуляторы имеют высокую надёжность и могут без потерь работать при более низких температурах до минус 30 градусов, в отличие от классических литий-ионных, которые уже при минус 5 градусах снижают свои показатели на 20 %.
На́нопроводнико́вый аккумуля́тор — вид литий-ионного аккумулятора, изобретённый группой под руководством д-ра И Цуя в Стэнфордском университете в 2007 г. Изобретение состоит в замене традиционного графитового анода аккумулятора на анод из нержавеющей стали, покрытый кремниевым нанопроводником. Кремний, способный удерживать в 10 раз больше лития чем графит, позволяет создавать значительно большую плотность энергии на аноде, снижая таким образом массу аккумулятора. В будущем увеличение площади поверхности анода позволит ускорить процесс зарядки и разрядки.

Литий-железо-фосфатный аккумулятор (LiFePO4, LFP) — тип электрического аккумулятора, являющийся видом литий-ионного аккумулятора, в котором используется LiFePO4 в качестве катода.

Щелочной элемент питания, щелочная батарейка — марганцево-цинковый гальванический элемент питания с щелочным электролитом. Изобретён Льюисом Урри.

Джон Баннистер Гуденаф — американский учёный, специалист в области физики и химии твёрдого тела и материаловедения. Известен своим вкладом в разработку первых литий-ионных аккумуляторов. Лауреат многих престижных премий, в том числе Нобелевской премии по химии 2019 года.

Натрий-ионный аккумулятор (Na-ion) — тип электрического аккумулятора, который имеет практически идентичные литий-ионному аккумулятору энергетические характеристики, но стоимость применяемых в нём материалов значительно ниже. Большим преимуществом натрий-ионных батарей является безвредность разряда до нуля, что делает более безопасной их перевозку и хранение.
Протонообменная мембрана или полимерно-электролитная мембрана - это полупроницаемая мембрана, обычно изготовленная из иономеров и предназначенная для проведения протонов, действуя как электронный изолятор и барьер для реагентов, например кислорода и водорода. Их основная функция при включении в мембранную электродную сборку (МЭС) топливного элемента с протонообменной мембраной или протонообменного мембранного электролизера - разделение реагентов и перенос протонов при блокировании прямого электронного пути через мембрану.
Батарея на расплавах солей — это аккумулятор, в котором в качестве электролита используются расплавленные соли. Такие аккумуляторы обеспечивают как высокую плотность энергии, так и высокую удельную мощность. Традиционные неперезаряжаемые термальные батареи могут храниться в твёрдом состоянии при комнатной температуре в течение длительного периода времени до активировации путём нагрева. Перезаряжаемые жидкометаллические батареи используются для промышленного резервного питания, электромобилей и для хранения энергии в сети, чтобы сбалансировать прерывистые возобновляемые источники энергии, такие как солнечные батареи и ветрогенераторы.

Батареи являлись основными источниками электричества до изобретения в конце XIX века электрогенераторов и электрических сетей. Успех в создании батарей ускорил развитие большинства электрических приборов: от телеграфов и телефонов до портативных компьютеров, мобильных телефонов и электроавтомобилей.













