Ангиогенин
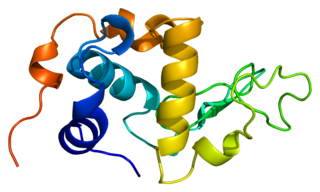
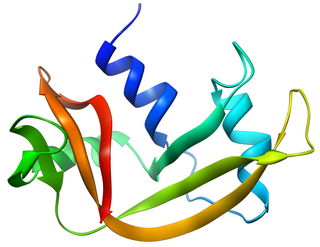
Ангиогенин — полипептид, вовлеченный в процесс ангиогенеза (образование новых сосудов). В отличие от других факторов ангиогенеза, ангиогенин обладает ферментативной активностью и его аминокислотная последовательность на 33 % сходна с последовательностью бычьей панкреатической рибонуклеазы (РНК-аза А). Ангиогенин разделяет общие каталитические свойства с рибонуклеазой (разрушает 3'-связь пиримидинов по механизму трансфосфорилирование/гидролиз), но его активность существенно отличается и по величине, и по специфичности.
Хотя ангиогенин содержит те же ключевые остатки аминокислот в активном центре, что и РНК-аза А, он расщеплет стандартные субстраты для РНК-аз в 105 — 106 медленнее, чем панкреатическая рибонуклеаза. Несмотря на эту очевидную слабость, каталитическая активность ангиогенина важна для его биологической роли: замена аминокислот в активном центре параллельно снижает и нуклеазную активность, и стимулирующее влияние на ангиогенеза, а замена, усиливающая ферментативную активность, стимулирует способность индуцировать пролиферацию сосудов.
Ангиогенин также может функционировать в качестве тРНК-специфической нуклеазы, связывающийся с актином на поверхности эндотелиальных клеток. Связавшись ангиогенин подвергается эндоцитозу, затем транслоцируется в ядро, обеспечивая эндотелиальную инвазивность, необходимую для формирования кровеносных сосудов. Ангиогенин индуцирует ангиогенез как в нормальных, так и в опухолевых тканях. Помимо этого он снижает уровень синтеза белка путём гидролиза клеточной тРНК.
Литература
- Давид Серван-Шрейбер. Антирак: новый образ жизни. - Москва : РИПОЛ классик, 2015.
- Saxena S. K., Rybak S. M., Davey R. T., et al. Angiogenin is a cytotoxic, tRNA-specific ribonuclease in the RNase A superfamily. (англ.) // J. Biol. Chem. : journal. — 1992. — Vol. 267, no. 30. — P. 21982—21986. — PMID 1400510.
- Weremowicz S., Fox E. A., Morton C. C., Vallee B. L. Localization of the human angiogenin gene to chromosome band 14q11, proximal to the T cell receptor alpha/delta locus. (англ.) // Am. J. Hum. Genet.[англ.] : journal. — 1990. — Vol. 47, no. 6. — P. 973—981. — PMID 1978563.
- Weremowicz S., Fox E. A., Morton C. C., Vallee B. L. The placental ribonuclease inhibitor (RNH) gene is located on chromosome subband 11p15.5. (англ.) // Genomics : journal. — Academic Press, 1991. — Vol. 8, no. 4. — P. 717—721. — doi:10.1016/0888-7543(90)90260-2. — PMID 2276743.
- Shapiro R., Riordan J. F., Vallee B. L. Characteristic ribonucleolytic activity of human angiogenin. (англ.) // Biochemistry : journal. — 1986. — Vol. 25, no. 12. — P. 3527—3532. — doi:10.1021/bi00360a008. — PMID 2424496.
- Weiner H. L., Weiner L. H., Swain J. L. Tissue distribution and developmental expression of the messenger RNA encoding angiogenin. (англ.) // Science : journal. — 1987. — Vol. 237, no. 4812. — P. 280—282. — doi:10.1126/science.2440105. — PMID 2440105.
- Bicknell R., Vallee B. L. Angiogenin activates endothelial cell phospholipase C. (англ.) // Proceedings of the National Academy of Sciences of the United States of America : journal. — 1988. — Vol. 85, no. 16. — P. 5961—5965. — doi:10.1073/pnas.85.16.5961. — PMID 2457905.
- Shapiro R., Vallee B. L. Site-directed mutagenesis of histidine-13 and histidine-114 of human angiogenin. Alanine derivatives inhibit angiogenin-induced angiogenesis. (англ.) // Biochemistry : journal. — 1990. — Vol. 28, no. 18. — P. 7401—7408. — doi:10.1021/bi00444a038. — PMID 2479414.
- Bicknell R., Vallee B. L. Angiogenin stimulates endothelial cell prostacyclin secretion by activation of phospholipase A2. (англ.) // Proceedings of the National Academy of Sciences of the United States of America : journal. — 1989. — Vol. 86, no. 5. — P. 1573—1577. — doi:10.1073/pnas.86.5.1573. — PMID 2646638.
- Lee F. S., Vallee B. L. Characterization of ribonucleolytic activity of angiogenin towards tRNA. (англ.) // Biochem. Biophys. Res. Commun.[англ.] : journal. — 1989. — Vol. 161, no. 1. — P. 121—126. — doi:10.1016/0006-291X(89)91569-6. — PMID 2730651.
- Lee F. S., Vallee B. L. Binding of placental ribonuclease inhibitor to the active site of angiogenin. (англ.) // Biochemistry : journal. — 1989. — Vol. 28, no. 8. — P. 3556—3561. — doi:10.1021/bi00434a061. — PMID 2742853.
- Strydom D. J., Fett J. W., Lobb R. R., et al. Amino acid sequence of human tumor derived angiogenin. (англ.) // Biochemistry : journal. — 1986. — Vol. 24, no. 20. — P. 5486—5494. — doi:10.1021/bi00341a031. — PMID 2866794.
- Kurachi K., Davie E. W., Strydom D. J., et al. Sequence of the cDNA and gene for angiogenin, a human angiogenesis factor. (англ.) // Biochemistry : journal. — 1986. — Vol. 24, no. 20. — P. 5494—5499. — doi:10.1021/bi00341a032. — PMID 2866795.
- Shapiro R., Vallee B. L. Human placental ribonuclease inhibitor abolishes both angiogenic and ribonucleolytic activities of angiogenin. (англ.) // Proceedings of the National Academy of Sciences of the United States of America : journal. — 1987. — Vol. 84, no. 8. — P. 2238—2241. — doi:10.1073/pnas.84.8.2238. — PMID 3470787.
- Rybak S. M., Fett J. W., Yao Q. Z., Vallee B. L. Angiogenin mRNA in human tumor and normal cells. (англ.) // Biochem. Biophys. Res. Commun.[англ.] : journal. — 1987. — Vol. 146, no. 3. — P. 1240—1248. — doi:10.1016/0006-291X(87)90781-9. — PMID 3619929.
- Shapiro R., Strydom D. J., Olson K. A., Vallee B. L. Isolation of angiogenin from normal human plasma. (неопр.) // Biochemistry. — 1987. — Т. 26, № 16. — С. 5141—5146. — doi:10.1021/bi00390a037. — PMID 3663649.
- Hu G. F., Strydom D. J., Fett J. W., et al. Actin is a binding protein for angiogenin. (англ.) // Proceedings of the National Academy of Sciences of the United States of America : journal. — 1993. — Vol. 90, no. 4. — P. 1217—1221. — doi:10.1073/pnas.90.4.1217. — PMID 7679494.
- Moroianu J., Riordan J. F. Identification of the nucleolar targeting signal of human angiogenin. (англ.) // Biochem. Biophys. Res. Commun.[англ.] : journal. — 1994. — Vol. 203, no. 3. — P. 1765—1772. — doi:10.1006/bbrc.1994.2391. — PMID 7945327.
- Moroianu J., Riordan J. F. Nuclear translocation of angiogenin in proliferating endothelial cells is essential to its angiogenic activity. (англ.) // Proceedings of the National Academy of Sciences of the United States of America : journal. — 1994. — Vol. 91, no. 5. — P. 1677—1681. — doi:10.1073/pnas.91.5.1677. — PMID 8127865.
- Acharya K. R., Shapiro R., Allen S. C., et al. Crystal structure of human angiogenin reveals the structural basis for its functional divergence from ribonuclease. (англ.) // Proceedings of the National Academy of Sciences of the United States of America : journal. — 1994. — Vol. 91, no. 8. — P. 2915—2919. — doi:10.1073/pnas.91.8.2915. — PMID 8159679.
- Hu G. F., Riordan J. F., Vallee B. L. A putative angiogenin receptor in angiogenin-responsive human endothelial cells. (англ.) // Proceedings of the National Academy of Sciences of the United States of America : journal. — 1997. — Vol. 94, no. 6. — P. 2204—2209. — doi:10.1073/pnas.94.6.2204. — PMID 9122172.
- ↑ 1 2 3 GRCh38: Ensembl release 89: ENSG00000214274 - Ensembl, May 2017
- ↑ 1 2 3 GRCm38: Ensembl release 89: ENSMUSG00000072115 - Ensembl, May 2017
- ↑ Ссылка на публикацию человека на PubMed: Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ↑ Ссылка на публикацию мыши на PubMed: Национальный центр биотехнологической информации, Национальная медицинская библиотека США.