Биосинтез гема

Биосинтез гема — метаболический многоступенчатый процесс образования молекул гема из его предшественников. Гем представляет собой плоский железосодержащий макроциклический комплекс, основу которого составляет четыре пиррольных кольца (тетрапиррол), объединённые между собой метениловыми мостиками (=СH-) и координированные двухвалентным железом (Fe2+). Гем имеет несколько типов, они отличаются как структурно, так и функционально. Но наиболее распространённым типом гема, является — гем Б[1].
Для позвоночных и некоторых видов прокариот (α-протеобактерий) биосинтез гема физиологически важный процесс, так как гем включается в состав многих белков и ферментов (в качестве простетической группы), которые участвуют в газообмене и переносе кислорода (гемоглобин — в эритроцитах и миоглобин — в мышцах), катализе, окислительном фосфорилировании, биотрансформации метаболитов и ксенобиотиков и защите от патогенов (каталаза, пероксидаза, цитохромы, NO-cинтаза, циклооксигеназы, миелопероксидаза и т.д.)[2][3]. Реакции синтеза гема у позвоночных протекает, как в митохондриях, так и в цитозоле клеток, у прокариот только в цитозоле. Практически все клетки тела позвоночных, включая и человека (кроме зрелых эритроцитов), способны синтезировать гем, однако, интенсивно этот процесс наблюдается в клетках эритропоэтической ткани красного костного мозга (проэритробластах, эритробластах, ретикулоцитах) и гепатоцитах печени.
Реакции
Синтез гема включает в себя восемь последовательных реакций, протекающие как в матриксе митохондрий (1, 6, 7 и 8-я реакции), так и в цитозоле (2, 3, 4 и 5-я реакции). Начало и конец синтеза локализованы в одном компартменте — митохондрии, что позволяет эффективнее регулировать данный процесс. Количество цитозольных ферментов, как правило, на порядки выше митохондриальных, так как они слабо индуцируются модуляторами.

Синтез аминолевулината
Первая реакция в синтезе молекул гема начинается в матриксе митохондрии. Глицин и сукцинил-КоА являются главными предшественниками в образовании гема. Под действием фермента АЛК-синтазы (КФ 2.3.1.37) происходит конденсация глицина с сукцинил-КоА, в результате которой образуется аминолевулинат (АЛК), углекислый газ и кофермент А. Схема реакции:
- сукцинил-КоА + глицин δ-аминолевулиновая кислота + КоА + CO2.

В качестве кофермента используется молекула пиридоксаль-5'-фосфата (PLP).
Данная реакция является ключевой в синтезе гема и протекает достаточно медленно по отношению к последующим (лимитирующая стадия). Реакция регулируется аллостерически гемом, также он влияет на транскрипцию АЛК-синтазы, прекращая её синтез. Свободные ионы двухвалентного железа (Fe2+) положительно влияют на синтез АЛК-синтазы. Барбитураты усиливают индукцию АЛК-синтазы в гепатоцитах, а гемин и глюкоза аллостерически ингибируют[4]. Образовавшийся в ходе реакции аминолевулинат из матрикса митохондрии поступает в цитозоль.
Конденсация аминолевулината в порфобилиноген
Вторая реакция в процессе синтеза гема характеризуется несимметричной конденсацией двух молекул аминолевулината (АЛК) и одновременно с этим происходящая циклизация, с образованием молекулы порфобилиногена. Реакцию катализирует фермент порфобилиногенсинтаза или АЛК-дегидратаза (КФ 4.2.1.24) по следующему уравнению:

- 2 5-аминолевулинат порфобилиноген + 2H2O.
Эта реакция является первой общей стадией биосинтеза всех природных тетрапирролов. Фермент в качестве кофактора использует ионы цинка Zn2+, они поддерживают активность. Фермент АЛК-дегидратаза регулируется аллостерически гемом (слабо ингибируется). Ионы свинца (Pb2+) являются сильным ингибитором, связывание которых приводит к полной и необратимой инактивации фермента.
Образование гидроксиметилбилана
В третьей реакции синтеза гема происходит конденсация четырёх молекул порфобилиногена и одновременно с этим дезаминирование, которые приводят к образованию линейного тетрапиррола — гидроксиметилбилана и аммиака. Фермент, катализирующий данную реакцию — гидроксиметилбилансинтаза или порфобилиноген дезаминаза (КФ 2.5.1.61). Схема реакции:
- 4порфобилиноген + H2O гидроксиметилбилан + 4NH3

Циклизация гидроксиметилбилана в уропорфириноген III
Четвёртая реакция синтеза гема протекает в цитозоле клеток. На этой стадии под действием фермента уропорфириноген III синтазы (КФ 4.2.1.75), линейные молекулы гидроксиметилбилана подвергаются циклизации в уропорфириноген III. При катализе происходит инверсия конечного пиррольного звена (кольцо D) линейной молекулы гидроксиметилбилана, связывая его с первым пиррольным звеном (кольцо А), тем самым образуя крупную макроциклическую структуру, уропорфириноген III[5].
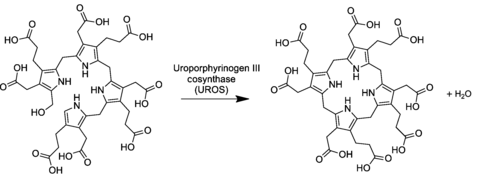
При сниженной активности или дефиците фермента уропорфириноген III синтазы наблюдается образование уропорфириногена I (неферментативно), который обнаруживается в моче и может накапливаться в клетках кожи, где окислятся под действием солнечного света до фототоксичного уропорфирина I. Заболевание, при котором наблюдается дефицит УПГ-III-синтазы называется врождённая эритропоэтическая порфирия или болезнь Гюнтера[6].
Образование копропорфириногена III
В пятой реакции синтеза гема молекулы уропорфириногена III декарбоксилируются с образованием копропорфириногена III. Реакцию катализирует фермент — уропорфириноген III декарбоксилаза (КФ 4.1.1.37). Схема реакции:
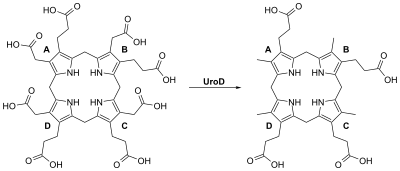
Интересной особенностью является то, что данный фермент не использует в качестве кофермента пиридоксаль-5′-фосфат, несмотря на то, что относится к декарбоксилазам.
Реакция протекает в цитозоле, образовавшийся копропорфириноген III далее поступает в матрикс митохондрии, где происходит его дальнейшее преобразование в протопорфириноген IX. В отчёте 2008 г. показано, что некатализируемая УПГ-III-декарбоксилазой скорость реакции составляет 10–19 с–1, поэтому при pH 10 ускорение реакции данным ферментом относительно некатализируемой, т.е. каталитическая эффективность, является наибольшим для любого известного фермента и составляет 6 х 1024 М-1[7].
Превращения копропорфириногена III в протопорфириноген IX
Шестая реакция синтеза гема протекает в матриксе митохондрии. На этой стадии копропорфириноген III поступает из цитозоля в матрикс митохондрии, где происходит его преобразование в протопорфириноген IX, под действием фермента копропорфириноген III оксидазы (КФ 1.3.3.3) Схема реакции:
- копропорфириноген III + 2O2 + 2H+ → протопорфириноген IX + 2H2O + 2CO2

Окисление протопорфириногена IX в протопорфирин IX
Седьмая реакция синтеза гема, в которой происходит образование молекул протопорфирина IX, путём окисления протопорфориногена IX, под действием фермента протопорфириноген IX оксидазы (КФ 1.3.3.4)[8]. Реакция протекает в митохондриальном матриксе. Схема реакции:
- протопорфириноген IX + 3O2 → протопорфирин IX + 3H2O2

Протопорфирин IX является первым окрашенным тетрапирролом в синтезе гема.
Образование гема из протопорфирина IX
Последняя реакция, которая завершает многостадийный процесс синтеза гема. В данной реакции происходит внедрение ионов железа (металлирование) внутрь плоского макроцикла протопорфирина IX. Катализирует реакцию фермент феррохелатаза (КФ 4.98.1.1). Схема реакции:
- протогем (гем Б) + 2H+ = протопорфирин IX + Fe+2.
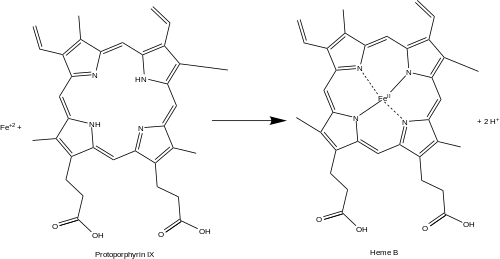
Феррохелатаза очень чувствительна к воздействию ионов тяжёлых металлов (Mn2+, Pb2+, Hg2+ и Cd2+), но в особенности к ионам свинца Pb2+, которые препятствуют высвобождению продукта после металлирования[9].
Регуляция
Синтез гема относится к метаболическим процессам со строгой регуляцией, которая осуществляется за счёт аллостерического воздействия продукта — гема на некоторые ферменты, участвующие в данном процессе. Также гем, может влиять не только на активность ферментов, но и на их количество, контролируя их синтез. К модуляторам индукции ферментов относят также ионы двухвалентного железа Fe2+, стероидные гормоны (особенно половые), некоторые лекарственные средства (барбитураты, диклофенак, сульфаниламиды, эстрогены, прогестины). На синтез гема влияют и физиологические факторы, например, сатурация (насыщение) крови кислородом.
Аллостерическая регуляция
Аллостерическая регуляция синтеза гема осуществляется самой молекулой, при связывании его с некоторыми ферментами. Когда концентрация образовавшегося гема достаточна для связывания с α- и β-цепями глобина (эквимолярная концентрация 1:1), происходит снижение активности АЛК-синтазы в митохондриях и АЛК-дегидратазы (в меньшей степени) в цитозоле клеток (отрицательная обратная связь).
Регуляция на уровне транскрипции и трансляции
Гем влияет на транскрипцию гена АЛК-синтазы. Гем транслоцируется в клеточное ядро, где его связывание с белком-репрессором приводит к подавлению активности РНК-полимеразы II, и как следствие прекращению синтеза мРНК. Прекращение синтеза мРНК гена АЛК-синтазы снижает количество данного фермента. Таким образом, гем отрицательно влияет на индукцию АЛК-синтазы.
Ионы двухвалентного железа Fe2+ являются сильным индуктором АЛК-синтазы в ретикулоцитах. На участке 5′-UTR мРНК, кодирующей данный фермент, имеется последовательность нуклеотидов, образующая шпилечную петлю, которая называется железозависимым элементом (от англ. Iron responsive element, сокр. IRE). При высоких концентрациях железа в клетках оно образует комплекс с остатками цистеина регуляторного железосвязывающего белка (англ. Iron responsive element-binding proteins, сокр. IRP-BP — белок, связывающий железозависимый элемент). Взаимодействие железа с регуляторным железосвязывающим белком вызывает снижение сродства этого белка к IRE-элементу мРНК, кодирующей аминолевулинатсинтазу, и продолжение трансляции. При низких концентрациях железа железосвязывающий белок присоединяется к железозависимому элементу, находящемуся на 5'-нетранслируемом конце мРНК, что приводит к препятствию посадки малой субъединицы рибосомы и инициация трансляция аминолевулинатсинтазы тормозится.
В гепатоцитах печени индукторами АЛК-синтазы являются лекарственные препараты, стероиды, витамин Е. Индукция данного фермента обусловлена высокой интенсивностью микросомальной системы окисления (осуществляет биотрансформацию метаболитов) в ЭПР, которой требуется гем для образования цитохрома P450. Большинство индукторов влияют на синтез АЛК-синтазы подобно липофильным гормонам (стероиды, йодтиронины), образуя в цитозоле комплекс лиганд-рецептор, который перемещается в ядро. В ядре комплекс лиганд-рецептор воздействует на локус гена аминолевулинатсинтазы как активатор транскрипции.
Сатурация крови
Низкая сатурация крови (менее 94 %) приводит к гипоксии. В ответ на гипоксию в клетках почки усиливается экспрессия гормона эритропоэтина (EPO), который воздействует на ферменты синтеза гема. Так, EPO действуя на собственные рецепторы в ретикулоцитах быстро вызывает индукцию АЛК-синтазы, тем самым положительно влияет на синтез гема. Одновременно EPO усиливает и синтез цепей глобина. Эрипоэтин увеличивает количество эритроцитов в плазме крови, за счёт их быстрого созревания. Данные процессы необходимы для быстрой компенсации низких уровней кислорода и поддержания тканевого дыхания клеток.
Клиническое значение
Синтез гема представляет собой довольно сложный и многостадийный регулируемый процесс, который зависит от слаженной работы ферментов и предшественников метаболитов, коферментов и многих других соединений. Клиническое значение данного процесса заключается в нарушениях, которые возникают и проявляются в результате различных факторов. Нарушения синтеза гема классифицирует на приобретённые и врождённые.
Порфирии
Врождённые заболевания связанные с дефицитом с ферментов синтеза гема называют — порфириями[10]. Общей характеристикой порфирий является избыточное накопление порфиринов (линейных и циклических тетрапирролов) в тканях и органах, а также их усиленная экскреция с мочой и калом (придавая им нехарактерный цвет). Порфирины, как правило, не являются биологически активными, но проявляются свойства сильных оксидантов. Накопления порфиринов в тканях и органах сопровождаются деструктивными процессами: разрушением соединительных тканей (связок, хрящей и т.д.), поражением кожи (фотодерматиты), гемолизом эритроцитов, нарушениями пищеварения, гиперпигментацией слизистых и зубной эмали, нейропатиями и дегенерацией нервной ткани (димиелинизация, энцефалопатии) и последующими психическими расстройствами.
В зависимости от основной локализации патологического процесса различают печёночные и эритропоэтические наследственные порфирии. Эритропоэтические порфирии сопровождаются накоплением порфиринов в нормобластах и эритроцитах, а печёночные — в гепатоцитах. По клиническому течению порфирии разделяют на острые (острая перемежающаяся порфирия, наследственная копропорфирия, вариегатная порфирия и т.д.) и хронические (врождённая эритропоэтическая порфирия, поздняя кожная порфирия и др.).
В зависимости от того, что больше накапливается — порфирины или их предшественники, может различаться и клиническая картина. В одних случаях превалируют поражения нервной системы (нейровисцеральные проявления), в других — кожных покровов (кожные проявления). Порфирии с острым, прогрессирующим течением, преобладающим поражением нервной системы принято называть острыми. Если доминируют кожные нарушения, то, как правило, болезнь имеет затяжное, подострое течение.
Патогенетическая классификация порфирий приведена в таблице
| Дефицит фермента | Наименование заболевания и характер наследования | Печёночная/эритропоэтическая форма | Клинические проявления |
|---|---|---|---|
| Эритроидная форма АЛК-синтазы (ALAS2) | X-сцепленная протопорфирия | Эритропоэтическая | Сидеробластная анемия, кожные — фотосенсибилизация без пузырей |
| АЛК-дегидратаза | Порфирия, обусловленная дефицитом АЛК-дегидратазы. Аутосомно-рецессивный | Печёночная* | Нейровисцеральные |
| ПБГ-дезаминаза | Острая перемежающаяся порфирия (ОПП). Аутосомно-доминантный | Печёночная | Нейровисцеральные |
| УПГ-III-синтаза | Врождённая эритропоэтическая порфирия (ВЭП) или болезнь Гюнтера. Аутосомно-рецессивный | Печёночная | Кожные — фотосенсибилизация без пузырей |
| УПГ-III-декарбоксилаза | Поздняя кожная порфирия (ПКП). Аутосомно-доминантный | Печёночная | Кожные — фотосенсибилизация с пузырями |
| КПГ-III-оксидаза | Наследственная копропорфирия (НКП). Аутосомно-доминантный | Печёночная | Нейровисцеральные. Редкие проявления фотосенсибилизации с пузырями |
| ППГ-IX-оксидаза | Вариегатная порфирия (ВП). Аутосомно-доминантный | Печёночная | Нейровисцеральные. Частые проявления фотосенсибилизации с пузырями |
| Феррохелатаза | Эритропоэтическая протопорфирия (ЭПП). Аутосомно-рецессивный | Эритропоэтическая | Кожные — фотосенсибилизация без пузырей |
| * Эти типы порфирий имеют смешанную форму. |
Врождённые дефициты железа
Врождённые дефициты железа очень редкие заболевания, связанные с нарушениями синтеза белков регулирующих и переносящих связанное железо. Одним из таких заболеваний, является железорезистентная железодефицитная анемия. В основе патогенеза лежит чрезмерный синтез пептидного гормона гепсидина в клетках печени. Гепсидин является одним из белков острой фазы, который регулирует концентрацию железа в плазме крови и его распределение в тканях и органах. Синтез гепсидина связан в первую очередь с воспалительными или инфекционными процессами, а действие направлено на снижение всасывании железа в энтероцитах, снижению выхода железа из гепатоцитов, энтероцитов и макрофагов, рециркуляции и накоплению его в клетках. Гепсидин регулируется с помощью сериновой протеазы матриптаза-2 (КФ 3.4.21.109). При мутациях гена, кодирующего матриптазу-2 — TMPRSS6, активность гепсидина резко повышается, что приводит к резкому снижению всасывания поступающего из пищи железа в организм человека. Заболевание носит аутосомно-рецессивный характер наследования. Течение заболевания доброкачественное, однако требует парентерального введения препаратов железа и постоянного контроля за уровнем сывороточного железа, особенно во время роста детей, при беременности или менструациях у лиц женского пола.
Приобретённые нарушения синтеза гема
К приобретённым нарушениям синтеза гема относят заболевания или дефициты вызванные негенетическими факторами, к ним относятся дефициты витаминов, микроэлементов, голодание, обильные кровопотери, отравления токсинами.
Гиповитаминоз В6
Гиповитаминоз В6 — редко встречаемый дефицит витамина В6. Основные причины его возникновения это скудное питание, обусловленное недоеданием, долговременное голодание, чрезмерная потеря при гемодиализе, хроническая алкогольная интоксикация или неконтролируемый приём противотуберкулёзных препаратов (например изониазида), которые проявляют антивитаминные свойства. Активная форма витамина B6 представлена пиридоксальфосфатом, который является коферментом множества ферментов, включая и АЛК-синтазу. Поэтому дефицит витамина В6 способен влиять на синтез гема.
Гиповитаминоз В6 сопровождается симптомами сидеробластной (гипохромной) микроцитарной анемией, для неё характерно наличие мелких по размеру эритроцитов светло-красного цвета. Такой цвет указывает на низкую способность синтеза гема (гипохромия). Гипохромная анемия, вызванная дефицитом В6 не поддаётся лечению препаратами железа.
Дефицит железа
Железо (Fe2+) является неотъемлемым компонентом гема. При наличии его дефицита, синтез гема протекает медленно и недостаточно чтобы исполнять свои физиологические функции.
Приобретённый дефицит железа характеризуется тем, что организм человека не получает нормальное количество железа с пищей, есть нарушения в работе органов ЖКТ, произошла обширная кровопотеря или имеются алиментарные факторы, влияющие на его поступление. Одним из таких факторов является недостаточность аскорбиновой кислоты и гипоацидный гастрит. Негемовое железо поступает с пищей обычно в виде ионов Fe3+, которые не способны всасываться в энтероцитах кишечника. Для этого необходимо наличие медьзависимого фермента — ферроредуктазы, она способна восстанавливать ионы Fe3+ в Fe2+. В такой форме железо далее всасывается внутрь клетки. В качестве кофактора-восстановителя ферроредуктаза использует молекулы аскорбата. При наличии гиповитаминоза С, негемовое железо не сможет эффективно всасываться в кишечнике. Наличие гипоацидного гастрита существенно ухудшает всасывание гемового железа, так как необходимая для высвобождения гема из белков соляная кислота слабо синтезируется. Бедная животным белком диета также сказывается на уровне железа в организме, в конечном итоге приводя к железодефицитной анемии. Все приобретённые формы железодефицита подаются терапии.
Отравления тяжёлыми металлами
Тяжёлые металлы являются ярко выраженными ингибиторами ферментов синтеза гема. Их действия на ферменты необратимые. Даже ничтожные количества ионов мышьяка или свинца могут существенно снижать процессы катализа ферментов. Симптомы таких отравлений и клиническое течение напоминают некоторые формы порфирий. Свинец также может вызывать приобретённую форму сидеробластной анемии. Поэтому отравления тяжёлыми металлами приводят к серьёзным поражениям кроветворения.
Бензол
Отравление бензолом нарушает синтез гема, как в гепатоцитах, так и в красном костном мозге. Но особенно чувствительны к его воздействию эритропоэтические клетки. Бензол является сильным миелотоксином, он воздействует на систему кроветворения, подавляя её за счёт дегенерации и деструкции миелоидной ткани, вплоть до апластической анемии, миелодиспластического сииндрома и миелоидного лейкоза[11]. Его воздействие на систему гемопоэза имеет сходство с ионизирующим излучением (радиомиметичность). Угнетение синтеза гема бензолом обусловлено тем, что продукты его окисления системой цитохрома P450, инициируют образование большего количества свободных радикалов (АФК). АФК вызывают избыточные цепные реакции, ионизацию и окисление при взаимодействии их с различными молекулами в клетках, включая нуклеиновые кислоты и ферменты. Ферменты, которые подвергаются воздействию АФК, в дальнейшем не способны к катализу. Продукты окисления бензола (оксид и эпоксид) нарушают нативную структуру ДНК, тем самым вызывая мутации и канцерогенез. Деструктивное влияние АФК на мембраны клеток приводят к их гибели. Таким образом, отравление бензолом может существенно снижать уровень здоровья и продолжительность жизни.
Примечания
- ↑ Ogun, Aminat S.; Joy, Neena V.; Valentine, Menogh (2022), "Biochemistry, Heme Synthesis", StatPearls, Treasure Island (FL): StatPearls Publishing, PMID 30726014, Архивировано 8 ноября 2022, Дата обращения: 3 января 2023
- ↑ Paoli, M. (2002). "Structure-function relationships in heme-proteins" (PDF). DNA Cell Biol. 21 (4): 271—280. doi:10.1089/104454902753759690. hdl:20.500.11820/67200894-eb9f-47a2-9542-02877d41fdd7. PMID 12042067. S2CID 12806393. Архивировано (PDF) 24 июля 2018.
- ↑ Alderton, W.K. (2001). "Nitric oxide synthases: structure, function and inhibition". Biochem. J. 357 (3): 593—615. doi:10.1042/bj3570593. PMC 1221991. PMID 11463332.
- ↑ Doss M, Sixel-Dietrich F, Verspohl F (1985). ""Glucose effect" and rate limiting function of uroporphyrinogen synthase on porphyrin metabolism in hepatocyte culture: relationship with human acute hepatic porphyrias" (PDF). J Clin Chem Clin Biochem. 23 (9): 505—13. doi:10.1515/cclm.1985.23.9.505. PMID 4067519.
- ↑ Raux E, Schubert HL, Warren MJ (December 2000). "Biosynthesis of cobalamin (vitamin B12): a bacterial conundrum". Cell. Mol. Life Sci. 57 (13—14): 1880—93. doi:10.1007/PL00000670. PMID 11215515. S2CID 583311.
- ↑ To-Figueras J, Badenas C, Mascaro JM, Madrigal I, Merino A, Bastida P, Lecha M, Herrero C (2007). "Study of the genotype-phenotype relationship in four cases of congenital erythropoietic porphyria". Blood Cells Mol. Dis. 38 (3): 242—6. doi:10.1016/j.bcmd.2006.12.001. PMID 17270473.
- ↑ Lewis CA, Wolfenden R (November 2008). "Uroporphyrinogen decarboxylation as a benchmark for the catalytic proficiency of enzymes". Proc. Natl. Acad. Sci. U.S.A. 105 (45): 17328—33. Bibcode:2008PNAS..10517328L. doi:10.1073/pnas.0809838105. PMC 2582308. PMID 18988736.
- ↑ Paul R. Ortiz de Montellano (2008). "Hemes in Biology". Wiley Encyclopedia of Chemical Biology. John Wiley & Sons. doi:10.1002/9780470048672.wecb221. ISBN 978-0470048672.
- ↑ Medlock, Amy E.; Carter, Michael; Dailey, Tamara A.; Dailey, Harry A.; Lanzilotta, William N. (October 2009). "Product Release Rather than Chelation Determines Metal Specificity for Ferrochelatase". Journal of Molecular Biology. 393 (2): 308—319. doi:10.1016/j.jmb.2009.08.042. PMC 2771925. PMID 19703464.
- ↑ porphyria. MedlinePlus (июль 2009). Дата обращения: 31 марта 2021. Архивировано 3 мая 2023 года.
- ↑ Smith, Martyn T. (2010). "Advances in understanding benzene health effects and susceptibility". Annu Rev Public Health. 31: 133—48. doi:10.1146/annurev.publhealth.012809.103646. PMC 4360999. PMID 20070208.