
Физи́ческая хи́мия — раздел химии, наука об общих законах строения, структуры и превращения химических веществ. Исследует химические явления с помощью теоретических и экспериментальных методов физики. Наиболее обширный раздел химии.
Кисло́ты — химические соединения, способные отдавать катион водорода, либо соединения, способные принимать электронную пару с образованием ковалентной связи.

Катализа́тор — химическое вещество, ускоряющее реакцию, но не расходующееся в процессе реакции.
Сверхкислота́ (или магическая кислота, су̀перкислота́) — комплексное неводное вещество или смесь веществ, параметр кислотности которых превышает кислотность 100%-ой серной кислоты. В данном случае параметр кислотности принимается как способность кислоты протонировать произвольное основание и фактически совпадает с функцией кислотности. Для 100 % серной кислоты параметр кислотности составляет H0 = −12,2. Наличие воды снижает кислотность сверхкислот, так как в присутствии воды сила кислоты ограничивается кислотностью иона гидроксония H3O+.

В биологии активный центр — это область фермента, где молекулы субстрата связываются и подвергаются химической реакции. Активный центр состоит из аминокислотных остатков, которые образуют временные связи с субстратом, и остатков, которые катализируют реакцию этого субстрата. Хотя активный центр занимает только ~ 10-20 % от объёма фермента он является наиболее важной частью, поскольку он непосредственно катализирует химическую реакцию. Обычно активный центр состоит из трех-четырех аминокислот, в то время как другие аминокислоты в белке необходимы для поддержания его третичной структуры.
Амфоте́рность — способность некоторых химических веществ и соединений проявлять в зависимости от условий как кислотные, так и осно́вные свойства.
Ката́лиз — избирательное ускорение одного из возможных термодинамически разрешённых направлений химической реакции под действием катализатора(ов), который, согласно теории промежуточных соединений, многократно вступает в промежуточное химическое взаимодействие с участниками реакции и восстанавливает свой химический состав после каждого цикла промежуточных химических взаимодействий.

Дми́трий Влади́мирович Соко́льский — советский ученый-химик, работавший в области органического катализа, профессор КазГУ (1949), академик АН КазССР (1951), первый директор Алма-Атинского института органического катализа и электрохимии (1969), основоположник химической науки в Казахстане, создатель научной школы катализа.

Алекса́ндр Нау́мович Фру́мкин — советский физикохимик, организатор науки, автор основополагающих работ в современной электрохимии; основоположник электрохимической кинетики, один из основателей современного учения об электрохимических процессах, создатель советской электрохимической научной школы.
Функция кислотности Гаммета — численное выражение способности среды быть донором протонов по отношению к произвольному основанию, безразмерная величина. Количественный параметр в теории Бренстеда-Лоури, в противовес водородному показателю рН в теории Аррениуса.
Тео́рии кисло́т и основа́ний — совокупность фундаментальных физико-химических представлений, описывающих природу и свойства кислот и оснований. Все они вводят определения кислот и оснований — двух классов веществ, реагирующих между собой. Задача теории — предсказание продуктов реакции между кислотой и основанием и возможности её протекания, для чего используются количественные характеристики силы кислоты и основания. Различия между теориями лежат в определениях кислот и оснований, характеристики их силы и, как следствие — в правилах предсказания продуктов реакции между ними. Все они имеют свою область применимости, каковые области частично пересекаются.
Уравнение Брёнстеда — уравнение, количественно описывающее зависимость скорости катализируемых кислотами или основаниями реакций от природы катализатора. Впервые установлено в 1924 году Брёнстедом и Педерсеном.
Автопротолиз — гомофазный процесс самоионизации, обратимый процесс передачи протона от одной нейтральной молекулы жидкости к другой и образования в результате равного числа катионов и анионов.
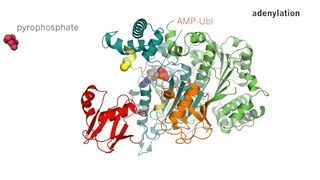
Ферментативный катализ — это увеличение скорости процесса с помощью биологической молекулы, «фермента». Большинство ферментов представляют собой белки, и большинство таких процессов представляют собой химические реакции. Внутри фермента катализ обычно происходит в локализованном центре, называемом активным центром.

Томас Мартин Лаури (Лоури) — британский химик. Основные научные работы посвящены изучению оптической активности органических соединений. Создатель протонной теории кислот и оснований.
Основания — химические соединения, способные образовывать ковалентную связь с протоном либо с вакантной орбиталью другого химического соединения. В узком смысле, под основаниями понимают осно́вные гидроксиды — сложные вещества, при диссоциации которых в водных растворах отщепляется только один вид анионов — гидроксид-ионы OH−.

Константи́н Бори́сович Яцими́рский (1916—2005) — советский и украинский учёный-химик, академик Академии наук Украинской ССР (1964).
Кисло́тно-осно́вные реа́кции — это химические реакции между кислотой и основанием. Сопровождаются передачей протона.

Гидрон (англ. Hydron) - общее название для катионной формы атома водорода, представляемый в таблице символом Н+. Термин "Гидрон", одобренный ИЮПАК, объединяет катионы водорода независимо от их изотопного состава. То есть, он относится к протонам (1H+) для изотопов протия, дейтронам (2H+ или D+) для изотопов дейтерия, и тритонам (3H+ или T+) для изотопов трития
Теория Брёнстеда–Лоури — это кислотно-основная теория, которая была предложена независимо друг от друга учёными Брёнстедом Йоханнесом Николаусом и Лоури Томасом Мартином в 1923 году. Фундаментальная основа этой теории в том, что когда кислота и основание реагируют друг с другом, кислота образует сопряженное основание, а основание образует сопряженную кислоту с помощью обмена протоном (катионом водорода или H+). Эта теория является обобщением теории Аррениуса.









