
Дезоксирибонуклеи́новая кислота́ (ДНК) — макромолекула, обеспечивающая хранение, передачу из поколения в поколение и реализацию генетической программы развития и функционирования организмов. Молекула ДНК хранит биологическую информацию в виде генетического кода, состоящего из последовательности нуклеотидов. ДНК содержит информацию о структуре различных видов РНК и белков.
Рибонуклеи́новая кислота́ (РНК) — одна из трёх основных макромолекул, которые содержатся в клетках всех живых организмов и играют важную роль в кодировании, прочтении, регуляции и экспрессии генов.

Этилендиаминтетрауксусная кислота, ЭДТА (от англ. EDTA), комплексон II — органическое соединение, четырёхосновная карбоновая кислота с химической формулой (HOOCCH2)2N(CH2)2N(CH2COOH)2, белый мелкокристаллический порошок, малорастворим в воде, нерастворим в большинстве органических растворителей, растворим в щелочах, с катионами металлов образует соли этилендиаминтетраацетаты. Получают конденсацией этилендиамина с монохлоруксусной кислотой. Соединение было впервые синтезировано в 1935 году Фердинандом Мюнцем, который получил соединение из этилендиамина и хлоруксусной кислоты.
Бу́ферные раство́ры — растворы с определённой устойчивой концентрацией водородных ионов, рН которых мало изменится при прибавлении к ним небольших количеств сильного основания или сильной кислоты, а также при разбавлении и концентрировании.

Нуклеи́новая кислота — высокомолекулярное органическое соединение, биополимер (полинуклеотид), образованный остатками нуклеотидов. Нуклеиновые кислоты ДНК и РНК присутствуют в клетках всех живых организмов и выполняют важнейшие функции по хранению, передаче и реализации наследственной информации.

Митохондриа́льная ДНК (мтДНК) — ДНК, находящаяся в митохондриях, органеллах эукариотических клеток.

В молекулярной биологии метод полимеразной цепной реакции с обратной транскрипцией принято обозначать как ОТ-ПЦР. ОТ-ПЦР представляет собой метод амплификации специфического фрагмента рибонуклеиновой кислоты (РНК).
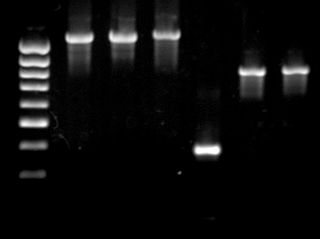
Электрофорез ДНК в агарозном геле — аналитический метод, применяемый для разделения фрагментов ДНК по длине. Основан на разной скорости движения фрагментов разной длины при движении в геле под действием внешнего электрического поля.
Гибридизация ДНК, гибридизация нуклеиновых кислот — соединение in vitro комплементарных одноцепочечных нуклеиновых кислот в одну молекулу. При полной комплементарности объединение происходит легко и быстро, а в случае частичной некомплементарности слияние цепочек замедляется, что позволяет оценить степень комплементарности. Возможна гибридизация ДНК-ДНК и ДНК-РНК.

ДНК-микрочип, или ДНК-чип — технология, используемая в молекулярной биологии и медицине. ДНК-микрочип представляет собой множество небольших одноцепочечных молекул — ДНК-зондов, которые ковалентно пришиты к твёрдому основанию. Каждый такой зонд имеет строго определённую последовательность нуклеотидов и место на микрочипе. Одинаковые зонды располагаются вместе, образуя сайт микрочипа. Между сайтом и последовательностью ДНК зонда есть взаимно-однозначное соответствие. ДНК-микрочипы используются для определения ДНК или РНК, которые могут быть как белок-кодирующими, так и не кодировать белки. Измерение генной экспрессии посредством кДНК называется профилем экспрессии, или экспрессионным анализом. На современных микрочипах можно полностью расположить целый геном, каждый известный ген которого будет являться зондом.
Натрий-фосфатный буфер — буферный раствор, используемый в биологических исследованиях. Представляет собой водный раствор солей, содержащий хлорид натрия, гидрофосфат натрия, хлорид калия и дигидрофосфат калия. Осмолярность и концентрации ионов в растворе обычно соответствуют концентрациям в теле человека.
Натрий-ацетатный буфер — буферный раствор, содержащий ацетат натрия и уксусную кислоту. Значение pK ацетатного буфера составляет около 4,75, поэтому применение находят буферы со значениями рН от 3 до 6.

Трис (англ. Tris, THAM) — сокращённое название химического соединения трис(гидроксиметил)аминометана (HOCH2)3CNH2. Трис широко используется в биохимии и молекулярной биологии в качестве буферного раствора, например, в буферных системах TAE и TBE, для растворения нуклеиновых кислот. По химической структуре трис является первичным амином и имеет характерные для аминов свойства, например, конденсируется с альдегидами.
Количественный анализ нуклеиновых кислот — определение концентрации ДНК или РНК в смеси или чистом препарате. Реакции с участием нуклеиновых кислот часто требуют точных сведений о количестве и чистоте препарата. Для определения концентрации нуклеиновой кислоты в растворе используют спектрофотометрический метод и УФ-флюоресценцию, если нуклеиновая кислота содержит краситель.

Спаренные основания — пара двух азотистых оснований нуклеотидов на комплементарных цепочках нуклеиновых кислот, соединённая с помощью водородных связей.

Нозерн-блот — метод исследования экспрессии генов путём тестирования молекул РНК (мРНК) и их фрагментов в образцах.
Трис-ацетатный буфер (TAE) — буферный раствор, содержащий трис, уксусную кислоту и ЭДТА.

Среда LB — богатая среда для роста культур бактерий. Аббревиатура LB часто неверно расшифровывается как Luria broth, Lennox broth, или Среда Luria-Bertani. Согласно автору прописи среды, Джузеппе Бертани, сокращение LB означает англ. lysogeny broth — лизогенная среда. Состав среды LB впервые опубликован в 1951 году в статье Бертани по лизогении. В этой статье описано выделение фагов энтеробактерий P1, P2 и P3 в разработанной им среде для оптимального роста Shigella и образования бляшек фагов.
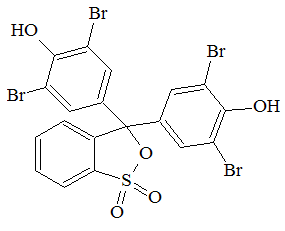
Бромфеноловый синий натуральный краситель, также применяемый в лабораторной практике как pH-индикатор и маркёр при проведении электрофореза.

HEPES представляет собой цвиттер-ионный органический буферный агент; один из двадцати в списке буферных растворов Гуда. HEPES широко используется в работах, связанными с клеточными культурами, главным образом потому, что лучше поддерживает физиологический рН, несмотря на изменения концентрации диоксида углерода по сравнению с бикарбонатными буферами, которые также широко используются в данной сфере. При уменьшении температуры диссоциация воды уменьшается, а константы диссоциации (pK) многих буферов при этом существенно не меняются. У HEPESа подобно воде уменьшается диссоциация при понижении температуры. Это делает HEPES более эффективным буферным агентом для поддержания структуры и функции ферментов при низких температурах. Однако, в публикации Лепе-Зунига и соавт. сообщалось о фототоксичности HEPES, когда под воздействием света образуется перекись водорода, чего не происходит в бикарбонатных клеточных буферах. Поэтому настоятельно рекомендуется как можно меньше подвергать раствор воздействию света.












