
Митохондриа́льная ДНК (мтДНК) — ДНК, находящаяся в митохондриях, органеллах эукариотических клеток.
Митохондриа́льные заболева́ния — группа наследственных заболеваний, связанных с дефектами в функционировании митохондрий, приводящими к нарушениям энергетических функций в клетках эукариот, в частности, человека. На 2021 год известно более 350 генов, приводящих к таким заболеваниям.
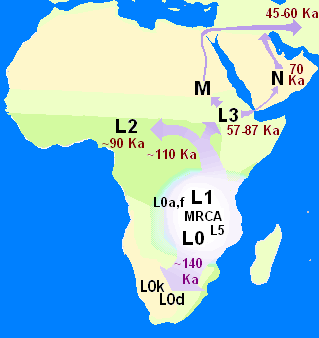
Митохондриальная Ева — имя, данное в популярной культуре женщине, от которой всё современное человечество унаследовало митохондриальную ДНК. Жила в Африке около 200 000 лет назад. Эта женщина стала единственной в своём поколении, чьи потомки по женской линии дожили до наших дней. Параллельно с ней жили и другие женщины, но их митохондриальные ДНК до нашего времени не дошли.

Гаплогруппа T — в популяционной генетике — гаплогруппа митохондриальной ДНК человека.
Митохондриальная тРНК лейцина 1 — тРНК человека, кодируемая митохондриальным геном MT-TL1. Представляет собой молекулу транспортной РНК длиной в 75 нуклеотидов, основной функцией MT-TL1 является перенос остатка аминокислоты лейцина к растущей полипептидной цепочке при трансляции митохондриальных мРНК на рибосомах митохондрий.
Наследуемый по материнской линии синдром сахарного диабета и глухоты (MIDD), или просто Диабет и глухота (DAD), — митохондриальное заболевание, вызываемое мутациями генов MTTL1, MTTE и MTTK. Собственно сахарный диабет при этом заболевании может развиваться довольно медленно; обычно ему предшествует нейросенсорное снижение слуха.

Синдром MELAS — прогрессирующее нейродегенеративное заболевание, характеризующееся проявлениями, перечисленными в названии, и сопровождается полиморфной симптоматикой — диабетом, судорогами, снижением слуха, сердечными заболеваниями, низким ростом, эндокринопатиями, непереносимостью физических нагрузок и нейропсихиатрическими отклонениями. В каждом конкретном случае набор симптомов и их тяжесть может сильно отличаться, поскольку синдром связан с мутациями во многих генах: MTTL1, MTTQ, MTTH, MTTK, MTTS1, MTND1, MTND5, MTND6, MTTS2. Мутации могут возникать впервые у конкретного пациента, либо наследоваться по материнской линии. Всего к 2009 году было обнаружено 23 миссенсных точечных мутаций и 4 делеции мтДНК, приводящих к MELAS, однако продолжаются сообщения о новых пациентах с симптомами расстройства при отсутствии известных мутаций.
Насле́дование — передача генетической информации от одного поколения организмов к другому. В основе наследования лежат процессы удвоения, объединения и распределения генетического материала, поэтому закономерности наследования у разных организмов зависят от особенностей этих процессов.

Свободнорадикальная теория старения утверждает, что старение происходит из-за накопления повреждений в клетках, нанесённых свободными радикалами с течением времени.
Наследственная оптическая нейропатия LHON Лебера, или атрофия зрительного нерва Лебера , является наследственной митохондриальной дегенерацией ганглионарных клеток (РСК) сетчатки и их аксонов, что приводит к острой или почти острой потере центрального зрения; это влияет преимущественно на молодых мужчин. Тем не менее, LHON передается только по материнской линии, прежде всего, из-за мутаций в митохондриальном геноме, и только яйцеклетка способствует митохондрии в зародыше. LHON, как правило, связана с одной из трех патогенных митохондриальных ДНК (мтДНК) точечных мутаций. Эти мутации действуют на нуклеотиды и репозиционируют 11778 G в А, 3460 G в А и 14484 T в C, соответственно, в ND4, ND1 и Nd6 субъединицах генов в комплексе I окислительного фосфорилирования цепочек в митохондриях. Мужчины не могут передать болезнь своему потомству.
Хроническая прогрессирующая внешняя офтальмоплегия (CPEO), также известная как прогрессирующая внешняя офтальмоплегия (ПЭО), является типом расстройства глаз, характеризующимся медленно прогрессирующей невозможностью перемещения глаз и бровей. Это часто единственная особенность этого митохондриального заболевания, в этом случае термин CPEO может быть использован как диагноз. У других людей, страдающих от митохондриальной болезни, CPEO происходит в рамках синдрома с участием более чем одной части тела, например, синдром Кернс-Сейр. Изредка CPEO может быть вызвана условиями, отличными от митохондриальных заболеваний.
Синдро́м Ке́рнса — Се́йра (англ. Kearns–Sayre syndrome, сокращённо KSS) — митохондриальная миопатия с типичным началом до 20-летнего возраста. KSS является более серьёзным синдромным вариантом хронической прогрессирующей внешней офтальмоплегии, синдром, который характеризуется изолированным поражением мышц, контролирующих движения век и контролирующих движения глаз. Это приводит к птозу и офтальмоплегии соответственно. KSS включает в себя триаду уже описанных CPEO, двустороннюю пигментную ретинопатию и блокаду сердца. Другие области участия могут включать в себя мозжечковую атаксию, проксимальную мышечную слабость, глухоту, сахарный диабет, дефицит гормона роста, гипопаратиреоз или другие эндокринные нарушения. В обоих этих заболеваниях вовлечение мышц может начаться односторонним, но всегда развивается в двусторонний дефицит, который является прогрессирующим.

Нибрин, также известный как NBN или Nbs1 — белок, кодируемый у человека геном NBN.

Цитохро́м-bс1-ко́мплекс или убихинол-цитохром с-оксидоредуктаза, или комплекс III — мультибелковый комплекс дыхательной цепи переноса электронов и важнейший биохимический генератор протонного градиента на мембране митохондрий. Этот мультибелковый трансмембранный комплекс кодируется митохондриальным и ядерным геномами.

Баркоди́рование ДНК — метод молекулярной идентификации, который позволяет по коротким генетическим маркерам в ДНК определять принадлежность организма к определённому таксону. В отличие от методов молекулярной филогенетики, ДНК-баркодирование используется для определения места данного организма в уже существующей классификации, а не для построения филогенетических деревьев и дополнения уже существующей классификации, поэтому вопрос об использовании баркодирования ДНК для идентификации видовой принадлежности нового организма является спорным. Наиболее часто используемым локусом генетического баркодинга для животных является участок митохондриального гена цитохромоксидазы I из примерно 600 пар нуклеотидов.

Негомологи́чное соедине́ние концо́в, или негомологи́чное воссоедине́ние концо́в — один из путей репарации двунитевых разрывов в ДНК. Негомологичным этот процесс называется потому, что повреждённые концы цепи соединяются лигазой напрямую, не нуждаясь в гомологичном шаблоне, в отличие от процесса гомологичной рекомбинации. NHEJ существенно менее точен, чем гомологичная рекомбинация, и часто он приводит к потере нуклеотидов, транслокациям или слиянию теломер, при этом последние два могут являться признаками опухолевой клетки. NHEJ обнаружен у представителей всех царств живой природы, кроме того, в клетках млекопитающих он служит основным путём репарации двуцепочечных разрывов.
Митофа́гия — селективное разрушение митохондрий путём аутофагии. Впервые этот термин был введён J. J. Lemasters в 2005 году, хотя ещё с 1962 года было известно о том, что лизосомы клеток печени содержат фрагменты митохондрий, а в 1977 году при изучении метаморфоза тутового шелкопряда было отмечено, что функциональные изменения митохондрий могут вызывать аутофагию. Митофагия необходима для поддержания жизнедеятельности клетки, она способствует кругообороту митохондрий и предотвращает накопление нефункциональных митохондрий, которые могут привести к дегенерации клетки. У дрожжей митофагия опосредуется белком Atg32, а у млекопитающих регуляция митофагии осуществляется белками PINK1 и паркином. Митофагия не приурочена только к повреждённым митохондриям, в ней могут участвовать и неповреждённые митохондрии.
Сомати́ческая гипермута́ция — один из молекулярных механизмов, обеспечивающих разнообразие антител. За счёт соматической гипермутации создаётся разнообразие B-клеточных рецепторов и антител, благодаря чему увеличивается спектр антигенов, которые может распознать адаптивная иммунная система. В ходе соматической гипермутации в вариабельных участках генов иммуноглобулинов происходит множество точечных мутаций. В отличие от мутаций в клетках зародышевой линии, мутации, появившиеся в результате соматической гипермутации, не передаются потомкам и имеются только в геномах B-клеток. Если соматическая гипермутация затрагивает участки, отличные от тех, которые кодируют вариабельные домены иммуноглобулинов, развиваются B-клеточные лимфомы и другие формы онкологических заболеваний.

Трёхцепочечная ДНК, H-ДНК или три́плекс-ДНК — форма ДНК, в которой три олигонуклеотида обвивают друг друга, формируя тройную спираль. В трёхцепочечной ДНК третья цепь ДНК связывается с двуцепочечной B-формой ДНК, сформированной за счёт уотсон—криковских взаимодействий, с помощью хугстиновских взаимодействий или обратных хугстиновских водородных связей. Трёхцепочечная ДНК может мешать нормальной репликации и повышать частоту мутаций в области формирования.
"Эгоистичная" митохондриальная ДНК — мутантная мтДНК, потерявшая большую часть генов или другим способом утратившая полезные для клетки свойства, но получившая эволюционное преимущество. Митохондрии являются потомками бактерий, и из-за этого имеют собственную ДНК и клеточную машинерию. Различные копии их ДНК конкурируют друг с другом внутри клетки, и возникающие мутации могут способствовать быстрому размножению соответствующей мтДНК. Подобная ДНК может вытеснять варианты без мутаций из клетки, приводя к ухудшению общего состояния организма, создавая таким образом митохондриально-ядерный конфликт: несовпадение эволюционных интересов клеточной (ядерной) и митохондриальной ДНК. Следовательно, она соответствует двум критериям, необходимым для присвоения статуса эгоистичного генетического элемента: имеет преимущество перед обычной ДНК и является вредоносной для носителя.










