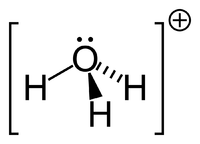
Вода́ (в химии — монооксид водорода, гидроксид водорода; химическая формула — H2O) — химическое вещество, представляющее собой бинарное неорганическое соединение, молекула которого состоит из двух атомов водорода и одного атома кислорода, соединённых между собой ковалентной связью. Вода является продуктом горения (окисления) водорода при реакции с кислородом, но также может выступать конечным результатом и иных химических реакций, таких как горение углеводородов и других органических соединений.

Аммиа́к (нитрид водорода, аммониа́к, химическая формула — NH3) — бинарное неорганическое химическое соединение, молекула которого состоит из одного атома азота и трёх атомов водорода.

Водоро́д — химический элемент первого периода периодической таблицы химических элементов Д. И. Менделеева, с атомным номером 1.
Кисло́ты — химические соединения, способные отдавать катион водорода, либо соединения, способные принимать электронную пару с образованием ковалентной связи.

Водоро́дный показа́тель (pH [пэ-аш] ← лат. pondus Hydrogenii «вес водорода») — мера кислотности водных растворов. Является способом выражения активности катионов водорода в растворах. Противоположна по знаку и равна по модулю десятичному логарифму активности (а) катионов водорода (Н+), выраженной в молях на литр, которую в сильно разбавленных растворах можно считать равной их равновесной молярной концентрации ([H+]):
 .
.
Ио́нное произведе́ние воды́ (KW) — произведение концентраций ионов водорода Н+ и гидроксид-ионов OH− в воде или в водных растворах, константа автопротолиза воды.


Гидрази́н  — неорганическое вещество, бесцветная, чрезвычайно токсичная, сильно гигроскопичная жидкость с неприятным запахом.
— неорганическое вещество, бесцветная, чрезвычайно токсичная, сильно гигроскопичная жидкость с неприятным запахом.

Аммоний — полиатомный катион с химической формулой  . Аммоний с анионами образует соли аммония, аммониевые соединения, последние входят в большой класс ониевых соединений. Ион аммония NH4+ является правильным тетраэдром с азотом в центре и атомами водорода в вершинах тетраэдра. Размер иона — 1,43 Å.
. Аммоний с анионами образует соли аммония, аммониевые соединения, последние входят в большой класс ониевых соединений. Ион аммония NH4+ является правильным тетраэдром с азотом в центре и атомами водорода в вершинах тетраэдра. Размер иона — 1,43 Å.
Амфоте́рность — способность некоторых химических веществ и соединений проявлять в зависимости от условий как кислотные, так и осно́вные свойства.

Бро́моводоро́д — неорганическое вещество, бинарное соединение брома с водородом. Бесцветный тяжёлый токсичный газ, образует туман в сыром воздухе.
Бу́ферные раство́ры — растворы с определённой устойчивой концентрацией водородных ионов, рН которых мало изменится при прибавлении к ним небольших количеств сильного основания или сильной кислоты, а также при разбавлении и концентрировании.
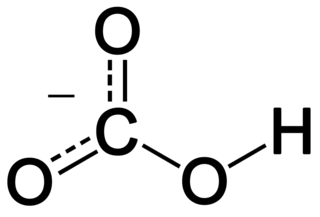
Гидрокарбона́ты — кислые соли угольной кислоты H2CO3. Формула аниона: HCO−
3. Устаревшие названия гидрокарбонатов: кислый, углекислый, двууглекислый, бикарбонаты.
Тео́рии кисло́т и основа́ний — совокупность фундаментальных физико-химических представлений, описывающих природу и свойства кислот и оснований. Все они вводят определения кислот и оснований — двух классов веществ, реагирующих между собой. Задача теории — предсказание продуктов реакции между кислотой и основанием и возможности её протекания, для чего используются количественные характеристики силы кислоты и основания. Различия между теориями лежат в определениях кислот и оснований, характеристики их силы и, как следствие — в правилах предсказания продуктов реакции между ними. Все они имеют свою область применимости, каковые области частично пересекаются.
Автопротолиз — гомофазный процесс самоионизации, обратимый процесс передачи протона от одной нейтральной молекулы жидкости к другой и образования в результате равного числа катионов и анионов.

Фторид аммония — неорганическое соединение, соль аммония и фтористоводородной кислоты с формулой NH4F, бесцветные кристаллы, растворимые в воде, образует кристаллогидрат.
Основания — химические соединения, способные образовывать ковалентную связь с протоном либо с вакантной орбиталью другого химического соединения. В узком смысле, под основаниями понимают осно́вные гидроксиды — сложные вещества, при диссоциации которых в водных растворах отщепляется только один вид анионов — гидроксид-ионы OH−.
Электрофил — реагент или молекула, имеющая свободную орбиталь на внешнем электронном уровне. Как правило такие реагенты являются акцепторами пары электронов при образовании химической связи с нуклеофилом, являющимся донором электронной пары и вытесняет уходящую группу в виде положительно заряженной частицы. Все электрофилы являются кислотами Льюиса.

Гидрон (англ. Hydron) - общее название для катионной формы атома водорода, представляемый в таблице символом Н+. Термин "Гидрон", одобренный ИЮПАК, объединяет катионы водорода независимо от их изотопного состава. То есть, он относится к протонам (1H+) для изотопов протия, дейтронам (2H+ или D+) для изотопов дейтерия, и тритонам (3H+ или T+) для изотопов трития
Теория Брёнстеда–Лоури — это кислотно-основная теория, которая была предложена независимо друг от друга учёными Брёнстедом Йоханнесом Николаусом и Лоури Томасом Мартином в 1923 году. Фундаментальная основа этой теории в том, что когда кислота и основание реагируют друг с другом, кислота образует сопряженное основание, а основание образует сопряженную кислоту с помощью обмена протоном (катионом водорода или H+). Эта теория является обобщением теории Аррениуса.