
Кислоро́д — химический элемент 16-й группы второго периода периодической системы Д. И. Менделеева с атомным номером 8.

Окси́д (синонимы: о́кисел, о́кись) — бинарное соединение химического элемента с кислородом в степени окисления −2, в котором сам кислород связан только с менее электроотрицательным элементом. Химический элемент кислород по электроотрицательности второй после фтора, поэтому к оксидам относятся почти все соединения химических элементов с кислородом. К исключениям относятся, например, дифторид кислорода OF2.
Сте́пень окисле́ния — вспомогательная условная величина для записи процессов окисления, восстановления и окислительно-восстановительных реакций. Она указывает на состояние окисления отдельного атома молекулы и представляет собой лишь удобный метод учёта переноса электронов: она не является истинным зарядом атома в молекуле.

Водородная связь — форма ассоциации между электроотрицательным атомом и атомом водорода H, связанным ковалентно с другим электроотрицательным атомом. Характерными примерами таких электроотрицательных атомов являются атомы элементов второго периода периодической системы — азота, кислорода и фтора, а также атомы некоторых других элементов с высокой относительно водорода электроотрицательностью. Водородные связи могут быть межмолекулярными или внутримолекулярными.
Кисло́ты — химические соединения, способные отдавать катион водорода, либо соединения, способные принимать электронную пару с образованием ковалентной связи.
Неоргани́ческие (минера́льные) кисло́ты — неорганические вещества, обладающие комплексом физико-химических свойств, которые присущи кислотам. Вещества кислотной природы известны для большинства химических элементов за исключением щелочных и щёлочноземельных металлов.
Восстановление, в химии, — это процесс, в результате которого:
- частица принимает один или несколько электронов;
- происходит понижение степени окисления какого-либо атома в данной частице;
- органическое вещество теряет атомы кислорода и (или) приобретает атомы водорода.
Перокси́ды или пе́рекиси — сложные химические соединения, в которых атомы кислорода соединены друг с другом, в результате чего молекула кислорода в общем анионе O2−2 имеет степень окисления −1.

Свободные радикалы в химии — частицы, содержащие один или несколько неспаренных электронов на внешней электронной оболочке. Свободные радикалы бывают твёрдыми, жидкими и газообразными веществами и могут существовать от очень короткого до очень долгого времени. Радикалы могут быть не только нейтральными, но и ионными, а также иметь более одного неспаренного электрона. Свободные радикалы обладают парамагнитными свойствами и являются очень реакционноспособными частицами.

Гидроксильная группа — функциональная группа OH органических и неорганических соединений, в которой атомы водорода и кислорода связаны ковалентной связью. В органической химии носит также название «спиртовой группы».

Анаэробы — организмы, получающие энергию при отсутствии доступа кислорода путём субстратного фосфорилирования, конечные продукты неполного окисления субстрата при этом могут быть окислены с получением большего количества энергии в виде АТФ.
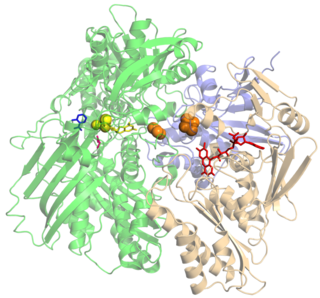
Ксантиноксидаза (ксантиноксидоредуктаза, КФ 1.17.3.2) — молибден-содержащая оксидоредуктаза, фермент, катализирующий окисление гипоксантина в ксантин и ксантина в мочевую кислоту:
- гипоксантин + O2 + H2O <-> ксантин + H2O2
- ксантин + O2 + H2O <-> мочевая кислота + H2O2

Супероксиддисмутаза относится к группе антиоксидантных ферментов. Вместе с каталазой и другими антиоксидантными ферментами она защищает организм человека от постоянно образующихся высокотоксичных кислородных радикалов. Супероксиддисмутаза катализирует дисмутацию супероксида в кислород и пероксид водорода. Таким образом, она играет важнейшую роль в антиоксидантной защите практически всех клеток, так или иначе находящихся в контакте с кислородом. Одним из редких исключений является молочнокислая бактерия Lactobacillus plantarum и родственные ей молочнокислые бактерии, использующие иной механизм защиты от образующегося супероксида.
Дыхательная цепь переноса электронов, также электрон-транспортная цепь (сокр. ЭТЦ, англ. ETC, Electron transport chain) — система трансмембранных белков и переносчиков электронов, необходимых для поддержания энергетического баланса. ЭТЦ поддерживает баланс за счёт переноса электронов и протонов из НАД∙Н и ФАДН2 в акцептор электронов. В случае аэробного дыхания акцептором может быть молекулярный кислород (О2). В случае анаэробного дыхания акцептором могут быть NO3−, NO2−, Fe3+, фумарат, диметилсульфоксид, сера, SO42−, CO2 и т. д. ЭТЦ у прокариот локализована в ЦПМ, у эукариот — на внутренней мембране митохондрий. Переносчики электронов расположены в порядке уменьшения сродства к электрону, то есть по своему окислительно-восстановительному потенциалу, где у акцептора самое сильное сродство к электрону. Поэтому транспорт электрона на всём протяжении цепи протекает самопроизвольно с выделением энергии. Выделение энергии в межмембранное пространство при переносе электронов происходит ступенчато, в виде протона (H+). Протоны из межмембранного пространства попадают в протонную помпу, где наводят протонный потенциал. Протонный потенциал преобразуется АТФ-синтазой в энергию химических связей АТФ. Сопряжённая работа ЭТЦ и АТФ-синтазы носит название окислительного фосфорилирования.

Трифенилметил — стабильный свободный радикал и первый радикал, описанный в органической химии. Трифенилметил может быть получен гомолитическим разложением трифенилметилхлорида 1 металлами, например, серебром или цинком, в бензоле или диэтиловом эфире. Радикал 2 находится в химическом равновесии с димером 3. В бензоле концентрация радикала составляет 2 %.
Нитроксильные радикалы — органические радикалы, содержащие нитроксильную группу N-O·. Впервые открыты в 1951 г. Первый синтез соединения 2,2,6,6-тетраметил-4-пиперидон-1-оксил (4-оксо-TEMPO) был выполнен О.Л. Лебедевым в 1959 г.

Индан-1,3-дион — органическое вещество, представитель ненасыщенных транс-фиксированных β-дикетонов. В кристаллическом виде бесцветное или желтоватое и существует в форме именно дикетона. В водном же растворе частично енолизирован. Значительный вклад в развитие химии индандиона и его производных внёс профессор РТУ Г. Я. Ванаг — основатель рижской школы химиков-органиков.

Триоксид диводорода (триоксид водорода, триоксидан) — неорганическое соединение состава H2O3, простейший представитель класса полиоксидов (в т.ч. гидротриоксидов и триоксидов). Может рассматриваться как высший гомолог пероксида водорода H2O2.
Оксигеназы — ферменты, катализирующие реакции присоединения одного (монооксигеназы) либо двух (диоксигеназы) атомов кислорода к молекуле субстрата, источником кислорода в этом случае является молекулярный кислород; являются подклассом класса оксидоредуктаз.
Алан Ка́ррингтон — английский учёный-физикохимик, один из наиболее известных спектроскопистов Великобритании XX века.
 HO2 + OH−
HO2 + OH−











