Иодид циркония(IV)
| Иодид циркония(IV) | |
|---|---|
 | |
| Общие | |
| Систематическое наименование | иодид циркония(IV) |
| Традиционные названия | иодистый цирконий |
| Хим. формула | ZrI4 |
| Физические свойства | |
| Состояние | жёлто-оранжевые кристаллы |
| Молярная масса | 598,84 г/моль |
| Плотность | 4,76; 4,85 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | под давл. 500 °C |
| • кипения | возг. 418 °C |
| Мол. теплоёмк. | 123 Дж/(моль·К) |
| Энтальпия | |
| • образования | −482 кДж/моль |
| Классификация | |
| Рег. номер CAS | 13986-26-0 |
| PubChem | 518853 и 84133 |
| Рег. номер EINECS | 237-780-9 |
| SMILES | |
| InChI | |
| ChemSpider | 75903 |
| Безопасность | |
| NFPA 704 | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Иодид циркония(IV) — неорганическое соединение, соль металла циркония и иодоводородной кислоты с формулой ZrI4, жёлто-оранжевые кристаллы, реагирует с водой.
Получение
- Реакция иода и порошкообразного циркония:
- Пропускание иодоводорода над порошкообразным цирконием:
- Вместо циркония можно использовать его карбид:
Физические свойства
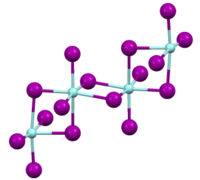
Иодид циркония(IV) образует жёлто-оранжевые кристаллы. Имеет две кристаллические модификации альфа - с параметрами ячейки P2/ a=8.35A, b=8.32A ,c = 17.92A и гамма модификация , кристаллизующаяся в P -1 a=8.348A, b= 8.343,c= 23.28 и углы 90.59(4) 90.50(4) 90.04(3).
В воде подвергается полному гидролизу. Растворяется в этаноле, бензоле и диэтиловом эфире.
Химические свойства
- Разлагается при нагревании:
- Реагирует с водой:
- Реагирует с концентрированной серной кислотой:
- Реагирует с щелочами:
- При нагревании реагирует с аммиаком с образованием нитрида циркония(III):
Литература
- Химическая энциклопедия / Редкол.: Зефиров Н.С. и др.. — М.: Большая Российская энциклопедия, 1998. — Т. 5. — 783 с. — ISBN 5-85270-310-9.
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 3-е изд., испр. — Л.: Химия, 1971. — Т. 2. — 1168 с.
- Лидин Р.А. и др. Химические свойства неорганических веществ: Учеб. пособие для вузов. — 3-е изд., испр. — М.: Химия, 2000. — 480 с. — ISBN 5-7245-1163-0.
- Рипан Р., Четяну И. Неорганическая химия. Химия металлов. — М.: Мир, 1972. — Т. 2. — 871 с.







![{\displaystyle {\mathsf {ZrI_{4}+4H_{2}SO_{4}\ {\xrightarrow {}}\ H_{2}[ZrO(SO_{4})_{2}]+2I_{2}\downarrow +2SO_{2}\uparrow +3H_{2}O}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/f6da8ce98899fd964ac276e0787f31f8011c8edb)