Капролактам
| Капролактам | |||
|---|---|---|---|
| |||
| Общие | |||
| Систематическое наименование | азепан-2-он | ||
| Традиционные названия | капролактам | ||
| Хим. формула | C6H11NO | ||
| Физические свойства | |||
| Состояние | твёрдое | ||
| Молярная масса | 113,16 г/моль | ||
| Плотность | 1,01 г/см³ | ||
| Энергия ионизации | 9,07 эВ[2] | ||
| Термические свойства | |||
| Температура | |||
| • плавления | 68,8 °C | ||
| • кипения | 270 °C | ||
| • вспышки | 282 ± 1 ℉[1] | ||
| Пределы взрываемости | 1,4 ± 0,1 об.%[1] | ||
| Давление пара | 8,0E−8 ± 1,0E−8 мм рт.ст.[1] | ||
| Классификация | |||
| Рег. номер CAS | 105-60-2 | ||
| PubChem | 7768 | ||
| Рег. номер EINECS | 203-313-2 | ||
| SMILES | |||
| InChI | |||
| RTECS | CM3675000 | ||
| ChEBI | 28579 | ||
| ChemSpider | 7480 | ||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
Капролактам (гексагидро-2H-азепин-2-он) — циклический амид (лактам) ε-аминокапроновой кислоты, бесцветные кристаллы; Τкип = 262,5 °C, Τпл = 68—69 °C.
Свойства
Белые кристаллы, хорошо растворимые в воде, спирте, эфире, бензоле. Капролактам — циклический амид ε-аминокапроновой кислоты. В промышленности для производства капролактама исходным сырьём служит бензол. При нагревании в присутствии небольших количеств воды, спирта, аминов, органических кислот и некоторых других соединений капролактам полимеризуется с образованием полиамидной смолы, из которой получают волокно капрон.
Водные растворы кислот и щелочей вызывают гидролиз капролактама до ε-аминокапроновой кислоты.
До января 2019 года капролактам являлся единственным веществом, занесённым агентством по изучению рака в список неканцерогенных веществ (группа 4) [3]. В 2019 году агентство исключило группу 4 из классификации [4], и перенесло капролактам в группу 3 ("не классифицируемые как канцерогенные для человека вещества") [5].
Получение
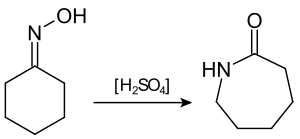
Существует несколько промышленных методов синтеза капролактама, все они на завершающей стадии технологической цепи включают перегруппировку Бекмана циклогексаноноксима в капролактам при действии олеума или концентрированной серной кислоты при 60—120 °C:
Побочным продуктом на этой стадии является сульфат аммония, используемый в качестве минерального удобрения.
В свою очередь, существует несколько методов синтеза циклогексаноноксима, в которых качестве исходного сырья могут использоваться фенол, бензол или толуол, что и определяет технологические схемы производств.
Фенольный процесс
Исторически первым процессом производства капролактама был процесс, использующий в качестве исходного сырья фенол. На первой стадии в этом процессе фенол гидрируется до циклогексанола над катализатором Pd/Al2O3 или Ni-Cr/Al2O3 при 120—140 °C и давлении 1—1,5 МПа либо 130—150 °C и 1,5—2,5 МПа соответственно:
Циклогексанол затем дегидрируется до циклогексанона (1), из которого затем реакцией с избытком водного раствора сульфата гидроксиламина в присутствии щелочи или аммиака при 0—100 °C получают циклогексаноноксим (2) и далее перегруппировкой Бекмана капролактам (3):
Бензольные процессы
Другой группой процессов синтеза капролактама являются процессы, в которых в качестве исходного сырья используется бензол. Они стали разрабатываться позже фенольного, когда мировой рынок насытился ацетоном — побочным продуктом производства фенола, и особенно — позднее, когда фенол, в отличие от бензола, стал дефицитным. Один из таких процессов был разработан в середине XX века в Государственном научно-исследовательском и проектном институте азотной промышленности и продуктов органического синтеза (ГИАП)[6].
Первой стадией этих процессов является каталитическое гидрирование бензола до циклогексана над Pt/Al2O3 или никель-хромовым катализатором при 250—350 и 130—220 °C соответственно.
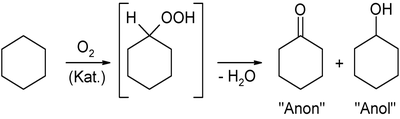
В наиболее распространённом бензольном процессе далее проводят жидкофазное каталитическое окисление циклогексана в циклогексанол («анол», в качестве примеси при этом образуется циклогексанон — «анон»):
и дальнейшего дегидрирования циклогексанола в циклогексанон (на цинк-хромовых при 360—400 °C, цинк-железных при 400 °C или медь-магниевых при 260—300 °C катализаторах), который через оксим затем превращается в капролактам. Выход капролактама ~85—88 % в пересчёте на бензол.
При методе прямого оксимирования циклогексан, полученный гидрированием бензола, нитрозируют нитрозилхлоридом при ультрафиолетовом облучении, получающийся нитрозоциклогексан in situ таутомеризуется в циклогексаноноксим.
Толуольный процесс
При синтезе капролактама из толуола первой стадией является окисление толуола до бензойной кислоты, катализируемое бензоатом кобальта, затем бензойную кислоту гидрируют до циклогексилкарбоновой кислоты при 170 °C и 1,4—1,5 МПа (катализатор — палладий на угле).
Циклогексилкарбоновая кислота далее нитрозируется нитрозилсерной кислотой при 75—80 °C. Реакция нитрозирования сопровождается декарбоксилированием, перегруппировкой образовавшегося нитрозоциклогексана в циклогексаноноксим и его перегруппировкой в капролактам под действием высвобождающейся при нитрозировании серной кислоты. Поскольку при нитрозировании на одной технологической стадии происходят четыре последовательных реакции, процесс недостаточно селективен и получаемый этим методом капролактам-сырец нуждается в дополнительной сложной очистке. Выход капролактама ~70 % в расчёте на толуол.
Techni-Chem процесс
В процессе Techni-Chem на первой стадии ацилируют циклогексанон кетеном с образованием циклогексенилацетата, который затем нитруют с отщеплением уксусной кислоты, получая 2-нитроциклогексанон.
2-Нитроциклогексанон затем подвергается гидролизу с образованием ε-нитрокапроновой кислоты, которую восстанавливают до ε-аминокапроновой кислоты; последнюю дегидратируют в капролактам при 300 °C и давлении 100 бар.
Главным преимуществом Techni-Chem процесса является минимизация образования побочных продуктов: уксусная кислота, отщепляющаяся при нитровании циклогексенилацетата, может быть пиролизована в кетен[7].
Применение
Капролактам используется, в основном, для получения полиамидных пластмасс и волокон (капрон, нейлон, полиамид). Полиамидные волокна и нити, как правило, применяются в производстве текстиля, ковровых покрытий, промышленных нитей, используемых в свою очередь для изготовления шинного корда. Кордная нить — крупнейший и наиболее быстрорастущий сегмент рынка ПА6.
Основная часть мирового потребления приходится на нити и волокна, значительное количество потребляется также в производстве конструкционных пластмасс. Остальной объём используется для изготовления упаковочных плёнок и других материалов.
Смола ПА6 также является основной для производства конструкционных пластиков, используемых для производства компонентов электронной и электрической техники, автомобильных деталей.
В упаковочной отрасли применяется ориентированная полиамидная плёнка, также изготовленная на основе смолы ПА6.
Небольшие объёмы капролактама уходят на синтез лизина, а также в качестве агента в производстве полиуретана.
Примечания
- ↑ 1 2 3 http://www.cdc.gov/niosh/npg/npgd0097.html
- ↑ David R. Lide, Jr. Basic laboratory and industrial chemicals (англ.): A CRC quick reference handbook — CRC Press, 1993. — ISBN 978-0-8493-4498-5
- ↑ Agents Classified by the IARC Monographs Архивная копия от 25 октября 2011 на Wayback Machine (англ.) (стр. 31)
- ↑ Proposed update to the Preamble to the IARC Monographs (англ.). Дата обращения: 25 марта 2024. Архивировано 4 июля 2022 года.
- ↑ List of Classifications (амер. англ.). monographs.iarc.who.int. Дата обращения: 25 марта 2024. Архивировано 5 апреля 2021 года.
- ↑ Владимиров С. Капрон из бензола // Химия и жизнь. — 1965. — № 1. — С. 28—29.
- ↑ Weissermel, Klaus; Arpe, Hans-Jürgen. Industrial Organic Chemistry (неопр.). — John Wiley & Sons, 2003. — С. 258. — ISBN 978-3-527-30578-0.
Литература
- Производство капролактама /Под ред. В. И. Овчинникова и В. Р. Ручинского. «Химия», М. 1977