
Физи́ческая хи́мия — раздел химии, наука об общих законах строения, структуры и превращения химических веществ. Исследует химические явления с помощью теоретических и экспериментальных методов физики. Наиболее обширный раздел химии.

Ферме́нты, или энзи́мы , — обычно сложные белковые соединения, РНК (рибозимы) или их комплексы, ускоряющие химические реакции в живых системах. Каждый фермент, свернутый в определённую структуру, ускоряет соответствующую химическую реакцию: реагенты в такой реакции называются субстратами, а получающиеся вещества — продуктами. Ферменты специфичны к субстратам: АТФ-аза катализирует расщепление только АТФ, а киназа фосфорилазы фосфорилирует только фосфорилазу.

Аналити́ческая хи́мия — наука, развивающая теоретические основы химического анализа веществ и материалов и разрабатывающая методы идентификации, обнаружения, разделения и определения химических элементов и их соединений, а также методы установления химического состава веществ. Проведение химического анализа в настоящее время заключается в получении информации о составе и природе вещества.

Катализа́тор — химическое вещество, ускоряющее реакцию, но не расходующееся в процессе реакции.
Ингиби́тор — общее название веществ, подавляющих или задерживающих течение физиологических и физико-химических процессов.

Перокси́д водоро́да (пе́рекись водоро́да, химическая формула — H2O2) — неорганическое химическое соединение водорода и кислорода, являющееся простейшим представителем класса пероксидов.
Гидри́рование (гидрогениза́ция) — химическая реакция, включающая присоединение водорода к органическому веществу. В ходе данной реакции молекула водорода присоединяется к двойной или тройной связи молекулы. Если в результате гидрирования происходит разрыв связи углерод — углерод или углерод — гетероатом, то такой процесс называется гидрогенолизом.

Иммуноферментный анализ — лабораторный иммунологический метод качественного или количественного определения различных низкомолекулярных соединений, макромолекул, вирусов и пр., в основе которого лежит специфическая реакция антиген-антитело. Выявление образовавшегося комплекса проводят с использованием фермента в качестве метки для регистрации сигнала. Теоретические основы ИФА опираются на современную иммунохимию и химическую энзимологию, знание физико-химических закономерностей реакции антиген-антитело, а также на основные принципы аналитической химии.

Элементный анализ — качественное обнаружение и количественное определение содержания элементов и элементного состава веществ, материалов и различных объектов. Это могут быть жидкости, твёрдые материалы, газы и воздух. Элементный анализ позволяет ответить на вопрос — из каких атомов (элементов) состоит анализируемое вещество.

Титриметрический анализ (титрование) — метод количественного/массового анализа, который часто используется в аналитической химии, основанный на измерении объёма раствора реактива точно известной концентрации, расходуемого для реакции с определяемым веществом. Титрование — процесс определения титра исследуемого вещества. Титрование производят с помощью бюретки, заполненной титрантом до нулевой отметки. Титровать начиная от других отметок не рекомендуется, так как шкала бюретки может быть неравномерной. Заполнение бюреток рабочим раствором производят через воронку или с помощью специальных приспособлений, если бюретка полуавтоматическая. Конечную точку титрования определяют с помощью индикаторов или физико-химическими методами. По количеству затраченного на титрование рабочего раствора рассчитывают результаты анализа.

Полярография — электрохимический метод качественного и количественного анализа и изучения кинетики химических процессов, предложенный в 1922 году чешским химиком Я. Гейровским. За разработку этого метода ему была присуждена в 1959 году Нобелевской премия по химии.
Ката́лиз — избирательное ускорение одного из возможных термодинамически разрешённых направлений химической реакции под действием катализатора(ов), который, согласно теории промежуточных соединений, многократно вступает в промежуточное химическое взаимодействие с участниками реакции и восстанавливает свой химический состав после каждого цикла промежуточных химических взаимодействий.
Автокатализ — катализ химической реакции одним из её продуктов или исходных веществ.
Химическая кинетика или кинетика химических реакций — раздел физической химии, изучающий закономерности протекания химических реакций во времени, зависимости этих закономерностей от внешних условий, а также механизмы химических превращений.
Ско́рость хими́ческой реа́кции — изменение количества одного из реагирующих веществ за единицу времени в единице реакционного пространства. Является ключевым понятием химической кинетики. Скорость химической реакции — величина всегда положительная, поэтому, если она определяется по исходному веществу, то полученное значение умножается на −1.
Фармакокине́тика — раздел фармакологии, изучающий кинетические закономерности химических и биологических процессов, происходящих с лекарственным средством в организме животного или человека.

Фотометрическое титрование — группа методов объёмного (титриметрического) анализа, в которых конечная точка титрования определяется по изменению оптической плотности раствора в ходе химической реакции между титрантом и титруемым веществом.

Осажде́ние, преципита́ция — образование твёрдого осадка в растворе в процессе химической реакции, например, при добавлении соответствующих реагентов. Химическое вещество, вызывающее образование твёрдого вещества, называют «осадителем».
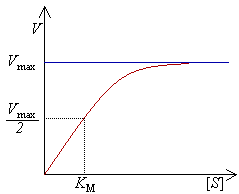
Ферментати́вная кине́тика — зависимость скорости химической реакции от её условий — раздел биохимии, предметом которого являются химические реакции, катализируемые ферментами, изучающий закономерности течения во времени и механизм ферментативных реакций. Ферментативная кинетика занимается исследованием закономерностей влияния химической природы реагентов, количественным изучением эффектов варьирования условий (кинетики) той или иной химической реакции, а также измеряет её скорость. Изучение ферментов позволяет выявить каталитический механизм действия определённого фермента и контролировать его роль в процессе обмена веществ, способного замедлять (ингибировать) или ускорять (активировать) ход химической реакции. Таким образом, кинетические исследования позволяют не только определить сродство и специфичность связывания субстратов и ингибиторов к ферментам, но и найти максимальную скорость процесса, катализируемого специфическим ферментом, а также попутно решить многие другие задачи и возникающие проблемы. При этом, основная часть проблем ферментативной кинетики сводится к:
- анализу предполагаемых схем ферментативных реакций,
- выводу уравнений скорости, соответствующих этим схемам,
- сопоставлению полученных зависимостей с данными эксперимента.

Александр Яковлевич Розовский — химик, лауреат премии имени А. А. Баландина.












