
Со́ли — сложные вещества, состоящие из катионов металлов и анионов кислотных остатков. ИЮПАК определяет соли как химические соединения, состоящие из катионов и анионов. Есть ещё одно определение: солями называют вещества, которые могут быть получены при взаимодействии кислот и оснований с выделением воды.

Окси́д (синонимы: о́кисел, о́кись) — бинарное соединение химического элемента с кислородом в степени окисления −2, в котором сам кислород связан только с менее электроотрицательным элементом. Химический элемент кислород по электроотрицательности второй после фтора, поэтому к оксидам относятся почти все соединения химических элементов с кислородом. К исключениям относятся, например, дифторид кислорода OF2.

Ба́рий — химический элемент 2-й группы шестого периода периодической системы химических элементов Д. И. Менделеева с атомным номером 56.
Кисло́ты — химические соединения, способные отдавать катион водорода, либо соединения, способные принимать электронную пару с образованием ковалентной связи.
Неоргани́ческие (минера́льные) кисло́ты — неорганические вещества, обладающие комплексом физико-химических свойств, которые присущи кислотам. Вещества кислотной природы известны для большинства химических элементов за исключением щелочных и щёлочноземельных металлов.
Oксид кальция — белое кристаллическое вещество, формула CaO. Относится к классу основных оксидов.
Щелочны́е мета́ллы — элементы 1-й группы периодической таблицы химических элементов : литий Li, натрий Na, калий K, рубидий Rb, цезий Cs, франций Fr. Гипотетический 119-й элемент унуненний в случае своего открытия, согласно строению своей внешней электронной оболочки, также будет отнесён к щелочным металлам. При растворении щелочных металлов в воде образуются растворимые гидроксиды, называемые щелочами.
Неорганические сульфиды (от лат. sulphur — сера) — класс химических соединений, представляющих собой соединения металлов (а также ряда неметаллов — В, Si, Р, As) с серой (S), где она имеет степень окисления −2. Могут рассматриваться как соли сероводородной кислоты H2S. Свойства сульфидов сильно зависят от металлов, входящих в их состав.
Осно́вные гидрокси́ды — это сложные вещества, которые состоят из атомов металла или иона аммония и гидроксогруппы (—OH) и в водном растворе диссоциируют с образованием анионов ОН− и катионов. Название основания обычно состоит из двух слов: слова «гидроксид» и названия металла в родительном падеже. Хорошо растворимые в воде основания называются щелочами.
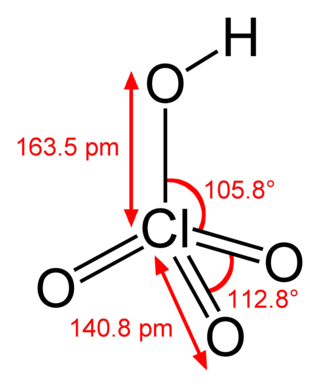
Хло́рная кислота́ (хим. формула — HClO4) — сильная одноосновная кислота.

Щёлочноземе́льные мета́ллы — химические элементы 2-й группы периодической таблицы элементов: бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba), радий (Ra). В случае своего открытия гипотетический 120-й элемент унбинилий, согласно строению внешней электронной оболочки, также будет отнесен к щёлочноземельным металлам.

Реакция нейтрализа́ции — реакция взаимодействия кислоты и основания между собой с образованием соли и слабо диссоциирующего вещества (воды).
Осно́вные окси́ды — солеобразующие оксиды металлов, которым соответствуют основания. Как правило, металлы в них проявляют степень окисления +1 или +2. К ним относятся оксиды щелочных и щёлочноземельных металлов, а также оксиды переходных металлов в низших степенях окисления.
Амфотерные оксиды — солеобразующие оксиды, проявляющие в зависимости от условий либо осно́вные, либо кислотные свойства. Образуются переходными металлами. Металлы в амфотерных оксидах обычно проявляют степень окисления от +3 до +4, за исключением ZnO, BeO, SnO, PbO.

Хлори́д желе́за(III) (хлорное железо, также — трихлорид железа) FeCl3 — средняя соль трёхвалентного железа и соляной кислоты, слабое амфотерное соединение.

Окси́д желе́за(III) (окись железа, колькотар, гематит, крокус; химическая формула — Fe2O3) — сложный неорганический солеобразующий оксид железа со степенью окисления железа +3.

Оксид азота (IV) (диоксид азота, двуокись азота) NO2 — бинарное неорганическое соединение азота с кислородом. Представляет собой ядовитый газ красно-бурого цвета с резким неприятным запахом или желтоватую жидкость.
Тео́рии кисло́т и основа́ний — совокупность фундаментальных физико-химических представлений, описывающих природу и свойства кислот и оснований. Все они вводят определения кислот и оснований — двух классов веществ, реагирующих между собой. Задача теории — предсказание продуктов реакции между кислотой и основанием и возможности её протекания, для чего используются количественные характеристики силы кислоты и основания. Различия между теориями лежат в определениях кислот и оснований, характеристики их силы и, как следствие — в правилах предсказания продуктов реакции между ними. Все они имеют свою область применимости, каковые области частично пересекаются.
Гидроксид стронция — неорганическое основание (щёлочь), состоящее из одного иона стронция и двух гидроксид-ионов, имеющее химическую формулу Sr(OH)2.

Вольфрамат натрия — неорганическое соединение, натриевая соль вольфрамовой кислоты. Бесцветные ромбические кристаллы, растворимые в воде. Образует дигидрат.




























