Глико́лиз, или путь Эмбдена — Мейергофа — Парнаса — процесс окисления глюкозы, при котором из одной молекулы глюкозы образуются две молекулы пировиноградной кислоты. Гликолиз состоит из цепи последовательных ферментативных реакций и сопровождается запасанием энергии в форме АТФ и НАДH. Гликолиз является универсальным путём катаболизма глюкозы и одним из трёх путей окисления глюкозы, встречающихся в живых клетках. Реакция гликолиза в суммарном виде выглядит следующим образом:
- Глюкоза + 2НАД+ + 2АДФ + 2Pi → 2 пируват + 2НАД*H + 2Н+ + 2АТФ + 2Н2O.

Аденозинтрифосфа́т (ион), Аденозинтрифосфорная кислота, АТФ — нуклеозидтрифосфат, играющий основную роль в обмене энергии в клетках живых организмов. Это универсальный источник энергии для всех биохимических процессов, протекающих в живых системах.
Глюконеогене́з — метаболический путь, приводящий к образованию глюкозы из неуглеводных соединений. Наряду с гликогенолизом, этот путь поддерживает в крови уровень глюкозы, необходимый для работы многих тканей и органов, в первую очередь, нервной ткани и эритроцитов. Он служит важным источником глюкозы в условиях недостаточного количества гликогена, например, после длительного голодания или тяжёлой физической работы. Глюконеогенез является обязательной частью цикла Кори, кроме того, этот процесс может быть использован для превращения пирувата, образованного при дезаминировании аминокислот аланина и серина.

Ци́кл трикарбо́новых кисло́т (сокр. ЦТК, цикл Кре́бса, цитра́тный цикл, цикл лимо́нной кислоты́) — центральная часть общего пути катаболизма, циклический биохимический процесс, в ходе которого ацетильные остатки (СН3СО-) окисляются до диоксида углерода (CO2). При этом за один цикл образуется 2 молекулы CO2, 3 НАДН, 1 ФАДH2 и 1 ГТФ (или АТФ). Электроны, находящиеся на НАДН и ФАДH2, в дальнейшем переносятся на дыхательную цепь, где в ходе реакций окислительного фосфорилирования образуется АТФ.

Фосфорилирование — процесс переноса остатка фосфорной кислоты от фосфорилирующего агента-донора к субстрату, как правило, катализируемый ферментами и ведущий к образованию сложных эфиров фосфорной кислоты:
- АТФ + R-OH → АДФ + R-OPO3H2
Катаболи́зм, также энергетический обмен, или диссимиляция — процесс метаболического распада (деградации) сложных веществ на более простые или окисления какого-либо вещества, обычно протекающий с освобождением энергии в виде тепла и в виде молекулы АТФ, универсального источника энергии всех биохимических процессов. Катаболические реакции лежат в основе диссимиляции: утраты сложными веществами своей специфичности для данного организма в результате распада до простых.

Фриц Альберт Ли́пман — немецко-американский биохимик. Лауреат Нобелевской премии по медицине в 1953 году совместно с Хансом Кребсом за открытие кофермента А.
Гидро́лиз — химическая реакция между веществом и водой, в результате которой происходит разложение этого вещества и воды с образованием новых соединений.
Мы́шечное сокраще́ние — реакция мышечных клеток на воздействие нейромедиатора, реже гормона, проявляющаяся в уменьшении длины клетки. Это жизненно важная функция организма, связанная с оборонительными, дыхательными, пищевыми, половыми, выделительными и другими физиологическими процессами.

Мы́шцы, также му́скулы — органы, состоящие из мышечной ткани; способны сокращаться под влиянием нервных импульсов. Часть опорно-двигательного аппарата. Выполняют различные движения, обеспечивая перемещение тела, поддержание позы, сокращение голосовых связок, дыхание и прочее. Мышечная ткань — упруга и эластична; состоит из миоцитов. Для мышц характерно утомление, которое проявляется при интенсивной работе или нагрузке.

Анаэробы — организмы, получающие энергию при отсутствии доступа кислорода путём субстратного фосфорилирования, конечные продукты неполного окисления субстрата при этом могут быть окислены с получением большего количества энергии в виде АТФ.

Окисли́тельное фосфорили́рование — метаболический путь, при котором энергия, образовавшаяся при окислении питательных веществ, запасается в митохондриях клеток в виде АТФ. Хотя различные формы жизни на Земле используют разные питательные вещества, АТФ является универсальным соединением, в котором запасается энергия, необходимая для других метаболических процессов. Почти все аэробные организмы осуществляют окислительное фосфорилирование. Вероятно, широкому распространению этого метаболического пути способствовала его высокая энергетическая эффективность по сравнению с анаэробным брожением.

Ге́рти Тере́за Ко́ри, урождённая Ра́дниц — американский биохимик. Член Национальной академии наук США (1948).

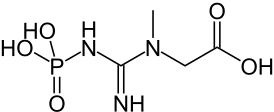
Креати́н — азотсодержащая карбоновая кислота, которая встречается в организме позвоночных. Участвует в энергетическом обмене в мышечных и нервных клетках. Креатин был выделен в 1832 году Шеврёлем из скелетных мышц.
Углеводный обмен, или метаболизм углеводов в организмах животных и человека. Метаболизм углеводов в организме человека состоит из следующих процессов:
- Расщепление в пищеварительном тракте поступающих с пищей поли- и дисахаридов до моносахаридов, дальнейшее всасывание моносахаридов из кишечника в кровь.
- Синтез и распад гликогена в тканях, прежде всего в печени.
- Гликолиз — распад глюкозы. Первоначально под этим термином обозначали только анаэробное брожение, которое завершается образованием молочной кислоты (лактата) или этанола и углекислого газа. В настоящее время понятие «гликолиз» используется более широко для описания распада глюкозы, проходящего через образование глюкозо-6-фосфата, фруктозо-1,6-дифосфата и пирувата как в отсутствие, так и в присутствии кислорода. В последнем случае употребляется термин «аэробный гликолиз», в отличие от «анаэробного гликолиза», завершающегося образованием молочной кислоты или лактата.
- Анаэробный путь прямого окисления глюкозы или, как его называют, пентозофосфатный путь.
- Взаимопревращение гексоз.
- Анаэробный метаболизм пирувата. Этот процесс выходит за рамки углеводного обмена, однако может рассматриваться как завершающая его стадия: окисление продукта гликолиза — пирувата.
- Глюконеогенез — образование углеводов из неуглеводных продуктов.
Общий путь катаболизма — совокупность биохимических процессов, которая включает в себя:
- окисление пирувата до ацетил-КоА;
- окисление ацетил-КоА в цикле трикарбоновых кислот;

Окисли́тельное декарбоксили́рование пирува́та — биохимический процесс, заключающийся в отщеплении одной молекулы углекислого газа (СО2) от молекулы пирувата и присоединении к декарбоксилированному пирувату кофермента А (КоА) с образованием ацетил-КоА; является промежуточным этапом между гликолизом и циклом трикарбоновых кислот. Декарбоксилирование пирувата осуществляет сложный пируватдегидрогеназный комплекс (ПДК), включающий в себя 3 фермента и 2 вспомогательных белка, а для его функционирования необходимы 5 кофакторов. Суммарное уравнение окислительного декарбоксилирования пирувата таково:
Бе́та-окисле́ние (β-окисление), также цикл Кноопа — Линена, — метаболический процесс деградации жирных кислот. Своё название процесс получил по 2-му углеродному атому (С-3 или β-положение) от карбоксильной группы (-СООН) жирной кислоты, который подвергается окислению и последовательному отделению от молекулы. Продуктами каждого цикла β-окисления являются ФАДH2, НАДH и ацетил-КоА. Реакции β-окисления и последующего окисления ацетил-КоА в цикле Кребса служат одним из основных источников энергии для синтеза АТФ по механизму окислительного фосфорилирования.
Субстратное фосфорилирование — характерная для всех живых организмов реакция синтеза АТФ или ГТФ путём прямого переноса фосфата (PO3) на АДФ или ГДФ с высокоэнергетического промежуточного продукта. В ходе окисления органических соединений в живых клетках неорганический фосфат переносится на органическое вещество с образованием богатых энергией молекул, с которых он переносится на АДФ или ГДФ. При этом перенос может происходить только с молекул с достаточно высоким потенциалом переноса групп. Энергия гидролиза химических связей таких молекул должна быть выше чем энергия гидролиза АТФ, чтобы за счёт энергетического сопряжения обеспечить синтез АТФ из АДФ и Фн. К таким молекулам с высоким потенциалом переноса групп принадлежат фосфоенолпируват, 1,3-бисфосфоглицерат, ацильные производные кофермента A и креатинфосфат.

Фосфагены — энергетические субстраты действуют как формы хранения и передачи высокого группового потенциала, также известны как высокоэнергетические (макроэрготические) фосфатсодержащие соединения, включая креатинфосфат, который находится в основном в скелетных мышцах. позвоночных, но также в сердце, сперме и головном мозге и фосфат аргинина, который содержится в мышцах беспозвоночных. В условиях, когда АТФ быстро используется в качестве источника энергии для сокращения мышц, фосфагены позволяют поддерживать его концентрацию, при высоком соотношении АТФ / АДФ концентрация фосфагенов может увеличиваться, действуя как накопитель энергии.