Лиганд (биохимия)

В биохимии и фармакологии лиганд — это химическое соединение (часто, но не всегда, малая молекула), которое образует комплекс с той или иной биомолекулой (чаще всего белком, например клеточным рецептором, но иногда, например, с ДНК) и производит, вследствие такого связывания, те или иные биохимические, физиологические или фармакологические эффекты. В случае связывания лиганда с белком лиганд обычно является малой сигнальной молекулой, связывающейся со специфическим участком связывания на белке-мишени (например, на рецепторе). В случае связывания лиганда с ДНК лиганд обычно также является малой молекулой или ионом,[1] или белком[2] который связывается с двойной спиралью ДНК.
Связывание лиганда с рецептором обычно происходит при помощи сил межмолекулярного взаимодействия, таких, как ионные связи, водородные связи, Силы Ван-дер-Ваальса (Вандерваа́льсовы си́лы) — силы межмолекулярного (и межатомного) взаимодействия с энергией 10—20 кДж/моль. Этим термином первоначально обозначались все такие силы, в современной науке он обычно применяется к силам, возникающим при поляризации молекул и образовании диполей. Открыты Й. Д. Ван дер Ваальсом в 1869 году.
Вандерваальсовы силы межатомного взаимодействия инертных газов обуславливают возможность существования агрегатных состояний инертных газов (газ, жидкость и твёрдые тела).
К вандерваальсовым силам относятся взаимодействия между диполями (постоянными и наведёнными). Название связано с тем фактом, что эти силы являются причиной поправки на внутреннее давление в уравнении состояния реального газа Ван-дер-Ваальса. Эти взаимодействия, а также водородные связи, определяют формирование пространственной структуры биологических макромолекул.
Вандерваальсовы силы также возникают между частицей (макроскопической частицей или наночастицей) и молекулой и между двумя частицами . Связывание или ассоциация лиганда с рецептором (так называемый «докинг» лиганда в специфическую «нишу» в рецепторе) обычно обратима и кратковременна. Обратный процесс называется диссоциацией лиганда из связи с рецептором. Необратимое ковалентное связывание лиганда с рецептором или другой молекулярной мишенью для данного лиганда является редкостью в биологических системах, по крайней мере в физиологических условиях. Однако искусственные, экзогенные лиганды, необратимо ковалентно связывающиеся с молекулами-мишенями, конечно, существуют, и даже имеют важное значение в медицине, как, например, необратимо алкилирующие ДНК противоопухолевые препараты алкилирующего типа или необратимо инактивирующие МАО антидепрессанты группы ИМАО, или необратимо инактивирующий α-адренорецепторы феноксибензамин. В отличие от принятого определения лиганда в металлоорганической и неорганической химии, для процесса взаимодействия лиганда с биомолекулами-мишенями совершенно неважно (и не требуется), чтобы лиганд взаимодействовал именно с металлом-кофактором в составе биологической молекулы (тем более что не все биологические молекулы содержат металлы в качестве кофакторов). Связывание лиганда именно с металлосодержащим сайтом биологической молекулы, тем не менее, в биологических системах часто встречается и имеет важное биологическое значение и для транспортных белков, таких, как гемоглобин (транспортирующий кислород, углекислый газ и способный транспортировать также другие эндогенные газы, в частности эндогенный угарный газ, эндогенный сероводород и эндогенный оксид серы (IV)), и для каталитических ферментов, многие из которых являются металлоферментами (содержат в составе активного каталитического центра ион того или иного металла в координационном комплексе с белком).
Связывание лиганда с рецептором (рецепторным белком) изменяет его конформационное состояние (трёхмерную пространственную конфигурацию). А это, в свою очередь, может приводить к изменению функционального состояния белка (например, к активации или инактивации рецептора или фермента, к диссоциации одной из субъединиц составного белка или, наоборот, к обретению белком в результате связывания с лигандом способности присоединять другой специфический лиганд или другой белок, или к открытию сопряжённого с белком ионного канала, или к само-фосфорилированию или иной самомодификации белка, или появлению возможностей для его фосфорилирования или иной модификации другим белком, и т. д.). В понятие «лиганда» включаются и субстраты ферментов, и распознаваемые антителами антигены, и разнообразные агонисты, антагонисты и обратные агонисты, в том числе эндогенные, такие, как нейромедиаторы, гормоны, цитокины и хемокины, и ингибиторы и активаторы тех или иных ферментов или регуляторных белков, и факторы транскрипции, и экзогенные, такие, как лекарства и т. д. Сила связывания лиганда с белком-мишенью (например, рецептором) называется «сродством», или аффинностью, лиганда к белку-мишени (например, рецептору). Сила связывания лиганда с белком-мишенью определяется не только силой прямых взаимодействий лиганда с данным белком (например, рецептором), но и микроокружением белковой молекулы, в частности, присутствующими вокруг молекулами растворителя, которые могут играть доминантную роль в обеспечении адекватных межмолекулярных взаимодействий нековалентного характера между лигандом и белком-мишенью (вода[3], липиды клеточной мембраны) и белков-партнёров (в случае, например, олигомерных рецепторов или G-белок-связанных рецепторов). В частности, повышение сродства трансмембранных рецепторов к эндогенным агонистам в присутствии холестерина и сфинголипидов является причиной того, что эти рецепторы, как правило, размещаются в определённых местах клеточной мембраны, называемых липидными рафтами и обогащённых холестерином и сфинголипидами.
Радиолигандами называют меченые радиоактивной меткой (тем или иным радиоактивным изотопом) достаточно высокоаффинные и селективные по отношению к некоторому желаемому подтипу рецепторов соединения, которые используются как in vivo для позитронно-эмиссионной томографии (ПЭТ) с целью изучения распределения этих рецепторов в живом организме и степени связывания с этими рецепторами тех или иных лекарств в клинически применяемых дозах, так и in vitro в качестве «горячих лигандов» для определения аффинности (степени сродства к рецептору) «холодного лиганда».
Степень сродства лиганда к рецептору (аффинность лиганда к рецептору)
Взаимодействие большинства лигандов с их сайтами связывания может быть охарактеризовано в терминах степени сродства лиганда к рецептору (аффинности лиганда к рецептору). В целом, высокая степень сродства того или иного лиганда к данному конкретному подтипу рецепторов (высокая аффинность лиганда к этому подтипу рецепторов) является результатом более сильного межмолекулярного взаимодействия между рецептором и его лигандом, и наоборот — меньшая степень сродства лиганда к данному рецептору (меньшая аффинность к этому рецептору) является, как правило, следствием меньшей силы межмолекулярного взаимодействия между ними. Это также означает, что, в целом, высокоаффинное (то есть с высоким сродством, иначе говоря, сильное) связывание лиганда с рецептором предполагает более продолжительное по времени пребывание лиганда на рецепторе (а значит, и больший процент занятости рецепторов при сравнительно низких дозах или концентрациях лиганда). Кроме того, высокая аффинность связывания лиганда с рецептором (высокое сродство лиганда к нему) часто имеет важные физиологические последствия, поскольку некоторая часть энергии связывания лиганда с рецептором (которая, естественно, выше при «высокоаффинном», с высоким сродством, связывании, как предполагающем большую силу межмолекулярного взаимодействия) может быть использована для изменения пространственной конфигурации рецептора, которая, в свою очередь, может привести к активации или, наоборот, деактивации рецептора и к открытию связанного с рецептором ионного канала или к изменению поведения (повышению или снижению активности) связанного с рецептором фермента или регуляторного белка. Таким образом, более аффинный (имеющий более высокое сродство к рецептору) лиганд с большей вероятностью окажется физиологически и фармакологически активным (то есть проявляющим ту или иную степень внутренней агонистической активности, с каким бы знаком она ни была — агонистом или же обратным агонистом). Однако это не гарантировано — высокоаффинные «нейтральные антагонисты», а вернее, агенты, близкие к нейтральным антагонистам, то есть имеющие очень малую по модулю внутреннюю агонистическую активность, близкую к нулю, но тем не менее проявляющие высокую или очень высокую степень сродства к рецептору, аффинности к нему — тоже существуют.
Рецепторный лиганд, который может связываться с рецептором, изменять пространственную конфигурацию этого рецептора таким образом, что это приводит к его активации, и быть, как следствие этого, способным вызывать тот или иной физиологический или биохимический ответ клетки (быть триггером такого ответа) — называется агонистом по отношению к этому рецептору. Связывание агониста с рецептором может быть охарактеризовано как с точки зрения того, насколько велик максимальный физиологический ответ, который может быть получен при стимуляции максимально доступного количества рецепторов данным конкретным агонистом («внутренняя агонистическая активность»), так и с точки зрения того, какая молярная концентрация данного агониста требуется для вызывания физиологического ответа той или иной силы («кривая зависимости доза-эффект»), и с точки зрения того, какая молярная концентрация данного агониста требуется для того, чтобы вызвать физиологический ответ в 50 % от максимально достижимого для данного агониста («половинная максимальная эффективная концентрация», или EC50, ЭК50). Таким образом определённая и измеренная величина EC50 как раз и является количественной характеристикой меры аффинности агониста к рецептору (меры его сродства к нему). Если же измерять концентрацию, которая требуется для получения 50 % от «максимально достижимого физиологического ответа вообще», а не 50 % от максимально достижимого для данного конкретного агониста (принимая за максимально достижимый, то есть за 100 % — максимальный эффект от эндогенного агониста), то мы получим значение EC50, которое зависит как от значения аффинности агониста (степени его сродства к рецептору), так и от соотношения его внутренней агонистической активности к внутренней агонистической активности эндогенного агониста, принятой за 100 %. Таким образом определённая EC50 будет количественной мерой не одной только лишь аффинности, а молярной активности вещества (его «потентности»), которая есть функция и от аффинности (сродства к рецептору), и от внутренней агонистической активности («рецепторной эффективности») данного лиганда.
Таким образом, высокоаффинное (с высоким сродством) связывание лиганда с рецептором означает, что относительно низкая концентрация лиганда требуется для обеспечения полной (максимально возможной для данной рецепторной системы) занятости участков связывания данного лиганда на рецепторах и вызывания максимально возможного для данного лиганда физиологического ответа (величина которого зависит от «внутренней агонистической активности» лиганда). То есть, чем ниже значение Ki, характеризующее аффинность связывания лиганда с рецептором, тем более вероятным является образование химической связи между молекулами лиганда и молекулами рецептора в результате случайного столкновения молекул при броуновском движении (так как между ними больше сила межмолекулярного взаимодействия). А большая сила межмолекулярного взаимодействия означает и большее среднее время удержания лиганда на рецепторе (большую продолжительность существования нековалентной химической связи). И наоборот, низкоаффинное связывание (с низким сродством к рецептору), то есть высокое значение Ki, означает, что для достижения максимальной занятости всех доступных участков связывания и вызывания максимального физиологического ответа, возможного для данного конкретного агониста, требуются относительно высокие концентрации данного лиганда. Это также значит, что образование химической связи между данным лигандом и рецептором в результате случайного столкновения молекул при броуновском движении для менее аффинного агониста (имеющего меньшее сродство к рецептору) менее вероятно, поскольку между ними меньше сила межмолекулярного взаимодействия и оно менее специфично. А среднее время удержания лиганда на рецепторе у низкоаффинного (имеющего малое сродство к рецептору) меньше, он быстрее освобождает рецептор и быстрее диссоциирует из связи с ним. Более высокая концентрация для низкоаффинного лиганда необходима как раз потому, что она повышает вероятность «случайного столкновения» молекул низкоаффинного лиганда с рецептором и вероятность образования химической связи между ними.
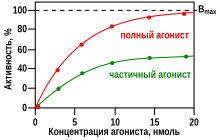
На картинке, показанной справа, два разных лиганда-агониста связываются с одним и тем же участком связывания рецептора. Только один из них способен максимально (то есть наиболее эффективно, с наибольшей вероятностью) стимулировать рецептор, и поэтому может определяться как «полный агонист» для данного подтипа рецепторов. Агонист, который в состоянии активировать рецепторы лишь частично (то есть делает это менее эффективно, чем полный агонист, с меньшей вероятностью приводя к «нужному» изменению конфигурации рецептора и к его активации после связывания, по сравнению с полным агонистом) и вследствие этого способен вызывать меньший по величине физиологический ответ, чем полный агонист, называется частичным агонистом, или парциальным агонистом. В этом примере, концентрация, при которой полный агонист (красная кривая) в состоянии вызвать 50 % от максимального физиологического ответа (то есть EC50), равна приблизительно 5 x 10−9 нано-моль (нМ).
Лиганды, которые связываются с рецепторами, однако не могут или почти не могут активировать рецептор (вернее делают это с пренебрежимо малой вероятностью) и соответственно сами по себе не могут вызывать и не вызывают физиологического ответа рецепторной системы, а лишь предотвращают связывание как агонистов, так и обратных агонистов, и физиологический ответ на них, называются антагонистами.

В примере, показанном слева, кривые зависимости «доза-эффект» показаны для двух лигандов с разной степенью сродства к рецептору (разной аффинностью к нему). Связывание лиганда с рецептором часто характеризуют в терминах того, какая концентрация лиганда требуется для того, чтобы занять 50 % от всех доступных участков связывания рецепторов — так называемая IC50. Величина IC50 связана с константой диссоциации Ki, но отличается от неё. Она отличается также и от величины EC50, поскольку занятие 50 % доступных рецепторов вовсе не обязательно приводит к продуцированию 50 % от максимального физиологического ответа для данного агониста, или 50 % от максимального физиологического ответа «вообще» (IC50 может быть как больше, так и меньше EC50, в зависимости от особенностей регуляции конкретной физиологической рецепторной системы — существуют как рецепторные системы, в которых занятие относительно малого количества рецепторов производит большой физиологический эффект, так и, наоборот, системы, в которых для создания значительного физиологического эффекта нужно занять большой процент доступных рецепторов, причём зависимость величины физиологического эффекта от процента занятости рецепторов, так же как и от дозы агониста, вовсе не обязана быть линейной). Лиганд, кривая зависимости «доза-эффект» для которого изображена красной линией, имеет более высокую степень сродства к рецептору (большую аффинность связывания), чем лиганд, кривая для которого изображена зелёной линией. Если оба лиганда присутствуют одновременно, то больший процент высокоаффинного (имеющего более высокое сродство к рецептору) лиганда будет связано с доступными сайтами связывания рецептора, по сравнению с менее аффинным лигандом. Этот механизм объясняет, в частности, то, почему оксид углерода (II) даже в низких концентрациях может конкурировать с кислородом за связывание с гемоглобином, являясь более высокоаффинным (имеющим большее сродство к гемоглобину) «агонистом» этого транспортного белка, и почему это часто приводит к отравлению угарным газом.
Аффинность связывания лиганда с рецептором (степень сродства лиганда к рецептору) чаще всего определяют с использованием метода вытеснения меченого радиоактивного лиганда (называемого «горячим лигандом») исследуемым лигандом (называемым «холодным», или «тестовым» лигандом). Эксперименты по гомологичному конкурентному связыванию лиганда с рецептором представляют собой эксперименты, в которых «горячий» (меченый радиоактивной меткой) и «холодный» (не помеченный) лиганд — это одно и то же химическое вещество, и они конкурируют между собой за доступные участки связывания с рецептором.[4] Существуют также методы без использования радиоактивной метки, такие, как поверхностный плазмонный резонанс, двойная поляризационная интерферометрия. Эти методы позволяют определить не только аффинность (степень сродства) агониста к рецептору, но и кинетику его ассоциации и диссоциации из связи с рецептором, а в случае двойной поляризационной интерферометрии — ещё и конфигурационные изменения рецептора, вызванные связыванием с ним агониста. В последнее время был разработан также метод микротермофореза.[5] Этот метод позволяет определять аффинность связывания, не накладывая никаких ограничений на молекулярную массу лиганда.[6]
Для анализа полученных данных о кинетике связывания лиганда с рецептором и об его аффинности используются методы статистической механики, в частности вычисление т. н. «конфигурационного интеграла».[7].
Сродство к рецепторам (аффинность) и молярная активность («потентность») лиганда
Степень сродства лиганда к рецепторам, или так называемая «аффинность» лиганда к рецепторам само по себе ещё не определяет молярную активность (общую «потентность») того или иного лиганда. Молярная активность (потентность) вещества является результатом сложного взаимодействия между его степенью сродства к рецепторам и его внутренней агонистической активностью (иначе говоря, его рецепторной эффективностью). Внутренняя агонистическая активность (рецепторная эффективность) — это количественная характеристика способности данного лиганда вызывать тот или иной биологический ответ после связывания с рецептором, и мера величины вызываемого им биологического ответа, в процентах от максимально возможного биологического ответа, за который принимается максимальная стимуляция эндогенным агонистом (100 %). В зависимости от природы, характера, знака и величины по модулю вызываемого лигандом биологического ответа, он классифицируется либо как агонист или даже суперагонист, либо как частичный агонист, либо как нейтральный антагонист, либо как обратный агонист.[8]
Селективные и неселективные лиганды
Селективные лиганды имеют тенденцию в клинически/физиологически релевантных (как правило, наномолярных) концентрациях клинически/физиологически значимо связываться только с достаточно ограниченным набором подтипов рецепторов (не обязательно все эти подтипы будут рецепторами к одному и тому же эндогенному лиганду). В то же время неселективные лиганды имеют тенденцию в релевантных концентрациях значимо связываться с достаточно широким набором подтипов рецепторов (часто — к разным эндогенным лигандам) и, тем самым, производить более широкий спектр клинических, биохимических и физиологических эффектов, как желательных, так и, нередко, нежелательных побочных эффектов.
Селективность лиганда является понятием достаточно условным и относительным, поскольку существует очень мало истинно селективных лигандов, которые связываются только с одним подтипом рецепторов во всём диапазоне «разумных», клинически достижимых у человека концентраций, и ещё меньше лигандов, способных сохранять 100 % селективность в тех концентрациях, которые можно создать в экспериментах на животных и тем более «в пробирке» (in vitro). Часто кажущаяся относительная селективность того или иного лиганда теряется при повышении дозы или концентрации (то есть в более высоких концентрациях или дозах он начинает взаимодействовать и с другими подтипами рецепторов), и это имеет важное клиническое значение (так, высокие дозы селективного агониста опиоидных рецепторов бупренорфина способны значимо угнетать дыхание и вызывать эйфорию, так как селективность по сравнению с морфином утрачивается; аналогичным образом высокие дозы селективных β-адреноблокаторов способны вызывать бронхоспазм, так как утрачивается селективность к подтипу β1, а высокие дозы β2-адреностимуляторов помимо устранения бронхоспазма способны также вызывать тахикардию; высокие дозы атипичных антипсихотиков наподобие рисперидона и оланзапина способны вызывать экстрапирамидные побочные явления, подобно типичным антипсихотикам).
Разработка новых, более селективных, лигандов является важной задачей современной экспериментальной и клинической фармакологии, поскольку селективные лиганды, избирательно активируя или блокируя только один «нужный» подтип рецепторов или несколько их подтипов, имеют тенденцию проявлять меньше побочных эффектов, в то время как неселективные лиганды, связываясь с широким кругом рецепторов, производят как желательные, так и нежелательные побочные эффекты. Хорошим примером является сравнение относительно неселективного хлорпромазина с более селективным галоперидолом: хлорпромазин, за счёт своей низкой селективности, производит множество побочных эффектов в дополнение к полезному антипсихотическому эффекту (так, α1-адреноблокада приводит к гипотензии и тахикардии, H1-гистаминовая блокада к сонливости, седации, повышению аппетита и прибавке массы тела, М-холиноблокада — к сухости рта и запорам и т. п., в то время как галоперидол эти явления вызывает в значительно меньшей мере и в клинически применяемых дозах вызывает в основном экстрапирамидные побочные явления, непосредственно связанные с его основным D2-блокирующим действием).
Мерой относительной селективности того или иного лиганда является величина соотношения его сродства (аффинности) к «желаемому», «основному» подтипу рецепторов (например, к D2, в случае антипсихотиков), и к ближайшему следующему по порядку величины показателя сродства (аффинности) подтипу рецепторов — то есть значение соотношения Ki(1) / Ki(2). Более высокоаффинные к «желаемому» типу рецепторов, более высокоактивные («более высокопотентные») соединения часто, хотя и не всегда, являются также и более селективными, по крайней мере в малых концентрациях (применение которых, опять-таки, становится возможным именно благодаря более высокой аффинности соединения по отношению к рецептору и большей активности соединения). Таким образом, важной задачей экспериментальной и клинической фармакологии является разработка новых, более высокоаффинных (обладающих более высоким сродством к рецептору) и более активных («более высокопотентных») по отношению к тем или иным типам рецепторов, соединений.
Бивалентные лиганды
Бивалентные лиганды состоят из двух соединённых молекул, каждая из которых является лигандом для определённого подтипа рецепторов (одного и того же или разных), причём в силу особенностей пространственного строения обе части молекулы способны одновременно связываться с двумя частями «составного» гомо- или гетеродимерного рецепторного комплекса. Бивалентные лиганды используются в научных исследованиях с целью обнаружения и исследования рецепторных гомо- и гетеродимерных комплексов и изучения их свойств. Бивалентные лиганды обычно являются крупными молекулами и имеют тенденцию не обладать нужными для лекарств свойствами, такими, как удобная фармакокинетика (приемлемая биодоступность, удобство клинического применения, приемлемый период полувыведения и т. д.), низкая аллергенность и приемлемая токсичность и уровень побочных эффектов, что делает их, как правило, непригодными или малопригодными для использования в клинической практике, за пределами исследовательских лабораторий.[9][10]
Привилегированная структура
Привилегированная структура[11] — это структурная часть молекулы, радикал или химический элемент, который или которая статистически часто повторяется среди уже известных лекарств данного фармакологического класса, среди уже известных лигандов данного типа или подтипа рецепторов или известных ингибиторов данного фермента, или среди некоего другого выделенного по неким общим признакам специфического подмножества уже известных биологически активных соединений. Эти статистически выделенные привилегированные элементы химической структуры[12] могут в дальнейшем быть использованы в качестве основы для разработки новых биологически активных соединений или новых лекарств со сходными или, возможно, даже улучшенными по сравнению с исходными соединениями свойствами, и даже для разработки целых библиотек таких соединений.
Характерными примерами являются, например, трициклические структуры разного химического строения в составе молекул трициклических антидепрессантов, или существование химически сходных целых подклассов антипсихотиков, таких, как производные бутирофенона (галоперидол, спиперон, дроперидол и др.), производные индола (резерпин, карбидин и др.), производные фенотиазина (хлорпромазин, перфеназин и др.).
См. также
Примечания
- ↑ Teif V.B. Ligand-induced DNA condensation: choosing the model (англ.) // Biophysical Journal[англ.] : journal. — 2005. — Vol. 89, no. 4. — P. 2574—2587. — doi:10.1529/biophysj.105.063909. — PMID 16085765. — PMC 1366757.
- ↑ Teif V. B., Rippe K. Statistical-mechanical lattice models for protein-DNA binding in chromatin (англ.) // Journal of Physics: Condensed Matter[англ.] : journal. — 2010. — Vol. 22, no. 41. — P. 414105. — doi:10.1088/0953-8984/22/41/414105. — PMID 21386588.
- ↑ Baron, Riccardo; Setny, Piotr; Andrew Mccammon, J. Water in Cavity-Ligand Recognition (англ.) // Journal of the American Chemical Society[англ.] : journal. — 2010. — Vol. 132, no. 34. — P. 12091—12097. — doi:10.1021/ja1050082. — PMID 20695475. — PMC 2933114.
- ↑ See Homologous competitive binding curves Архивировано 19 декабря 2007 года., A complete guide to nonlinear regression, curvefit.com.
- ↑ Baaske P., Wienken C. J., Reineck P., Duhr S., Braun D. Optical Thermophoresis quantifies Buffer dependence of Aptamer Binding (англ.) // Angew. Chem. Int. Ed. : journal. — 2010. — February (vol. 49, no. 12). — P. 1—5. — doi:10.1002/anie.200903998. — PMID 20186894.
- ↑ Wienken CJ et al. Protein-binding assays in biological liquids using microscale thermophoresis (англ.) // Nature Communications : journal. — Nature Publishing Group, 2010. — Vol. 1, no. 7. — P. 100. — doi:10.1038/ncomms1093. — . — PMID 20981028. Архивировано 23 января 2011 года.
- ↑ Vu-Quoc, L.[1], 2011.
- ↑ Kenakin, Terrance P. A pharmacology primer: theory, applications, and methods (англ.). — Academic Press, 2006. — P. 79. — ISBN 978-0-12-370599-0.
- ↑ Shonberg, Jeremy; Scammells, Peter J.; Capuano, Ben. Design strategies for bivalent ligands targeting GPCRs (датск.) // ChemMedChem[англ.]. — 2011. — Juni (bd. 6, nr. 6). — S. 963—974. — doi:10.1002/cmdc.201100101. — PMID 21520422.
- ↑ Berque-Bestel, I; Lezoualc'h, F; Jockers, R. Bivalent ligands as specific pharmacological tools for G protein-coupled receptor dimers (англ.) // Curr Drug Discov Technol : journal. — 2008. — December (vol. 5, no. 4). — P. 312—318. — doi:10.2174/157016308786733591. — PMID 19075611.
- ↑ Privileged Scaffolds for Library Design and Drug Discovery. Дата обращения: 2 октября 2017. Архивировано 8 февраля 2020 года.
- ↑ Kombarov R., Altieri A., Genis D., Kirpichenok M., Kochubey V., Rakitina N., Titarenko Z. BioCores: identification of a drug/natural product-based privileged structural motif for small-molecule lead discovery. (англ.) // Molecular diversity. — 2010. — Vol. 14, no. 1. — P. 193—200. — doi:10.1007/s11030-009-9157-5. — PMID 19468851.












