Молекулярная геометрия
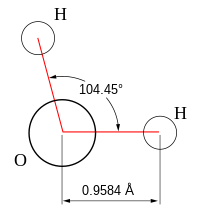
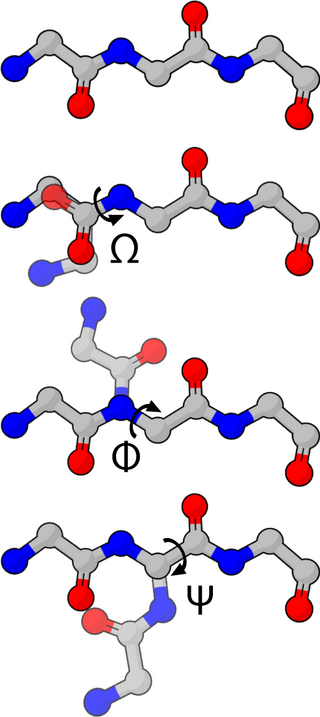
Молекулярная геометрия — это трехмерное расположение атомов, составляющих молекулу. Она включает в себя общую форму молекулы, а также длины связей, валентные углы, торсионные углы и любые другие геометрические параметры, которые определяют положение каждого атома.
Геометрия молекулы влияет на ряд свойств вещества, включая его реакционную способность, полярность, фазу вещества, цвет, магнетизм и биологическую активность[1][2][3]. Углы между связями, которые образует атом, слабо зависят от остальной части молекулы, то есть их можно рассматривать как приблизительно локальные и, следовательно, переносимые[англ.] свойства.
Определение
Геометрия молекулы может быть определена различными спектроскопическими и дифракционными методами. ИК, микроволновая и рамановская спектроскопия могут дать информацию о геометрии молекулы на основе деталей колебательного и вращательного поглощения, обнаруживаемых этими методами. Рентгеновская кристаллография, дифракция нейтронов и дифракция электронов могут дать молекулярную структуру кристаллических твердых тел на основе расстояния между ядрами и концентрации электронной плотности. Газовая дифракция электронов может использоваться для небольших молекул в газовой фазе. Методы ЯМР и FRET могут использоваться для определения дополнительной информации, включая относительные расстояния[4][5][6], двугранные углы[7][8], углы и связность. Молекулярную геометрию лучше всего определять при низкой температуре, потому что при более высоких температурах молекулярная структура усредняется по более доступным геометриям (см. следующий раздел). Более крупные молекулы часто существуют в нескольких стабильных геометриях (конформационная изомерия), близких по энергии на поверхности потенциальной энергии. Геометрии также могут быть вычислены с помощью ab initio методов квантовой химии с высокой точностью. Геометрия молекулы может быть разной для твердого тела, в растворе и в газе.
Положение каждого атома определяется природой химических связей, которыми он связан со своими соседними атомами. Геометрия молекулы может быть описана положением этих атомов в пространстве, откуда выводятся длины связи двух связанных атомов, валентные углы в тройках связанных атомов и торсионные углы (двугранные углы) трех последовательных связей.
Влияние теплового возбуждения
«Движение» атомов в молекуле определяется квантовой механикой. Общие (внешние) квантово-механические движения, трансляция и вращение практически не меняют геометрию молекулы. В некоторой степени вращение влияет на геометрию через силы Кориолиса и центробежное искажение, но для настоящего обсуждения это несущественно. В дополнение к поступательному движению и вращению, третьим типом движения является молекулярная вибрация, которая соответствует внутренним движениям атомов, таким как растяжение связи и изменение угла связи. Колебания молекул являются гармоническими (по крайней мере, в хорошем приближении), и атомы колеблются около своего положения равновесия даже при температуре абсолютного нуля. При абсолютном нуле все атомы находятся в своем основном колебательном состоянии и демонстрируют квантово-механические нулевые колебания, так что волновая функция одной колебательной моды представляет собой не острый пик, а экспоненту конечной ширины. При более высоких температурах колебательные моды могут быть термически возбуждены (в классической интерпретации это выражается утверждением, что «молекулы будут колебаться быстрее»), но они по-прежнему колеблются вокруг узнаваемой геометрии молекулы.
Примечания
- ↑ John McMurry. Organic chemistry. — 3rd ed. — Pacific Grove, Calif.: Brooks/Cole Pub, 1992. — 1 volume (various pagings) с. — ISBN 0-534-16218-5, 978-0-534-16218-4, 0-534-97956-4, 978-0-534-97956-0. Архивировано 8 мая 2022 года.
- ↑ Advanced inorganic chemistry.. — 6th edition. — New York, 1999. — xv, 1355 pages с. — ISBN 0-471-19957-5, 978-0-471-19957-1, 981-253-044-4, 978-981-253-044-8.
- ↑ Alexandros Chremos, Jack F. Douglas. Communication: When does a branched polymer become a particle? (англ.) // The Journal of Chemical Physics. — 2015-09-21. — Vol. 143, iss. 11. — P. 111104. — ISSN 1089-7690 0021-9606, 1089-7690. — doi:10.1063/1.4931483. Архивировано 29 января 2021 года.
- ↑ Fluorescent Resonance Energy Transfer as a Probe of Proximity in Proteins. web.archive.org (18 сентября 2008). Дата обращения: 22 июля 2021. Архивировано из оригинала 18 сентября 2008 года.
- ↑ Alexander Hillisch, Mike Lorenz, Stephan Diekmann. Recent advances in FRET: distance determination in protein–DNA complexes (англ.) // Current Opinion in Structural Biology. — 2001-04. — Vol. 11, iss. 2. — P. 201–207. — doi:10.1016/S0959-440X(00)00190-1. Архивировано 1 февраля 2022 года.
- ↑ FRETImaging.org - Introduction to FRET. web.archive.org (14 октября 2008). Дата обращения: 22 июля 2021. Архивировано из оригинала 14 октября 2008 года.
- ↑ (H-J-J-H) Coupling Constant to Dihedral Angle Converter. web.archive.org (7 декабря 2008). Дата обращения: 22 июля 2021. Архивировано 7 декабря 2008 года.
- ↑ General Karplus Calculator. web.archive.org (28 декабря 2005). Дата обращения: 22 июля 2021. Архивировано 28 декабря 2005 года.