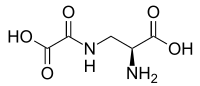
Алани́н — алифатическая аминокислота. α-Аланин входит в состав многих белков, β-аланин — в состав ряда биологически активных соединений.

Аминокисло́ты, также аминокарбо́новые кисло́ты, АМК — органические соединения, в молекуле которых одновременно содержатся карбоксильные и аминные группы. Основные химические элементы аминокислот — это углерод (C), водород (H), кислород (O) и азот (N), хотя другие элементы также встречаются в радикале определенных аминокислот. Известны около 500 встречающихся в природе аминокислот . Аминокислоты могут рассматриваться как производные карбоновых кислот, в которых один или несколько атомов водорода заменены на аминогруппы.

Ци́кл трикарбо́новых кисло́т (сокр. ЦТК, цикл Кре́бса, цитра́тный цикл, цикл лимо́нной кислоты́) — центральная часть общего пути катаболизма, циклический биохимический процесс, в ходе которого ацетильные остатки (СН3СО-) окисляются до диоксида углерода (CO2). При этом за один цикл образуется 2 молекулы CO2, 3 НАДН, 1 ФАДH2 и 1 ГТФ (или АТФ). Электроны, находящиеся на НАДН и ФАДH2, в дальнейшем переносятся на дыхательную цепь, где в ходе реакций окислительного фосфорилирования образуется АТФ.
Трансфера́зы (КФ2) — отдельный класс ферментов, катализирующих перенос функциональных групп и молекулярных остатков от одной молекулы к другой. Широко распространены в растительных и животных организмах, участвуют в превращениях углеводов, липидов, нуклеиновых и аминокислот.

Сери́н — гидроксиаминокислота, существует в виде двух оптических изомеров — L и D.

Кофермент A — кофермент ацетилирования; один из важнейших коферментов, принимающий участие в реакциях переноса ацильных групп при синтезе и окислении жирных кислот и окислении пирувата в цикле лимонной кислоты.

Гиппу́ровая кислота́ — N-бензоилглицин, бесцветные кристаллы, слаборастворимые в холодной воде и хорошо растворимые в горячей воде и этаноле. Гиппуровая кислота содержится в моче травоядных и человека, впервые обнаружена в моче лошади, благодаря чему и получила своё название.
Жёлчные пигме́нты, также билины — биологические пигменты, линейные тетрапирролы, формально являющиеся производными билана (билиногена) с окисленными терминальными пиррольными ядрами, образующиеся при катаболизме гема. Впервые выделены из жёлчи, которой придают характерную окраску, откуда и получили своё название; цвет различных жёлчных пигментов — от жёлто-оранжевого до сине-зелёного. Образуются во многих организмах как продукт метаболизма некоторых порфиринов. Билин был назван как желчный пигмент млекопитающих, но его также можно обнаружить в низших позвоночных, беспозвоночных, а также в красных водорослях, зелёных растениях и цианобактериях. Цвет билинов может варьировать от красного, оранжевого, жёлтого и коричневого до голубого и зелёного.
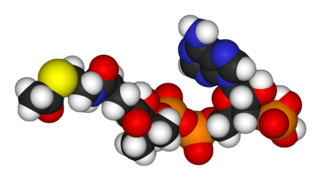
Ацетилкофермент А, ацетил-коэнзим А, сокращённо ацетил-КоА — важное для обмена веществ соединение, используемое во многих биохимических реакциях. Его главная функция — доставлять атомы углерода с ацетил-группой в цикл трикарбоновых кислот, чтобы те были окислены с выделением энергии. По своей химической структуре ацетил-КоА — тиоэфир между коферментом А (тиолом) и уксусной кислотой. Ацетил-КоА образуется во время второго шага кислородного клеточного дыхания, декарбоксилирования пирувата, который происходит в матриксе митохондрии. Ацетил-КоА затем поступает в цикл трикарбоновых кислот.
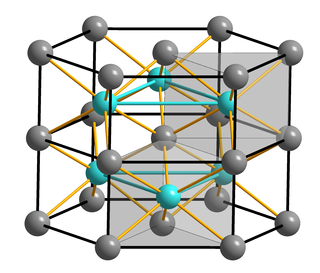
Сульфи́д ко́бальта(II) — бинарное неорганическое соединение, соль металла кобальта и сероводородной кислоты с химической формулой CoS, серые кристаллы, нерастворимые в воде.

Сирогем — гемоподобная простетическая группа нитрит- и сульфитредуктаз, катализирующих шестиэлектронное восстановление серы сульфита или азота нитрита до сульфида и аммиака.
Общий путь катаболизма — совокупность биохимических процессов, которая включает в себя:
- окисление пирувата до ацетил-КоА;
- окисление ацетил-КоА в цикле трикарбоновых кислот;

Лотавстралин — органическое соединение, глюкозид циангидрина метилэтилкетона, цианогенный гликозид, содержащийся в некоторых бобовых растениях, растениях родов родиола и маниок, а также ряде других растений.

Прунази́н — гликозид циангидрина бензальдегида (манделонитрила), цианогенный гликозид, содержащийся в растениях рода Prunus (Слива) — миндале, вишнях, абрикосе и др.

Аллантоиновая кислота — 2,2-диуреидоуксусная кислота, бесцветные кристаллы, растворимые в воде.
Оксигеназы — ферменты, катализирующие реакции присоединения одного (монооксигеназы) либо двух (диоксигеназы) атомов кислорода к молекуле субстрата, источником кислорода в этом случае является молекулярный кислород; являются подклассом класса оксидоредуктаз.
Бе́та-окисле́ние (β-окисление), также цикл Кноопа — Линена, — метаболический процесс деградации жирных кислот. Своё название процесс получил по 2-му углеродному атому (С-3 или β-положение) от карбоксильной группы (-СООН) жирной кислоты, который подвергается окислению и последовательному отделению от молекулы. Продуктами каждого цикла β-окисления являются ФАДH2, НАДH и ацетил-КоА. Реакции β-окисления и последующего окисления ацетил-КоА в цикле Кребса служат одним из основных источников энергии для синтеза АТФ по механизму окислительного фосфорилирования.
Непротеиногенные аминокислоты — аминокислоты, которые не участвуют в биосинтезе белка. Непротеиногенные аминокислоты часто не входят в состав непатогенных и «нормальных» белков человека, не следует их путать с нестандартными аминокислотами, которые образуются непосредственно при синтезе белка или в результате различных ковалентных модификаций молекулярных структур протеиногенных (кодируемых) аминокислот в составе белков, например, гидроксипролина, десмозина или аллизина. Однако они могут входить в состав некоторых небольших молекул или пептидов, синтез которых является нерибосомальным. Химически синтезированные аминокислоты можно назвать неприродными аминокислотами. Многие из них являются токсинами и ингибиторами ферментов разнообразных метаболических реакций. Известно свыше 400 природных аминокислот и, возможно, больше тысячи их комбинаций. Неприродные аминокислоты могут быть синтетически получены из их нативных аналогов с помощью модификаций, таких как алкилирование аминогруппы, замещение боковой цепи, циклизация за счёт удлинения структурных связей и изостерических замен в аминокислотном остове.

Карнитин-О-ацетилтрансфераза, также Карнитин-ацетилтрансфераза, сокр. КАТ (англ. Carnitine O-acetyltransferase, сокр. CRAT) — фермент (КФ 2.3.1.7), из семейства ацилтрансферазы (класс трансферазы), катализирующий перенос ацетильной группы (СH3-CO) от молекулы ацетил-КоА на молекулу субстрата — карнитина и обратно, когда субстратом уже служит кофермент А, по уравнению:
Транслоказы — отдельный класс ферментов, катализирующих перенос ионов или молекул через мембраны или их разделение в мембранах. Этот класс ферментов сформировался из ранее принадлежащих другим классам ферментов.