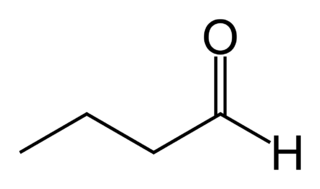
Пропаналь
| Пропаналь | |||
|---|---|---|---|
| |||
| Общие | |||
| Систематическое наименование | пропиональдегид, пропионовый альдегид | ||
| Традиционные названия | пропаналь | ||
| Хим. формула | СН3СН2СHO | ||
| Физические свойства | |||
| Состояние | жидкость | ||
| Молярная масса | 58,1 г/моль | ||
| Плотность | 0,81 г/см³ | ||
| Энергия ионизации | 9,95 эВ[1] | ||
| Термические свойства | |||
| Температура | |||
| • плавления | −81 °C | ||
| • кипения | 48,8 °C | ||
| • вспышки | -30 °C | ||
| • самовоспламенения | 207 °C | ||
| Пределы взрываемости | 2,6-17,0 % | ||
| Давление пара | 31,3 кПа 20°C | ||
| Химические свойства | |||
| Растворимость | |||
| • в воде | 16,7 г/100 мл | ||
| Оптические свойства | |||
| Показатель преломления | 1,3636 | ||
| Структура | |||
| Дипольный момент | 2,52 Д | ||
| Классификация | |||
| Рег. номер CAS | 123-38-6 | ||
| PubChem | 527 | ||
| Рег. номер EINECS | 204-623-0 | ||
| SMILES | |||
| InChI | |||
| RTECS | UE0350000 | ||
| ChEBI | 17153 | ||
| Номер ООН | 1275 | ||
| ChemSpider | 512 | ||
| Безопасность | |||
| NFPA 704 | |||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
Пропаналь (пропионовый альдегид, пропиональдегид) — альдегид пропионовой кислоты. Является изомером ацетона.
Физические свойства
Бесцветная жидкость с характерным запахом. Смешивается со многими органическими растворителями (например, спиртом), с водой образует азеотропную смесь (т. кип. 47,8 °С, 98,1 % пропаналя). Koэффициент распределения октанол/вода как lg Pow: 0,83
Получение
В промышленности в основном получается гидроформилированием этилена, синтез-газом (смесь угарного газа и водорода) в присутствии родия или карбонила кобальта:
- ,
а также окислением бутан-пропановой фракции:
- .
Может быть также получен путём дегидрирования 1-пропанола на серебряном катализаторе при 400 °C:
- .
Лабораторный способ получения основывается на частичном окислении пропанола-1 бихроматом калия в присутствии серной кислоты. При этом к кипящему пропанолу добавляют раствор бихромата калия в разбавленной серной кислоте. Пары проходят через обратный холодильник установленный под углом 45° и охлаждаемый водой с температурой до 60 °С. Таким образом непрореагировавший пропанол-1 возвращается обратно в реакционный сосуд, а пары пропаналя уносятся. К верху обратного холодильника присоединён нисходящий холодильник, охлаждаемый холодной водой, где конденсируется пропаналь. Выход реакции достигает 50 %[2].
Также он может быть получен изомеризацией пропиленоксида над силикагелем при 300 °C[3] и гидрированием акролеина[4]:
- .
Применение
В органическом синтезе
Конденсацией с трет-бутиламином получают CH3CH2CH=N-t-Bu, который является трёхатомным билдинг-блоком. Под действием LDA он депротонируется, образуя CH3CHLiCH=N-t-Bu. Это вещество далее контролируемо взаимодействует с альдегидами.
Безопасность
Оказывает наркотическое и раздражающее действие, поражает дыхательную систему, паренхиматозные органы, гемопоэз[5]. Хорошо всасывается через неповрежденную кожу. Раздражает кожу и при длительном контакте вызывает некроз. При попадании в глаза — сильное раздражение, ожоги роговицы[5]. Для крыс при внутрижелудочном введении ЛД50 — 1410 мг/кг. ПДК р. з. — 5 мг/м3; пары, класс опасности — 3. ОБУВ а. в. — 0,01 мг/м3[6]. ПДК м. р. — 0,015 мг/м3. Пропаналь является одним из метаболитов пропиленгликоля в организме (образуется в очень небольших количествах).
Горюч. Пределы взрываемости паров в воздухе: 2,6—17,0 об.%.
ПДК в воздухе рабочей зоны — 5 мг/м3 (максимально разовая)[7]. А порог восприятия запаха может достигать, например, 240 мг/м3[8]. У части людей порог был значительно выше среднего значения. Поэтому можно ожидать, что использование широко распространённых фильтрующих СИЗОД в сочетании с «заменой фильтров по появлении запаха под маской» (как это почти всегда рекомендуется в РФ поставщиками СИЗОД) приведёт к чрезмерному воздействию токсичных[9] паров пропиональдегида на, по крайней мере, часть работников — из-за запоздалой замены противогазных фильтров. Для защиты от пропаналя следует использовать значительно более эффективные изменение технологии и средства коллективной защиты.
Примечания
- ↑ David R. Lide, Jr. Basic laboratory and industrial chemicals (англ.): A CRC quick reference handbook — CRC Press, 1993. — ISBN 978-0-8493-4498-5
- ↑ Синтезы органических препаратов. Сборник 2. М.: Иностранная Литература, 1949, стр. 424.
- ↑ Hurd C. D., Meinert R. N.: Propionaldehyde. In: Organic Syntheses. v. 12, 1932, p. 65
- ↑ Sabatier P., Senderens J.-B.: «Nouvelles méthodes générales d’hydrogénation» in Ann. phys. chim. (8) 1905, v. 4, p. 398
- ↑ 1 2 Вредные вещества в промышленности, 7-е издание, Ленинград, «Химия» 1976, Т. 1., С. 512
- ↑ ГН 2.1.6.2309-07 Ориентировочные безопасные уровни воздействия (ОБУВ) загрязняющих веществ в атмосферном воздухе населенных мест. Дата обращения: 10 ноября 2020. Архивировано 3 ноября 2020 года.
- ↑ (Роспотребнадзор). № 1819. Пропиональдегид (пропаналь) // ГН 2.2.5.3532-18 «Предельно допустимые концентрации (ПДК) вредных веществ в воздухе рабочей зоны» / утверждены А.Ю. Поповой. — Москва, 2018. — С. 125. — 170 с. — (Санитарные правила). Архивировано 12 июня 2020 года.
- ↑ Pliska V. and G. Janicek. Die Veranderungen der Wahrnehmungsschwellen - Konzentration der Riechstoffe in Einiger Homologischen Serien (нем.) // Heymans Institute of Pharmacology Archives internationales de pharmacodynamie et de therapie. — Gent (Belgium), 1965. — Vol. 156. — S. 211—216. — ISSN 0003-9780.
- ↑ МКХБ Международная организация труда. МКХБ № 0550. Пропионовый альдегид. Пропаналь. www.ilo.org/dyn/icsc/ (2018). Дата обращения: 12 ноября 2019.