Ами́ды — производные кислородсодержащих кислот, в которых гидроксильная группа кислотного остатка заменена аминогруппой. Амиды также можно рассматривать как ацилпроизводные аминов. Соединения с одним, двумя или тремя ацильными заместителями у атома азота называются первичными, вторичными и третичными амидами соответственно. Вторичные амиды также называют имидами.
Ами́ны — органические соединения, являющиеся производными аммиака, в молекуле которого один или несколько атомов водорода замещены на углеводородные радикалы. По числу замещённых атомов водорода различают соответственно первичные (замещён один атом водорода), вторичные (замещены два атома из трёх) и третичные амины (замещены все три атома). Выделяют также четвертичные аммониевые соединения вида R4N+X-.
Гетероциклические соединения (гетероциклы) — органические соединения, содержащие циклы, в состав которых входят атомы как минимум двух различных элементов. Могут рассматриваться как карбоциклические соединения с гетерозаместителями (гетероатомами) в цикле. Наиболее разнообразны и хорошо изучены ароматические азотсодержащие гетероциклические соединения. Предельные случаи гетероциклических соединений — соединения, не содержащие атомов углерода в цикле, например, пентазол.
Алкилирование — введение алкильного заместителя в молекулу органического соединения. Типичными алкилирующими агентами являются алкилгалогениды, алкены, эпоксисоединения, спирты, реже альдегиды, кетоны, эфиры, сульфиды, диазоалканы. Катализаторами алкилирования являются минеральные кислоты, кислоты Льюиса ,а также цеолиты.
Ката́лиз — избирательное ускорение одного из возможных термодинамически разрешённых направлений химической реакции под действием катализатора(ов), который, согласно теории промежуточных соединений, многократно вступает в промежуточное химическое взаимодействие с участниками реакции и восстанавливает свой химический состав после каждого цикла промежуточных химических взаимодействий.

Оксимы (или изонитрозосоединения) — органические соединения, включающие в себя одну или несколько изонитрозогрупп RR1C=N-OH. Обычно рассматриваются как производные альдегидов (R1 = H) — альдоксимы и кетонов — кетоксимы. Для альдоксимов и оксимов несимметричных кетонов характерна цис-транс-изомерия по связи C=N.
Краун-эфиры (краун-соединения) — макрогетероциклические соединения, содержащие в своих циклах более 11 атомов, из которых не менее четырёх — гетероатомы, которые связаны между собой этиленовыми мостиками.
Перегруппировка Бекмана — это химическая реакция превращения оксимов в амиды под действием кислотных дегидратирующих агентов, таких как H2SO4, олеум и др. Открыта в 1886 году немецким химиком Э. О. Бекманом
Перегруппировка Брука — в органической химии реакция, в ходе которой органосилильная группа мигрирует с атома углерода на атом кислорода прилежащей гидроксильной группы. Конечным продуктом является силильный эфир. Данный процесс протекает под действием основания. Реакция названа так по имени канадского химика Адриана Гиббса Брука.
Бензидиновая перегруппировка — превращение 1,2-диарилгидразинов в 4,4'-диаминодиарилы, протекает по [5,5]-сигматропному механизму. Открыта Н. Н. Зининым в 1845 г..
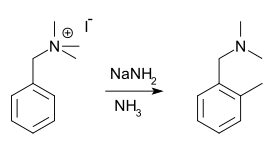
Реакция Соммле — метод синтеза альдегидов взаимодействием соединений, содержащих галогенметильную группу, с гексаметилентетрамином (уротропином) с образованием и последующим гидролизом образующейся четвертичной аммонийной соли, открыта в 1913 г. Марселем Соммле :



Имины — органические соединения общей формулы R1R2C=NR3, где R1, R2 — H, Alk, Ar и R3 — H, Alk, Ar, азотистые аналоги альдегидов (R2 — H, альдимины) и кетонов (R1, R2 — Alk, Ar, кетимины), содержащие фрагмент NR3, соединенный двойной связью с атомом углерода.
Азиды — органические соединения, содержащие азидную группу -N=N+=N−, обычно связанную с атомом углерода, однако к азидам также относят и элементоорганические соединения (например, триалкилсилил- и триалкилстаннилазиды), и азидпроизводные сульфокислот (сульфонилазиды RSO2N3).
Кри́стофер Кельк И́нгольд — английский химик, знаменит за свои фундаментальные работы в области физической органической химии. Его новаторские работы в 1920—1930-х годах, посвящённые изучению механизмов реакций и электронной структуре органических соединений, послужили отправной точкой для введения в органическую химию таких понятий как нуклеофил, электрофил, индуктивный и мезомерный эффекты. Ингольд ввел в химию концепты SN1, SN2, E1, и E2 механизмов, предсказал и открыл механизмы гидролиза сложных эфиров карбоновых кислот. Кроме того, он — один из соавторов правил Кана — Ингольда — Прелога. За свою карьеру Ингольд опубликовал свыше 450 статей и писем в научные журналы. Он по праву считается одним из основоположников физической органической химии.
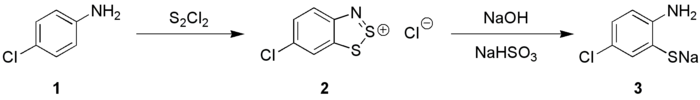
Реакция Херца — метод синтеза 2-аминотиофенолов из ароматических аминов взаимодействием дитиодихлорида с анилинами (1), ведущим к образованию циклических 1,2,3-бензодитиазолиевых солей и последующим расщеплением дитиазолиевого цикла:
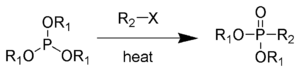
Реакция Арбузова — в классическом варианте — алкилирование триалкилфосфитов алкилгалогенидами с образованием диалкилфосфонатов:
Лигирование по Штаудингеру — модификация реакции Штаудингера, широко применяемая в области химической биологии и биоконъюгации для ковалентного связывания биомолекул с низкомолекулярными метками, а также для мечения клеток в живых организмах. Реакция предложена в 2000 году группой К. Бертоцци. Поскольку участвующие в ней функциональные группы практически не представлены в организмах и не склонны взаимодействовать с природными соединениями, лигирование по Штаудингеру относится к биоортогональным реакциям.
Перегруппировка Небера — перегруппировка O-сульфонатов кетоксимов под действием сильных оснований в азирины и далее в α-аминокетоны.

Перегруппировка Вольфа — реакция в органической химии, в которой α-диазокарбонильное соединение превращается в кетен потерей азота, сопровождающейся 1,2-перегруппировкой. В перегруппировке Вольфа кетен является интермедиатом, который может далее подвергаться нуклеофильной атаке со слабокислыми нуклеофилами, образуя производные карбоновых кислот или продукт [2+2]-циклоприсоединения, содержащий четырёхчленный цикл. Механизм перегруппировки Вольфа был предметом обсуждения с момента его первого использования, но ни один из предложенных механизмов не описывает реакцию полностью. Реакция открыта Людвигом Вольфом в 1902 году. Перегруппировка Вольфа имеет широкое применение в органическом синтезе благодаря доступности α-диазакарбонильных соединений, разнообразию реакций с участием кетенового интермедиата и стереохимическому удержанию мигрирующей группы. Тем не менее, перегруппировка Вольфа имеет ограничения из-за высокой реакционной способности α-диазокарбонильных соединений, которые могут претерпевать различные конкурирующие реакции.