Ретровирусы
| Ретровирусы | |
|---|---|
 | |
| Научная классификация | |
| Международное научное название | |
| Retroviridae | |
| Подсемейства | |
| |
| Группа по Балтимору | |
| VI: оцРНК-ОТ-вирусы | |
Ретрови́русы[2][3] (лат. Retroviridae, от лат. retro — обратный) — семейство РНК-содержащих вирусов, заражающих преимущественно позвоночных. Наиболее известный и активно изучаемый представитель — вирус иммунодефицита человека.
После инфицирования клетки ретровирусом в цитоплазме начинается синтез вирусного ДНК-генома с использованием вирионной РНК в качестве матрицы. Все ретровирусы используют для репликации своего генома механизм обратной транскрипции: вирусный фермент обратная транскриптаза (или ревертаза) синтезирует одну нить ДНК на матрице вирусной РНК, а затем уже на матрице синтезированной нити ДНК достраивает вторую, комплементарную ей нить. Образуется двунитевая молекула ДНК, которая интегрируется в хромосомную ДНК клетки во время клеточного деления, когда нет ядерной оболочки, (исключением является ВИЧ, ДНК которого активно проникает в ядро) и далее служит матрицей для синтеза молекул вирусных РНК. Эти РНК выходят из клеточного ядра и в цитоплазме клетки упаковываются в вирусные капсиды, способные инфицировать новые клетки.
По одной из гипотез, ретровирусы могли произойти от ретротранспозонов — подвижных участков генома эукариот[4].
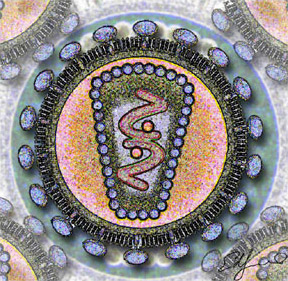
Устройство
Вирионы сферической формы размером 80—100 нм, покрыты внешней липопротеиновой оболочкой, имеющей ворсинки длиной 8—10 нм. Внутри икосаэдрального капсида находится спиральный рибонуклеопротеид. Наружная оболочка, капсидная мембрана и нуклеоид на разрезе вириона расположены концентрически. Чувствительны к эфиру, термолабильны, относительно резистентны к УФ-лучам. Характерной чертой семейства является наличие в составе вириона РНК-зависимой ДНК-полимеразы, иначе называемой обратной транскриптазой. Это и послужило основой для названия семейства (от лат. retro — обратный). Вирионы имеют 6 структурных белков, из них 4 внутренних (капсидных) негликолизированных и 2 гликопротеина оболочки.
Основными структурными генами, кодирующими трансляцию белков, из которых в последующем строится вирус, являются gag (group-specific antigens), pol (polymerase), env (envelope). К регуляторным генам относятся: tat (трансактиватор всех вирусных белков), rev (регулятор экспрессии вирионных белков), vif (вирионный инфекционный фактор), vpr (функции остаются неясными), nef (негативный фактор экспрессии), vpx (функции неизвестны).
Капсидные белки несут группоспецифические межвидовые антигены и являются основой для разделения вирусов на роды и подроды. Гликопротеиды являются типоспецифическими антигенами, участвуют в реакции нейтрализации. Геном ретровирусов представлен однонитчатой РНК с молекулярной массой 7 мегадальтон и состоит из двух копий, каждая из которых является полноценным геномом и содержит одинаковую генетическую информацию, однако неизвестно, обе ли они функциональны. Нуклеиновая кислота онковирусов имеет гомологию с клеточной ДНК своего вида хозяина. Вирионная РНК неинфекционна. Вирусная РНК транскрибируется в ковалентно связанную двунитчатую ДНК, которая интегрируется с клеточной ДНК в виде ДНК-провируса. Провирус, экстрагированный из клетки, обладает инфекционностью. Многие вирусы этого семейства вызывают неопластические процессы, главным образом лейкемии и саркомы ряда видов животных. Нормальные клетки некоторых видов животных содержат интегрированные копии соответствующих видов онковирусов. Они могут никак не проявляться или активируются некоторыми физическими и химическими факторами, а возможно, и при инфекции другими онковирусами. Часто встречаются дефектные вирусы, размножающиеся с помощью вируса-помощника. Передаются вертикально и горизонтально.
Жизненный цикл
Ретровирус раздваивает функции своего генетического материала: инфекционную функцию, то есть функцию самораспространения, выполняет вирусная РНК, а функцию экспрессии вирусных генов и синтеза молекул РНК, которые затем перенесут генетическую информацию в другие клетки, выполняет вирусная ДНК.
Попадая внутрь клетки в ходе вирусной инфекции, ретровирусная РНК служит матрицей для синтеза ДНК путём хорошо теперь известного процесса обратной транскрипции. Эта ДНК встраивается в геномную ДНК и с этого момента становится неотъемлемой частью генома клетки. А вирус становится провирусом. Провирус для животной клетки это то же самое, что профаг для бактериальной. Идеи лизогении, по-видимому, и привели Говарда Темина, который вместе с Дэвидом Балтимором открыл обратную транскрипцию, к идее провирусного состояния ретровирусов. По информационному содержанию ДНК-вариант генома ретровируса отличается от РНК-варианта только тем, что ДНК содержит не короткие концевые повторы, а длинные концевые повторы, LTR.
Особенности трансляции РНК ретровирусов
Находясь в составе геномной ДНК, вирусные гены транскрибируются под контролем LTR.
LTR, long terminal repeats. Последовательности LTR включают в себя последовательности STR. Возникновение LTR очень важно для экспрессии вирусных генов. Они содержат вирусные регуляторные транскрипционные элементы: промотор, энхансер, и другие. Например, некоторые вирусы содержат элементы, определяющие зависимость вирусной транскрипции от наличия определённых гормонов. LTR и являются теми регуляторными сигналами, которые вирус использует для эксплуатации клеточной транскрипционной машины в своих целях.
Продуктом транскрипции является полноразмерная вирусная РНК. Она должна транслироваться. И здесь вирусу необходимо решить такую проблему: нужно синтезировать много белков, а РНК одна. И в клетках эукариот РНК моноцистронны, то есть предназначены для синтеза только одного белка. Синтез белка в большинстве случаев начинается с ближайшего к кэп-сайту инициирующего кодона[5].
Если просмотреть открытую рамку считывания от этого ближайшего инициирующего кодона, то мы увидим, что если бы вирус пользовался традиционными способами экспрессии, то он смог бы синтезировать только полипептид GAG. А дальше идёт стоп-кодон. Как быть с POL и ENV? Кроме того, эти полипептиды очень длинны, а в вирусе содержатся гораздо более короткие. Проблема решается несколькими способами.
Во-первых, с помощью сплайсинга эта одна РНК превращается в нашем упрощённом варианте ещё в одну, более короткую. При этом последовательности, кодирующие ENV полипептид, оказываются рядом с инициирующим кодоном, ближайшим к кэп-сайту, и начинают транслироваться.
Во-вторых, разными для разных ретровирусов способами они ухитряются[] обойти стоп-кодон после открытой рамки считывания GAG и синтезировать сплавленный полипротеин GAG-POL, который содержит последовательности обеих групп белков.
В-третьих, полученные длинные полипептиды подвергаются процессингу и разрезаются на множество белков, которые и функционируют либо в роли регуляторных, как, например, обратная транскриптаза, либо в роли структурных, как, например, белки оболочки зрелых вирусов.
Иными словами, ретровирусы используют гибкую тоталитарную систему для весьма тонкой регуляции синтеза большого разнообразия белков под контролем одного промотора.
Ретровирусы как векторы
Ретровирусы могут применяться в качестве векторов, например, в генотерапии. Механизм проникновения внутрь клеток при помощи слияния мембран. У них есть ряд преимуществ: широкий круг хозяев, стабильность в интегрированном в геном хозяина состоянии. Недостатки: сложно добиться высокого титра, заражает только делящиеся клетки.[]
Классификация
На март 2018 года в семейство включают 2 подсемейства с 6 и 5 родами соответственно[6]:
- Подсемейство Orthoretrovirinae (от др.-греч. ortho — прямой, собственно ретровирусы[7])
- Род Alpharetrovirus — Альфаретровирусы[8] (9 видов)
- Род Betaretrovirus — Бетаретровирусы[8] (5 видов)
- Род Gammaretrovirus — Гаммаретровирусы[8] (18 видов)
- Feline leukemia virus — Вирус лейкоза кошачьих
- Род Deltaretrovirus — Дельтаретровирусы (4 вида)
- Bovine leukemia virus — Вирус лейкоза крупного рогатого скота[8]
- Human T-lymphotropic virus — Т-лимфотропный вирус человека
- Род Epsilonretrovirus — Эпсилонретровирусы[8] (3 вида)
- Род Lentivirus — Лентивирусы (10 видов)
- Human immunodeficiency virus 1 — Вирус иммунодефицита человека 1
- Human immunodeficiency virus 2 — Вирус иммунодефицита человека 2
- Подсемейство Spumaretrovirinae (от лат. spuma — пена, в клетках с вирусами образуется множество вакуолей[7])
- Род Bovispumavirus (1 вид)
- Род Equispumavirus (1 вид)
- Род Felispumavirus (2 вида)
- Род Prosimiispumavirus (1 вид)
- Род Simiispumavirus (14 видов)
См. также
Примечания
- ↑ Таксономия вирусов (англ.) на сайте Международного комитета по таксономии вирусов (ICTV).
- ↑ Атлас по медицинской микробиологии, вирусологии и иммунологии : Учебное пособие для студентов медицинских вузов / Под ред. А. А. Воробьева, А. С. Быкова. — М. : Медицинское информационное агентство, 2003. — С. 132. — ISBN 5-89481-136-8.
- ↑ Coffin J; Blomberg J; Fan H; et al. (2021). "ICTV Virus Taxonomy Profile: Retroviridae 2021". J Gen Virol. 102 (12): 001712. doi:10.1099/jgv.0.001712. PMID 34939563.
- ↑ А. Марков. Данные сравнительной геномики проливают свет на происхождение ретровирусов Архивная копия от 12 марта 2008 на Wayback Machine
- ↑ Kozak, 1986 (см. в статье консенсусная последовательность Козак)
- ↑ Таксономия вирусов (англ.) на сайте Международного комитета по таксономии вирусов (ICTV). (Дата обращения: 6 апреля 2018).
- ↑ 1 2 3 4 Пиневич А. В., Сироткин А. К., Гаврилова О. В., Потехин А. А. Вирусология : учебник. — СПб. : Издательство Санкт-Петербургского университета, 2012. — С. 408—410. — ISBN 978-5-288-05328-3.
- ↑ 1 2 3 4 5 Сергеев В. А., Непоклонов Е. А., Алипер Т. И. Вирусы и вирусные вакцины. — М. : Библионика, 2007. — С. 348—351. — ISBN 5-98685-012-2.
Литература
- Хесин Р. Б. Непостоянство генома / Отв. ред. Ю. Н. Зограф, Б. А. Лейбович; Институт молекулярной генетики АН СССР. — М.: Наука, 1985. — 472 с. — 3000 экз.