
Термодинами́ческая фа́за — гомогенная часть гетерогенной системы, ограниченная поверхностью раздела. Менее строго, но более наглядно фазой называют гомогенную часть системы, отделенную от остальных частей видимой поверхностью раздела, на которой скачком меняются какие-либо характеристики фазы, например плотность, состав, оптические свойства. При этом совокупность отдельных гомогенных частей системы, обладающих одинаковыми свойствами, считается одной фазой. Каждая фаза системы характеризуется собственным уравнением состояния.
Фа́зовый перехо́д в термодинамике — переход вещества из одной термодинамической фазы в другую при изменении внешних условий. С точки зрения движения системы по фазовой диаграмме при изменении её интенсивных параметров, фазовый переход происходит, когда система пересекает линию, разделяющую две фазы. Поскольку разные термодинамические фазы описываются различными уравнениями состояния, всегда можно найти величину, которая скачкообразно меняется при фазовом переходе.

Глюко́за, или виноградный сахар, или декстроза (D-глюкоза), C6H12O6 — органическое соединение, моносахарид (6-атомный гидроксиальдегид, гексоза), один из самых распространённых источников энергии в живых организмах. Встречается в соке многих фруктов и ягод, в том числе и винограда, от чего и произошло название этого вида сахара. Глюкозное звено входит в состав полисахаридов (целлюлоза, крахмал, гликоген) и ряда дисахаридов (мальтозы, лактозы и сахарозы), которые в пищеварительном тракте расщепляются на мономеры: например, сахароза — на глюкозу и фруктозу, лактоза — на глюкозу и галактозу, и т. д.
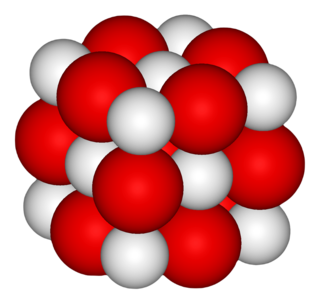
Oксид кальция — белое кристаллическое вещество, формула CaO. Относится к классу основных оксидов.

Эвте́ктика — нонвариантная точка в системе из n компонентов, в которой находятся в термодинамическом равновесии n твёрдых фаз и жидкая фаза. Эвтектическая композиция представляет собой жидкий раствор, кристаллизующийся при наиболее низкой температуре для сплавов данной системы. Соответственно, температура плавления сплава эвтектического состава — также самая низкая, по сравнению со сплавами другого состава для данной системы компонентов. Это явление как раз и отражает этимология термина.

Тетраоксид диазота (азотный тетраоксид, АТ, «амил») — вещество с формулой N2O4, преобладающее в жидкости, полученной охлаждением диоксида азота ниже точки кипения. Это теоретически бесцветная, но на практике окрашенная в жёлто-коричневый цвет (обусловленный примесью мономерного диоксида азота) летучая ядовитая жидкость с едким запахом. Температура кипения при атмосферном давлении +21,15 °C, кристаллизации — −11 °C. В кристаллическом виде при температурах ниже −12 °C бесцветен.

Сульфа́т меди(II) (медь(II) серноки́слая, традиционное название кристаллогидрата — ме́дный купоро́с) — неорганическое соединение, медная соль серной кислоты с формулой CuSO4.

Амо́рфные вещества́ (тела́) — конденсированное состояние веществ, атомная структура которых имеет ближний порядок и не имеет дальнего порядка, характерного для кристаллических структур. В отличие от кристаллов, стабильно-аморфные вещества не затвердевают с образованием кристаллических граней, и, обладают изотропией свойств, то есть не обнаруживают различия свойств в разных направлениях.
Раствори́мость — способность вещества образовывать с другими веществами однородные системы — растворы, в которых вещество находится в виде отдельных атомов, ионов, молекул или частиц. Растворимость выражается концентрацией растворённого вещества в его насыщенном растворе либо в процентах, либо в весовых или объёмных единицах, отнесённых к 100 г или 100 см³ (мл) растворителя. Растворимость газов в жидкости зависит от температуры и давления. Растворимость жидких и твёрдых веществ — практически только от температуры. Все вещества в той или иной степени растворимы в растворителях. В случае, когда растворимость слишком мала для измерения, говорят, что вещество нерастворимо.

Метастабильное состояние — состояние квазиустойчивого равновесия физической системы, в котором система может находиться длительное время.
Выпаривание — это метод химико-технологической обработки для выделения растворителя из раствора, концентрирования раствора, кристаллизации растворенных веществ. Иногда выпаривание проводят до получения насыщенных растворов, с целью дальнейшей кристаллизации из них твёрдого вещества. Выпаривание широко применяется в химической промышленности. Производство многих продуктов проходит в жидкой фазе, в виде суспензий и эмульсий, а для получения целевого продукта жидкую фазу следует удалить. Наиболее простым и производительным способом является тепло- и массообмен. Выпаривание принципиально отличается от испарения тем, что при выпаривании обычно осуществляется частичное удаление растворителя из всего объёма раствора при его температуре кипения, а испарение происходит с поверхности раствора при любых температурах ниже температуры кипения.

Ацета́т на́трия (этаноа́т на́трия, химическая формула — C2H3O2Na или CH3COONa или AcONa) — органическая натриевая соль уксусной кислоты.

Грелка каталитическая — химическая грелка, предназначенная для индивидуального согревания человека за счёт беспламенного окисления паров бензина высокой очистки, например, Нефрас С2 80/120 или спирта 95—97% в присутствии катализатора. Часто каталитической грелкой неверно называют инфракрасный обогреватель.
Расплав — жидкое расплавленное состояние вещества при температурах в определённых границах, удалённых от критической точки плавления и расположенных между температурами плавления и кипения.
CALPHAD — метод расчёта фазовых диаграмм, предложенный Л. Кауфманом в 1960-х годах. Под равновесными фазовыми диаграммами обычно понимают диаграммы зависимости состава химической системы от температуры. На фазовой диаграмме отмечаются области существования соединений и растворов и области их сосуществования. Фазовые диаграммы — очень мощный инструмент для прогнозирования состояния системы при различных условиях. Впервые они появились как графический метод обобщения экспериментальной информации о равновесии. В сложных системах вычислительные методы, такие как CALPHAD, используются для моделирования термодинамических свойств для каждой фазы и моделирования поведения многокомпонентной системы в целом. Подход CALPHAD базируется на том факте, что фазовая диаграмма — это проявление равновесных термодинамических свойств системы, которые слагаются из свойств составляющих систему фаз. Таким образом, существует возможность расчёта фазовой диаграммы путём начальной оценки термодинамических свойств всех фаз системы.
Па́мять с измене́нием фа́зового состоя́ния — компьютерная память на основе фазового перехода, также известна как PCM, PRAM, PCRAM, Ovonic Unified Memory, Chalcogenide RAM, C-RAM — тип энергонезависимой памяти (NVRAM), основанный на свойствах халькогенидов, которые при изменении температуры могут «переключаться» между двумя состояниями: кристаллическим и аморфным. В последних разработках[каких?] смогли добавить ещё два дополнительных состояния, что удвоило информационную ёмкость чипов при прочих равных.

Пересы́щенный пар — пар, давление которого превышает давление насыщенного пара при данной температуре. Может быть получен путём увеличения давления пара в объёме, свободном от центров конденсации. Другой способ получения — охлаждение насыщенного пара при тех же условиях. В связи с последним способом получения насыщенного пара применительно к нему используется также наименование переохлаждённый пар. Кроме того, иногда в литературе встречается термин перенасыщенный пар.
Гре́лка, также термофор — устройство для согревания части тела сухим теплом с целью обогрева и предупреждения переохлаждения, либо для местного теплолечения; грелкой может называться и небольшое устройство для обогрева комнаты.

Солевая железа, или надглазничная железа, — особый орган у птиц, позволяющий эффективно выводить излишки соли из организма и являющийся частью осморегулирующей системы. Позволяет морским птицам удовлетворять потребности в жидкости за счёт морской воды и является основным органом, выводящим большую часть солей из организма этих птиц.
Температура замерзания — температура, при которой вещество совершает фазовый переход из жидкого состояния в твёрдое. Обычно совпадает с температурой плавления. Формирование кристаллов происходит при специфичной для конкретного вещества температуре, слегка варьирующейся с давлением; в некристаллических аморфных телах затвердевание происходит в определённом диапазоне температур. В случае аморфных тел температурой плавления считается точка, в которой исчезают последние признаки твёрдой фазы, а температурой замерзания — точка, в которой, наоборот, полностью исчезает жидкая фаза; и эти две температуры различаются.













