Стентирование

Стенти́рование — медицинское оперативное вмешательство, проводимое с целью установки стента — специального каркаса, который помещается в просвет полых органов человека или животного, например, коронарных сосудов сердца или жёлчного протока, и обеспечивает расширение участка, суженного патологическим процессом. Стентирование следует отличать от шунтирования, то есть создания обходного пути вместо поражённого участка сосуда. Операцию на коронарных сосудах проводит кардиохирург. Операции на внутренних органах проводят профильные специализированные хирурги.
Значимость
Сердечные заболевания являются одной из главных причин смертности людей. По данным ВОЗ, в 2019 году в мире 17,9 миллиона человек умерли от болезней сердечно-сосудистой системы, что составило 32 % от всех смертей[1]. Проблемы с сердечно-сосудистой системой чаще встречаются у лиц старше 50 лет. Тем не менее, из-за нездорового образа жизни риск возникновения таких заболеваний увеличивается и среди более молодого населения, что также включает их в группу риска. Сердце — мощный мышечный насос, обеспечивающий циркуляцию крови. С циркулирующей кровью к органам и тканям поступают питательные вещества и кислород, без которых была бы невозможна их жизнедеятельность и работа самого сердца.
Для совершения этой значительной работы сердцу необходимо большое количество кислорода, за доставку которого отвечает разветвлённая система коронарных артерий. Патологическое изменение состояния сосудов неизменно ведёт к ухудшению кровоснабжения сердца и, как следствие, к развитию серьёзных сердечно-сосудистых заболеваний.
Атеросклероз — наиболее распространённое хроническое заболевание, поражающее артерии. Постепенно растущие на внутренней оболочке сосудистой стенки атеросклеротические бляшки, одиночные или множественные, являются главным образом холестериновыми отложениями.
Разрастание в артерии соединительной ткани (склероз) и кальциноз стенки сосуда приводят к медленно прогрессирующей деформации, сужению просвета вплоть до полного запустевания (облитерации) артерии и тем самым вызывают хроническую, медленно нарастающую недостаточность кровоснабжения органа, питаемого через поражённую артерию. В случае недостаточности кровоснабжения сердечной мышцы человек может ощущать развитие следующих симптомов:
- боли в грудной клетке, сопровождающиеся чувством страха смерти
- тошнота
- одышка
- тахикардия
- чрезмерное потоотделение.
Однако подобные симптомы могут быть связанными с другими причинами или другими заболеваниями не кардиологической этиологии, или вообще не проявляться, отчего затягивается процесс обращения к специалистам и затрудняется последующее лечение.
Кроме наследственной обусловленности развитию заболевания сердца способствуют повторяющиеся психоэмоциональные напряжения (стрессы), курение, неправильное питание, ведущее к нарушению обмена веществ, и сниженная физическая активность. В связи с пандемией COVID-19 Всемирная организация здравоохранения распространила данные исследований, указывающие на связь вирусной инфекции с заболеваниями сердца, наблюдавшимися в 2020—2021 годы во время пандемии, в которой причины смертности от вирусного заболевания включают и кардиологические осложнения. COVID-19 и больное сердце составляют сложный и опасный конандрум; исследования подтверждают связь кардиологических осложнений с пандемией.[2]
Сужение сосудов приводит к тому, что сердечная мышца — миокард — страдает от недостатка кислорода. Сердце, находящееся в ишемии, постепенно декомпенсируется и все менее успешно выполняет свою функцию. Через некоторое время развивается ишемическая болезнь сердца.
Кардиологи имеют на вооружении много прогрессивных методов оперативного лечения. До появления внутрисосудистых методов лечения единственным хирургическим методом лечения ишемической болезни сердца была операция коронарного шунтирования (создание шунта в обход суженного участка кровеносного сосуда). Сейчас многим больным удаётся избежать хирургического вмешательства благодаря использованию эффективных и малотравматичных методов, одним из которых является коронарное стентирование (имплантация коронарного стента).
Сущность метода
Концепцию расширения поражённых участков сосуда с помощью некоего каркаса ещё 50 лет назад предложил американский радиолог, один из пионеров интервенционной радиологии Чарлз Доттер (Charles Dotter, 1920—1985). Разработка метода заняла длительное время, первая операция по этой технологии была произведена только в 1986 году. И лишь в 1993 году была доказана эффективность метода стентирования для восстановления проходимости коронарной артерии и удержания её в новом состоянии в дальнейшем.
Стент — это тонкая металлическая трубочка, состоящая из проволочных ячеек, раздуваемая специальным баллоном. Он вводится в поражённый сосуд и, расширяясь, вжимается в стенки сосуда, увеличивая его просвет. Так улучшается кровоснабжение сердца.
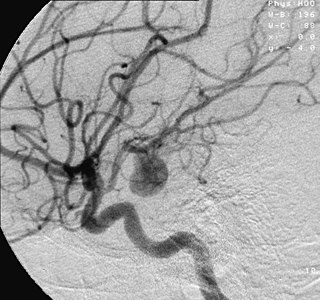
На стадии диагностики выполняется коронарная ангиография, позволяющая определить характер, месторасположение и степень сужения коронарных сосудов. По специальному катетеру через бедренную артерию вводится контрастное вещество, с током крови оно заполняет коронарные артерии, что позволяет их визуализировать. Рентгеновские снимки делаются под несколькими углами, результат выводится на монитор и архивируется в цифровом формате.
В специально оборудованной операционной под рентгеновским контролем производят операцию, постоянно регистрируя кардиограмму пациента. Для этой операции не требуется осуществления разрезов, проводится она под местным обезболиванием. Пациент может говорить в процессе и сообщать о своём самочувствии, делать вдохи и задерживать дыхание по просьбе врача.
Через сосуд на бедре или руке в устье суженной коронарной артерии вводится специальный катетер, через который проводится тонкий металлический проводник под наблюдениями на мониторе. Проводник снабжён специальным баллончиком, размер которого подбирается в соответствии с особенностями суженного участка. На баллончике смонтирован в сжатом состоянии стент, который обязательно совместим с органами и тканями человека, гибкий и упругий, подстраивающийся под состояние сосуда. Введённый баллончик на проводнике раздувается, стент расширяется и вдавливается во внутреннюю стенку. Для полной уверенности в том, что стент расширился правильно, баллон раздувается несколько раз. Затем баллон сдувается и удаляется из артерии вместе с проводником и катетером. Стент остаётся и сохраняет просвет сосуда. В зависимости от размера поражённого сосуда могут использоваться один или несколько стентов.
При введении катетера в артерию используют йодсодержащее вещество, поэтому у пациента не должно быть аллергии на йод. К тому же при обострении хронических заболеваний желательно по возможности отложить плановые процедуры (впрочем, это правило актуально для любых оперативных вмешательств, являющихся серьёзным стрессом для организма).
Прогноз
Обычно результаты операции хорошие, она относительно безопасна и риск осложнений после неё минимален. Иногда возможна аллергическая реакция организма на вещество, вводимое в процессе операции для рентгеновского наблюдения. Бывает также гематома или кровотечение в месте пункции артерии. Для профилактики осложнений пациент остаётся в отделении интенсивной терапии с соблюдением постельного режима. Уже через несколько дней, после заживления ранки в месте пункции, прооперированный пациент выписывается из стационара. Ограничения после этого обычно снимаются, человек возвращается к обычной жизни, а наблюдение проводится периодически у врача по месту жительства.
Бескровность и видимая простота операции, короткий послеоперационный период и эффективность коронарного стентирования делают его современным и популярным решением проблемы многих сердечно-сосудистых заболеваний. В отличие от хирургической операции, которая проходит с использованием искусственного кровообращения, процедура стентирования длится 30-40 минут и практически не даёт осложнений.
Стентирование не обладает абсолютной эффективностью, примерно в 15-20 % случаев происходит обратный процесс, и сосуд снова сужается. Одной из причин такого процесса является чрезмерное разрастание мышечной ткани, и, как следствие, сужение стенки сосуда. Однако исследования кардиологов не прекращаются, улучшая технологию коронарного стентирования и добиваясь все более стабильной положительной статистики результатов. Так, сейчас разработано новое поколение стентов со специальным лекарственным покрытием. Оболочка такого стента в течение нескольких недель постепенно высвобождает лекарство, предотвращающее чрезмерное разрастание тканей. Применение стентов нового поколения значительно снижает количество случаев, когда необходима повторная операция (повторное сужение наблюдается лишь в 5 % случаев). Однако этот метод до сих пор сталкивался с проблемами, связанными с несовершенством таких покрытий.
В 2019 году международный научный коллектив, работающий на базе Томского политехнического университета (ТПУ) под руководством российских специалистов, разработал новое лекарствовыделяющее покрытие для сосудистых стентов, которое лишено многих из упомянутых несовершенств. Новое покрытие на основе полидиметилсилоксановой матрицы представляет собой систему постепенно биоразлагаемых цилиндрических микрокамер диаметром 5 мкм и высотой 3 мкм каждая[3]. Внутрь каждой такой камеры российские учёные научились помещать дозированный лекарственный препарат, который, постепенно выделяясь из силоксанового покрытия, предотвращает повторное сужение сосуда, образование в нём бляшек и тромбов. Скоростью выделения препарата из инновационного микрокамерного покрытия стента можно управлять с помощью ультразвука[3]. Такое «умное» покрытие можно использовать на коронарных стентах, что позволит получить дополнительный фармакологический эффект[4][5].
В настоящее время разработано около 400 различных моделей стентов, и развитие метода ведёт к постоянной их модернизации. Эти стенты различаются сплавом, из которого они изготовлены, длиной, формой отверстий, покрытием поверхности, контактирующей с кровью, системой доставки в коронарные сосуды. Так, кроме раскрываемых баллоном, существуют самораскрывающиеся стенты и др.
Однако стоит помнить, что даже самые совершенные методы кардиохирургии не отменяют необходимости профилактики и внимательного отношения к своему здоровью и здоровью своего сердца. Регулярные физические нагрузки, соразмерные возрасту и физическим возможностям, свежий воздух, рациональное питание, обогащённое витаминами и исключающее прибавку массы тела, ограничение потребления продуктов, содержащих холестерин, — это понятия, никогда не теряющие своей актуальности.
Стентирование жёлчных протоков
Стентирование жёлчных протоков осуществляется посредством установки специальных билиарных стентов. Основная цель установки билиарного стента состоит в обеспечении эффективного протока желчи в просвет двенадцатиперстной кишки. Этот эффект достигается путём установки полой трубки из металла или пластика в жёлчный проток эндоскопическими методами[6]. Первые установки билиарных стентов были проведены в 1980 году двумя различными командами: Soehendra N. & Reynders-Frederix V.[7] и Laurence B.H. & Cotton P.B.[8]. Тогда же стало очевидно, что предпочтительнее установка стентов бо́льшего диаметра, поскольку это уменьшает риск воспаления жёлчных путей и продлевает период билиарной проходимости[9].
Следующим этапом в развитии стало использование стентов из самораскрывающихся металлических сеток, расширяющихся в месте имплантации. Эта особенность сделала использование самораскрывающиеся металлических стентов (SEMS) более подходящим, чем пластиковых, особенно при первичном лечении злокачественной структуры жёлчных протоков. С тех пор характеристики SEMS-стентов непрерывно улучшались по двум основным направлениям: обеспечение продления проходимости протока при злокачественных заболеваниях; и обеспечение возможности оперативной замены или удаления стента[9]. Со временем билиарные стенты подвергались различным модификациям для улучшения терапии, как злокачественных непроходимостей жёлчных путей, так и доброкачественных стенозов. Разработаны различные типы функциональных стентов, такие как антимиграционные стенты, легко извлекаемые или меняющие форму стенты, противогиперплазивные стенты, стенты с высвобождающимся со временем лекарственным покрытием (DES), радиоактивные стенты и биодеградируемые стенты[10].
Элютированные стенты с высвобождающимся со временем лекарственным покрытием применяются, например, для предотвращения опухолевого прорастания в стент (обработка стента антиопухолевыми агентами). При этом как металлические, так и полимерные элютированные стенты используются для предотвращения рестеноза жёлчного протока[9]. Увеличение эффективности элютированных стентов связано с использованием сурфактантов и усилителей действия лекарств, модификацией структуры стентов, улучшения материалов для изготовления стента, обработкой металлической поверхности, методами нанесения препаратов, и новыми типами полимеров[10]. Антирефлюксные стенты (ARS) с клапаном предотвращают попадание панкреатического сока в жёлчный проток и дальнейшее развитие холангита[10].
Считается, что возможности совершенствования и модификации стентов ограничены, поскольку стент представляет собой инородное тело в человеческом организме[6]. Улучшение функциональных свойств стентов в ближайшей перспективе позволит продлевать период билиарной проходимости и терапевтического действия под каждую конкретную патологию[10]. Перспективным является использование биодеградируемых билиарных стентов с различным покрытием[11].
Примечания
- ↑ ВОЗ Всемирная организация здравоохранения. Cardiovascular diseases (CVDs). Key facts: 17.9 million people died from CVDs in 2019, representing 32 % of all global deaths. [1] Архивная копия от 18 апреля 2018 на Wayback Machine
- ↑ COVID-19 и сердце [2] Архивная копия от 19 ноября 2022 на Wayback Machine
- ↑ 1 2 Yulia Zykova, Valeriya Kudryavtseva, Meiyu Gai, Anna Kozelskaya, Johannes Frueh. Free-standing microchamber arrays as a biodegradable drug depot system for implant coatings // European Polymer Journal. — 2019-05-01. — Т. 114. — С. 72—80. — ISSN 0014-3057. — doi:10.1016/j.eurpolymj.2019.02.029. Архивировано 25 мая 2019 года.
- ↑ "Сосуды без тромбов": в России создано уникальное покрытие для стентов. РИА Новости (22 мая 2019). Дата обращения: 25 мая 2019. Архивировано 25 мая 2019 года.
- ↑ Российские и зарубежные ученые создали уникальное покрытие для стентов. www.tatar-inform.ru. Дата обращения: 25 мая 2019. Архивировано 24 мая 2019 года.
- ↑ 1 2 Дюжева Т. Г. и др. Перспективы создания тканеинженерного желчного протока //Гены и клетки. — 2016. — Т. 11. — №. 1. — С. 43-7.
- ↑ Soehendra N., Reynders-Frederix V. Palliative bile duct drainage-a new endoscopic method of introducing a transpapillary drain //Endoscopy. — 1980. — Т. 12. — №. 01. — С. 8-11.
- ↑ Laurence B. H., Cotton P. B. Decompression of malignant biliary obstruction by duodenoscopic intubation of bile duct //Br Med J. — 1980. — Т. 280. — №. 6213. — С. 522—523.
- ↑ 1 2 3 Blero D., Huberty V., Devière J. Novel biliary self-expanding metal stents: indications and applications //Expert review of gastroenterology & hepatology. — 2015. — Т. 9. — №. 3. — С. 359—367.
- ↑ 1 2 3 4 Jang S. I., Lee D. K. Stents with specialized functions: drug-eluting stents and stents with antireflux devices //Gastrointestinal Intervention. — 2015. — Т. 4. — №. 1. — С. 50-54.
- ↑ Дюжева Т. Г. и др. Биодеградируемые материалы и методы тканевой инженерии в хирургии желчных протоков //Анналы хирургической гепатологии. — 2012. — Т. 17. — №. 1. — С. 94-99.
См. также
- Чарлз Теодор Доттер (англ.)
- Аортокоронарное шунтирование