
Органи́ческая хи́мия — раздел химии, изучающий структуру, свойства и методы синтеза соединений углерода с другими химическими элементами, относящихся к органическим соединениям. Первоначальное значение термина органическая химия подразумевало изучение только соединений углерода растительного и животного происхождения. По этой причине ряд углеродсодержащих соединений традиционно не относят к органическим, а рассматривают как неорганические соединения. Условно можно считать, что структурным прототипом органических соединений являются углеводороды.
Сте́пень окисле́ния — вспомогательная условная величина для записи процессов окисления, восстановления и окислительно-восстановительных реакций. Она указывает на состояние окисления отдельного атома молекулы и представляет собой лишь удобный метод учёта переноса электронов: она не является истинным зарядом атома в молекуле.
Гетероциклические соединения (гетероциклы) — органические соединения, содержащие циклы, в состав которых входят атомы как минимум двух различных элементов. Могут рассматриваться как карбоциклические соединения с гетерозаместителями (гетероатомами) в цикле. Наиболее разнообразны и хорошо изучены ароматические азотсодержащие гетероциклические соединения. Предельные случаи гетероциклических соединений — соединения, не содержащие атомов углерода в цикле, например, пентазол.

Хими́ческое соедине́ние — сложное вещество, состоящее из химически связанных атомов двух или более элементов. Некоторые простые вещества также могут рассматриваться как химические соединения, если их молекулы состоят из атомов, соединённых ковалентной связью . Инертные (благородные) газы и атомарный водород нельзя считать химическими соединениями.
Хими́ческая фо́рмула — условное обозначение химического состава и структуры соединений с помощью символов химических элементов, числовых и вспомогательных знаков. Химические формулы являются составной частью языка химии, на их основе составляются схемы и уравнения химических реакций, а также химическая классификация и номенклатура веществ. Одним из первых начал использовать их русский химик А. А. Иовский.

Функциона́льная гру́ппа — атом или группа атомов, которые, являясь структурными фрагментами разных химических соединений, проявляют похожие химические свойства. Определяют характерные физические и химические свойства класса химических соединений .

Фри́дрих А́вгуст Ке́куле фон Штра́дониц — немецкий химик-органик, прославившийся созданием теории валентности. Впервые применил теорию валентности к органическим веществам.
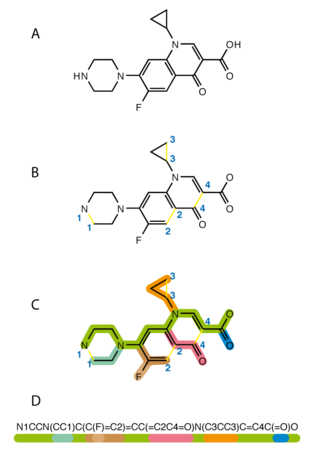
SMILES — система правил (спецификация) однозначного описания состава и структуры молекулы химического вещества с использованием строки символов ASCII. Название в английском языке является омонимом к слову smiles (улы́бки), однако пишется только заглавными буквами. В русском языке однозначного аналога не имеет, рекомендуется употребление на языке оригинала. Произносится как «смайлз».

Вале́нтность — способность атомов образовывать определённое количество химических связей, которые образует атом, или число атомов, которое может присоединить или заместить атом данного элемента.

Аромати́чность — особое свойство некоторых химических соединений, благодаря которому сопряжённое кольцо ненасыщенных связей проявляет аномально высокую стабильность; большую чем та, которую можно было бы ожидать только при одном сопряжении.
Алифатические соединения в органической химии — соединения, не содержащие ароматических связей. Алифатические соединения могут представлять собой открытые цепи или замкнутые. Иногда к алифатическим соединениям относят только ациклические, а алициклические выделяют в отдельный класс.
Углеводоро́дный радика́л (от лат. radix «корень»), также углеводоро́дный оста́ток в химии — группа атомов, соединённая с функциональной группой молекулы. Обычно при химических реакциях радикал переходит из одного соединения в другое без изменения. Но радикал и сам может содержать функциональные группы, поэтому с его «неизменностью» нужно быть осторожным: например, аминокислота аспарагиновая кислота содержит в той части молекулы, которая в общем виде рассматривается как остаток аминокислоты, ещё одну карбоксильную группу. Часто углеводородный радикал называют просто радикал, что может вызвать путаницу с понятием свободного радикала. Некоторые углеводородные радикалы могут также являться функциональными группами, например, фенил (−C6H5), винил (−C2H3) и др. Углеводородными радикалами обычно являются остатки углеводородов, которые входят в состав многих органических соединений.

Пи-связь (π-связь) — ковалентная связь, образующаяся перекрыванием атомных p-орбиталей. В отличие от сигма-связи, осуществляемой перекрыванием s-орбиталей вдоль линии соединения атомов, пи-связи возникают при перекрывании p-орбиталей по обе стороны от линии соединения атомов. Считается, что пи-связь реализуется в кратных связях — двойная связь состоит из одной сигма- и одной пи-связи, тройная — из одной сигма- и двух ортогональных пи-связей.

Теория валентных связей — приближённый квантовохимический расчётный метод, основанный на представлении о том, что каждая пара атомов в молекуле удерживается вместе при помощи одной или нескольких общих электронных пар.
Циклические соединения — химические соединения, в которых присутствует три или более связанных атомов, образующие кольцо. Соединение, кольцо которого включает 9 и более атомов, называется макроциклическим.

Проекция Фишера — способ изображения трёхмерной молекулы в виде проекции, в которой вертикальные связи удаляются за проекционную плоскость, а горизонтальные связи выступают перед этой плоскостью. Данные формулы были предложены Э. Фишером в 1891 году для изображения структур углеводов. Использование проекций Фишера для неуглеводных молекул может ввести в заблуждение и не рекомендуется ИЮПАК.
Псевдогалоге́ны (галогено́иды) — сильно связанные, как правило линейные, молекулярные одновалентные неорганические радикалы (далее обозначены Z), которые проявляют химические свойства, характерные для галогенов, т.е. способны образовывать:
- однозарядные анионы Z−,
- псевдогалогенводородные кислоты HZ,
- малорастворимые соли серебра AgZ, ртути(I) Hg2Z2 и свинца(II) PbZ2,
- нейтральные димеры — дипсевдогалогены Z2, диспропорционирующие в воде и способные атаковать двойную связь,
- интерпсевдогалогенные молекулы Z–X.
Сопряжение связей — это явление выравнивания связей и зарядов в реальной молекуле по сравнению с несуществующей идеальной структурой этой молекулы. Происходит из-за взаимодействия между собой электронных систем атомов. За счёт сопряжения происходит изменение длины кратных и одинарных связей, что в свою очередь вызывает геометрическое изменение строения молекулы. Главным признаком сопряжения является распределение электронной плотности по всей системе. Системы, в которых происходит сопряжение, называются сопряжёнными системами, которые делятся на открытые и циклические. Чтобы сопряжение произошло, необходимо, чтобы все электронные системы находились в одной плоскости для взаимодействия друг с другом, и для образования плоского σ-скелета. Если этого не происходит из-за структурного строения молекулы, то говорят о пространственных препятствиях сопряжению.

Гексаметилбензол, также известный как меллитен, представляет собой углеводород с молекулярной формулой C12H18 и конденсированной структурной формулой C6(CH3)6. Это ароматическое соединение и производное бензола, где шесть атомов водорода бензола заменены метильной группой. В 1929 году Кэтлин Лонсдейл сообщила о кристаллической структуре гексаметилбензола, продемонстрировав, что центральное кольцо является гексагональным и плоским, и тем самым закончила продолжающиеся дебаты о физических параметрах бензольной системы. Это был исторически значимый результат, как для области рентгеновской кристаллографии, так и для понимания ароматичности.
Арильная группа (арил) — в химии группа углеводородных радикалов, производная от простого ароматического кольца, в котором удален один атом водорода. В названии углеводорода применяется суффикс -yl (-ил), например, индолил, фенил и т. д. Арильную группу часто называют просто «арил». В химических формулах обозначается Ar, что совпадает с обозначением химического элемента аргона, но смешивание этих понятий маловероятно, так как арильная группа используется в соединениях органической химии, а аргон — инертный газ, способность которого образовывать вообще какие-либо соединения по состоянию на 2021 год не доказана.











