Температура
| Температура | |
|---|---|
| , | |
| Размерность | Θ |
| Единицы измерения | |
| СИ | К |
| СГС | К |
Температу́ра (от лат. temperatura — надлежащее смешение, нормальное состояние) — скалярная физическая величина, характеризующая термодинамическую систему и количественно выражающая интуитивное понятие о различной степени нагретости тел.
Живые существа способны воспринимать ощущения тепла и холода непосредственно, с помощью органов чувств. Однако точное определение температуры требует, чтобы температура измерялась объективно, с помощью измерительных приборов. Такие приборы называются термометрами и измеряют так называемую эмпирическую температуру. В эмпирической шкале температур устанавливаются одни реперные точки и число делений между ними — так были введены используемые ныне шкалы Цельсия, Фаренгейта и другие. Измеряемая в кельвинах абсолютная температура вводится по одной реперной точке[1] с учётом того, что в природе существует минимальное предельное значение температуры — абсолютный нуль. Верхнее значение температуры ограничено планковской температурой.
Если система находится в тепловом равновесии, то температура всех её частей одинакова. В противном случае в системе происходит передача энергии от более нагретых частей системы к менее нагретым, приводящая к выравниванию температур в системе, и говорят о распределении температуры в системе или скалярном поле температур. В термодинамике температура — интенсивная термодинамическая величина.
Наряду с термодинамическим, в других разделах физики могут вводиться и другие определения температуры. В молекулярно-кинетической теории показывается, что температура пропорциональна средней кинетической энергии частиц системы. Температура определяет распределение частиц системы по уровням энергии (см. Статистика Максвелла — Больцмана), распределение частиц по скоростям (см. Распределение Максвелла), степень ионизации вещества (см. Уравнение Саха), спектральную плотность излучения (см. Формула Планка), полную объёмную плотность излучения (см. Закон Стефана — Больцмана) и т. д. Температуру, входящую в качестве параметра в распределение Больцмана, часто называют температурой возбуждения, в распределение Максвелла — кинетической температурой, в формулу Саха — ионизационной температурой, в закон Стефана — Больцмана — радиационной температурой. Для системы, находящейся в термодинамическом равновесии, все эти параметры равны друг другу, и их называют просто температурой системы[2].
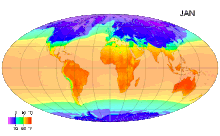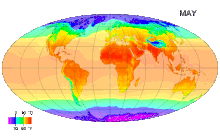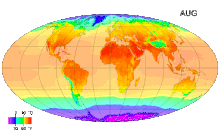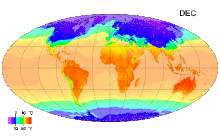


В Международной системе величин (англ. International System of Quantities, ISQ) термодинамическая температура выбрана в качестве одной из семи основных физических величин системы. В Международной системе единиц (СИ), основанной на Международной системе величин, единица этой температуры — кельвин — является одной из семи основных единиц СИ[3]. В системе СИ и на практике используется также температура Цельсия, её единицей является градус Цельсия (°С), по размеру равный кельвину[4]. Это удобно, так как большинство климатических процессов на Земле и процессов в живой природе связаны с диапазоном от −50 до +50 °С.
Температура как локальный параметр. Температурное поле
Физика сплошных сред рассматривает температуру как локальную макроскопическую переменную, то есть величину, характеризующую мысленно выделяемую область (элементарный объём) сплошной среды (континуума), размеры которой бесконечно малы по сравнению с неоднородностями среды и бесконечно велики по отношению к размерам частиц (атомов, ионов, молекул и т. п.) этой среды[5]. Значение температуры может меняться от точки к точке (от одного элементарного объёма к другому); распределение температуры в пространстве в данный момент времени задаётся скалярным полем температуры (температурным полем)[6]. Температурное поле может быть как нестационарным (изменяющимся во времени), так и не зависящим от времени стационарным. Среду с одинаковыми во всех точках значениями температуры называют термически однородной. Математически температурное поле описывают уравнением зависимости температуры от пространственных координат (иногда рассмотрение ограничивают одной или двумя координатами) и от времени. Для термически однородных систем
Термодинамическое определение
История термодинамического подхода
Слово «температура» возникло в те времена, когда люди считали, что в более нагретых телах содержится большее количество особого вещества — теплорода, чем в менее нагретых[7].
В равновесном состоянии температура имеет одинаковое значение для всех макроскопических частей системы. Если в системе два тела имеют одинаковую температуру, то между ними не происходит передачи кинетической энергии частиц (тепла). Если же существует разница температур, то тепло переходит от тела с более высокой температурой к телу с более низкой.
Температура связана также с субъективными ощущениями «тепла» и «холода», связанными с тем, отдаёт ли живая ткань тепло или получает его.
Некоторые квантовомеханические системы (например, рабочее тело лазера, в котором присутствуют инверсно заселённые уровни) могут находиться в состоянии, при котором энтропия не возрастает, а убывает при добавлении энергии, что формально соответствует отрицательной абсолютной температуре. Однако такие состояния находятся не «ниже абсолютного нуля», а «выше бесконечности», поскольку при контакте такой системы с телом, обладающим положительной температурой, энергия передаётся от системы к телу, а не наоборот (подробнее см. Отрицательная абсолютная температура).
Свойства температуры изучает раздел физики — термодинамика. Температура также играет важную роль во многих областях науки, включая другие разделы физики, а также химию и биологию.
Равновесная и неравновесная температуры
Система, находящаяся в состоянии термодинамического равновесия, имеет стационарное температурное поле. Если в такой системе отсутствуют адиабатические (энергонепроницаемые) перегородки, то все части системы имеют одну и ту же температуру. Иначе говоря, равновесная температура термически однородной системы не зависит явно от времени (но может меняться в квазистатических процессах). Неравновесная система в общем случае имеет нестационарное температурное поле, в котором каждый элементарный объём среды имеет собственную неравновесную температуру, в явном виде зависящую от времени.
Температура в феноменологической термодинамике
Определение температуры в феноменологической термодинамике зависит от способа построения математического аппарата данной дисциплины (см. Аксиоматика термодинамики).
Отличия в формальных определениях термодинамической температуры в различных системах построения термодинамики не означают большую наглядность некоторых из таких систем по сравнению с другими, ибо во всех этих системах, во-первых, в описательном определении температуру рассматривают как меру нагретости/охлаждённости тела, и, во-вторых, содержательные определения, устанавливающие связь между термодинамической температурой и используемыми для её измерения температурными шкалами, совпадают.
В рациональной термодинамике, изначально отвергающей деление этой дисциплины на термодинамику равновесную и термодинамику неравновесную (то есть не проводящей различия между равновесной и неравновесной температурами), температура есть первоначальная неопределяемая переменная, описываются только такими свойствами, которые можно выразить языком математики[8]. Понятия энергии, температуры, энтропии и химического потенциала вводятся в рациональной термодинамике одновременно; по отдельности определить их принципиально нельзя. Методика введения этих понятий показывает, что можно ввести в рассмотрение много различных температур, отвечающих разным энергетическим потокам. Например, можно ввести температуры трансляционных и спинорных движений, температуру радиационных излучений и т. д.[9]
Нулевое начало (закон) вводит в равновесную термодинамику понятие эмпирической температуры[10][11][12][13] как параметра состояния, равенство которого во всех точках есть условие термического равновесия в системе без адиабатических перегородок.
В подходе к построению термодинамики, используемом последователями Р. Клаузиуса[14], равновесные параметры состояния — термодинамическую температуру и энтропию — задают посредством термодинамического параметра, характеризующего термодинамический процесс. А именно,
| (Термодинамическая температура и энтропия по Клаузиусу) |
где — количество теплоты, получаемое или отдаваемое закрытой системой в элементарном (бесконечно малом) равновесном процессе. Далее понятие о термодинамической температуре по Клаузиусу распространяют на открытые системы и неравновесные состояния и процессы, обычно не оговаривая специально, что речь идёт о включении в используемый набор законов термодинамики дополнительных аксиом.
В аксиоматике Каратеодори[15][16] рассматривают как дифференциальную форму Пфаффа, а равновесную термодинамическую температуру — как интегрирующий делитель этой дифференциальной формы[17].
В системе аксиом А. А. Гухмана[18][19] изменение внутренней энергии системы в элементарном равновесном процессе выражают через потенциалы взаимодействия и координаты состояния:
| (Уравнение Гухмана) |
причём тепловым потенциалом служит термодинамическая температура , а тепловой координатой — энтропия ; давление (с обратным знаком) играет роль потенциала механического деформационного взаимодействия для изотропных жидкостей и газов, а сопряжённой с давлением координатой служит объём; при химических и фазовых превращениях координатами состояния и потенциалами служат массы компонентов и сопряжённые с ними химические потенциалы. Другими словами, в аксиоматике Гухмана температуру, энтропию и химические потенциалы вводят в равновесную термодинамику одновременно посредством фундаментального уравнения Гиббса. Используемый Гухманом и его последователями термин координаты состояния, в перечень которых наряду с геометрическими, механическими и электромагнитными переменными включают энтропию и массы компонентов, исключает неоднозначность, связанную с термином обобщённые термодинамические координаты: одни авторы относят к обобщённым координатам, помимо прочих переменных, энтропию и массы компонентов[20], тогда как другие ограничиваются геометрическими, механическими и электромагнитными переменными[21].)
В термодинамике Гиббса равновесную температуру выражают через внутреннюю энергию и энтропию[22][23][24]
| (Термодинамическая температура по Гиббсу) |
где — набор (без энтропии) естественных переменных внутренней энергии, рассматриваемой как характеристические функции. Равенство температур во всех точках системы без адиабатических перегородок как условие термического равновесия в термодинамике Гиббса следует из экстремальных свойств внутренней энергии и энтропии в состоянии термодинамического равновесия.
Аксиоматика Фалька и Юнга[25] при определении энтропии не делает различия между равновесными и неравновесными состояниями, и, следовательно, даваемое в этой системе аксиом определение температуры через энтропию и внутреннюю энергию одинаково применимо для любых термически однородных систем:
| (Термодинамическая температура по Фальку и Юнгу) |
где — набор (в который не входит внутренняя энергия) независимых переменных энтропии.
Принцип локального равновесия разрешает для неравновесных систем заимствовать определение температуры из равновесной термодинамики и использовать данную переменную в качестве неравновесной температуры элементарного объёма среды[26].
В расширенной неравновесной термодинамике (РНТ), базирующейся на отказе от принципа локального равновесия, неравновесную температуру задают посредством соотношения, аналогичного используется в аксиоматике Фалька и Юнга (см. Термодинамическая температура по Фальку и Юнгу), но с другим набором независимых переменных для энтропии[27]. Локально-равновесная термодинамическая температура по Гиббсу также отличается от РНТ-неравновесной температуры выбором независимых переменных для энтропии[27].
В аксиоматике Н. И. Белоконя[28]. исходное определение температуры вытекает из постулата Белоконя, носящего название — постулат второго начала термостатики. Температура есть единственная функция состояния тел, определяющая направление самопроизвольного теплообмена между этими телами, то есть тела, находящиеся в тепловом равновесии, имеют одинаковую температуру в любой температурной шкале. Отсюда следует, что два тела, не имеющие теплового контакта между собой, но каждое из которых находится в тепловом равновесии с третьим (измерительный прибор), имеют одинаковую температуру.
Эмпирическая, абсолютная и термодинамическая температуры
Температура не может быть измерена непосредственно. Об изменении температуры судят по изменению других физических свойств тел (объёма, давления, электрического сопротивления, ЭДС, интенсивности излучения и др.), однозначно с ней связанных (так называемых термометрических свойств). Количественно же температура определяется указанием способа её измерения с помощью того или иного термометра. Такое определение ещё не фиксирует ни начало отсчёта, ни единицу измерения температуры, поэтому любой метод измерения температуры связан с выбором температурной шкалы. Эмпирическая температура — это температура, измеренная в выбранной температурной шкале.
Даваемые феноменологической термодинамикой определения термодинамической температуры не зависят от выбора термометрического свойства, использованного для её измерения; единицу измерения температуры задают с помощью одной из термодинамических температурных шкал.
В термодинамике в качестве аксиомы принимается основанное на опыте положение о том, что равновесная термодинамическая температура есть величина, для всех систем ограниченная с одной стороны, причём температура, соответствующая этой границе, одинакова для всех термодинамических систем и, следовательно, может быть использована в качестве естественной реперной точки шкалы температур. Если этой реперной точке присвоить равное нулю значение температуры, то температуры в шкале, базирующейся на данном репере, всегда будут иметь один и тот же знак[29]. Приписывая второй реперной точке положительное значение температуры, получают абсолютную температурную шкалу с положительными температурами; температуру, отсчитываемую от абсолютного нуля, называют абсолютной температурой[30]. Соответственно термодинамическую температуру, отсчитываемую от абсолютного нуля, называют абсолютной термодинамической температурой (см. Шкала температур Кельвина). Примером эмпирической температурной шкалы с отсчётом температуры от абсолютного нуля служит международная практическая температурная шкала.
Температурная шкала Цельсия не является абсолютной.
Некоторые авторы под абсолютностью температуры подразумевают не её отсчёт от абсолютного нуля, а независимость температуры от выбора термометрического свойства, используемого для её измерения[31][32].
Отрицательные абсолютные температуры
Равновесная термодинамическая абсолютная температура всегда положительна (см. Эмпирическая, абсолютная и термодинамическая температуры). Использование отрицательных (по шкале Кельвина) температур есть удобный математический приём описания неравновесных систем с особыми свойствами[33]. Приём этот состоит в мысленном выделении в самостоятельную подсистему объектов с особыми свойствами, входящих в состав физической системы, и сепаратном рассмотрении полученной парциальной подсистемы. Иными словами, один и тот же объём пространства рассматривается как одновременно занимаемый двумя и более парциальными подсистемами, слабо взаимодействующими друг с другом.
Примером использования данного подхода может служить рассмотрение ядерных спинов находящегося в магнитном поле кристалла как системы, слабо зависящей от тепловых колебаний кристаллической решётки. При быстром изменении направления магнитного поля на обратное, когда спины не успевают следовать за изменяющимся полем, система ядерных спинов некоторое время будет иметь отрицательную неравновесную температуру[34], то есть с формальной точки зрения в это время в одной и той же пространственной области будут находиться две слабо взаимодействующие системы с разными температурами[35]. В силу всё-таки имеющего место взаимодействия температуры обеих систем спустя какое-то время сравняются.
Формализм классической феноменологической термодинамики может быть дополнен представлениями об отрицательных абсолютных температурах[36][35]. В соответствии с постулатом Тиссы внутренняя энергия любой системы ограничена снизу, и эта граница соответствует абсолютному нулю температуры[37]. В системах, у которых имеется не только нижняя, но и верхняя граница внутренней энергии, с ростом температуры внутренняя энергия увеличивается и достигает своего предельного значения; дальнейшее повышение температуры ведёт уже не к увеличению внутренней энергии, а к уменьшению энтропии системы ( при )[35]. В соответствии с формулами термодинамики это соответствует переходу из области положительных температур через точку с температурой (точки с температурами и физически тождественны[38]) в сторону точки с недостижимым предельным значением температуры, равным [39][35].
Молекулярно-кинетическое определение
В молекулярно-кинетической теории (МКТ) температура определяется как величина, характеризующая приходящуюся на одну степень свободы среднюю кинетическую энергию частиц макроскопической системы, находящейся в состоянии термодинамического равновесия.
... мерилом температуры является не само движение, а хаотичность этого движения. Хаотичность состояния тела определяет его температурное состояние, и эта идея (которая впервые была разработана Больцманом), что определённое температурное состояние тела вовсе не определяется энергией движения, но хаотичностью этого движения, и является тем новым понятием в описании температурных явлений, которым мы должны пользоваться…П. Л. Капица[40]
Для одноатомного идеального газа температура может быть записана как
- ,
где — масса молекулы, = 1,38⋅10−23 Дж/К — постоянная Больцмана, — скорость молекулы. Этой записью высвечивается физический смысл температуры в рамках МКТ, но универсальной она не является, ибо далеко не все системы сводятся к модели идеального газа.
Определение температуры в статистической физике
В статистической физике, как и в термодинамическом подходе, температура определяется производной от энергии системы по её энтропии:
(если объём и число частиц в системе неизменны, частная производная заменяется полной). В рамках статистической физики существует конкретное выражение для энтропии, позволяющее выполнять вычисления:
- ,
где — статистический вес состояния — количество возможных микросостояний (способов), с помощью которых можно составить макроскопическое состояние с данной энергией (в этом контексте иногда обозначаемой буквой ).
Введённая таким образом величина является одинаковой для разных тел при термодинамическом равновесии. При контакте двух тел тело с бо́льшим значением будет отдавать энергию другому.
Измерение температуры

Для измерения термодинамической температуры выбирается некоторый термодинамический параметр термометрического вещества. Изменение этого параметра однозначно связывается с изменением температуры. Классическим примером термодинамического термометра может служить газовый термометр, в котором температуру определяют методом измерения давления газа в баллоне постоянного объёма. Известны также термометры абсолютные радиационные, шумовые, акустические.
Термодинамические термометры — это очень сложные установки, которые невозможно использовать для практических целей. Поэтому большинство измерений производится с помощью практических термометров, которые являются вторичными, так как не могут непосредственно связывать какое-то свойство вещества с температурой. Для получения функции интерполяции они должны быть отградуированы в реперных точках международной температурной шкалы.
Для измерения температуры какого-либо тела обычно измеряют какой-либо физический параметр, связанный с температурой, например, геометрические размеры (см. Дилатометр) для газов — объём или давление, скорость звука, электрическую проводимость, электромагнитные спектры поглощения или излучения (например, пирометры и измерение температуры фотосфер и атмосфер звёзд — в последнем случае по доплеровскому уширению спектральных линий поглощения или излучения).
В повседневной практике температуру обычно измеряют с помощью специальных приборов — контактных термометров. При этом термометр приводят в тепловой контакт с исследуемым телом, и, после установления термодинамического равновесия тела и термометра, — выравнивания их температур, по изменениям некоторого измеримого физического параметра термометра судят о температуре тела. Тепловой контакт между термометром и телом должен быть достаточным, чтобы выравнивание температур происходило быстрее, также, ускорение выравнивания температур достигается снижением теплоёмкости термометра по сравнению с исследуемым телом, обычно, уменьшением размеров термометра. Снижение теплоёмкости термометра также меньше искажает результаты измерения, так как меньшая часть теплоты исследуемого тела отбирается или передаётся термометру. Идеальный термометр имеет нулевую теплоёмкость[41].
Средства измерения температуры часто проградуированы по относительным шкалам — Цельсия или Фаренгейта.
На практике для измерения температуры также используют
Самым точным практическим термометром является платиновый термометр сопротивления[42]. Разработаны новейшие методы измерения температуры, основанные на измерении параметров лазерного излучения[43].
Единицы и шкала измерения температуры
Поскольку температура — это мера средней кинетической энергии теплового движения частиц системы[44], наиболее естественно было бы измерять её в энергетических единицах (то есть в системе СИ в джоулях; см. также эВ). Исходя из соотношения температуры и энергии частиц в одноатомном идеальном газе Eкин = 3⁄2kТ[45]. В температурных единицах 1 эВ соответствует 11 604,518 12 К[46] (см. постоянная Больцмана)[47].
Однако измерение температуры началось задолго до создания молекулярно-кинетической теории, поэтому все практические шкалы измеряют температуру в условных единицах — градусах.
Абсолютная температура. Шкала температур Кельвина
Понятие абсолютной температуры было введено У. Томсоном (Кельвином), в связи с чем шкалу абсолютной температуры называют шкалой Кельвина или термодинамической температурной шкалой. Единица абсолютной температуры — кельвин (К).
Абсолютная шкала температуры называется так, потому что мера основного состояния нижнего предела температуры — абсолютный ноль, то есть наиболее низкая возможная температура, при которой в принципе невозможно извлечь из вещества тепловую энергию.
Абсолютный ноль определён как 0 K, что равно −273,15 °C и −459,67 °F.
Шкала температур Кельвина — это шкала, в которой начало отсчёта ведётся от абсолютного нуля.
Важное значение имеет разработка на основе термодинамической шкалы Кельвина Международных практических шкал, основанных на реперных точках — фазовых переходах чистых веществ, определенных методами первичной термометрии. Первой международной температурной шкалой являлась принятая в 1927 г. МТШ-27. С 1927 г. шкала несколько раз переопределялась (МТШ-48, МПТШ-68, МТШ-90): менялись реперные температуры, методы интерполяции, но принцип остался тот же — основой шкалы является набор фазовых переходов чистых веществ с определенными значениями термодинамических температур и интерполяционные приборы, градуированные в этих точках. В настоящее время действует шкала МТШ-90. Основной документ (Положение о шкале) устанавливает определение Кельвина, значения температур фазовых переходов (реперных точек)[48] и методы интерполяции.
Используемые в быту температурные шкалы — как Цельсия, так и Фаренгейта (используемая, в основном, в США), — не являются абсолютными и поэтому неудобны при проведении экспериментов в условиях, когда температура опускается ниже точки замерзания воды, из-за чего температуру приходится выражать отрицательным числом. Для таких случаев были введены абсолютные шкалы температур.
Одна из них называется шкалой Ранкина, а другая — абсолютной термодинамической шкалой (шкалой Кельвина); температуры по ним измеряются, соответственно, в градусах Ранкина (°Ra) и кельвинах (К). Обе шкалы начинаются при температуре абсолютного нуля. Различаются они тем, что цена одного деления по шкале Кельвина равна цене деления шкалы Цельсия, а цена деления шкалы Ранкина эквивалентна цене деления термометров со шкалой Фаренгейта. Температуре замерзания воды при стандартном атмосферном давлении соответствуют 273,15 K, 0 °C, 32 °F.
Масштаб шкалы Кельвина был привязан к тройной точке воды (273,16 К), при этом от неё зависела постоянная Больцмана. Это создавало проблемы с точностью интерпретации измерений высоких температур. Поэтому в 2018—2019 годах в рамках изменений в СИ было введено новое определение кельвина, основанное на фиксации численного значения постоянной Больцмана, вместо привязки к температуре тройной точки[49].
Шкала Цельсия
В технике, медицине, метеорологии и в быту в качестве единицы измерения температуры используется шкала Цельсия. В настоящее время в системе СИ термодинамическую шкалу Цельсия определяют через шкалу Кельвина[4]: t(°С) = Т(К) — 273,15 (точно), то есть цена одного деления в шкале Цельсия равна цене деления шкалы Кельвина. По шкале Цельсия температура тройной точки воды равна приблизительно 0,008 °C,[50] и, следовательно, точка замерзания воды при давлении в 1 атм очень близка к 0 °C. Точка кипения воды, изначально выбранная Цельсием в качестве второй реперной точки со значением, по определению равным 100 °C, утратила свой статус одного из реперов. По современным оценкам, температура кипения воды при нормальном атмосферном давлении в термодинамической шкале Цельсия составляет около 99,975 °C. Шкала Цельсия очень удобна с практической точки зрения, поскольку вода и её состояния распространены и крайне важны для жизни на Земле. Ноль по этой шкале является особой точкой для метеорологии, поскольку связан с замерзанием атмосферной воды. Шкала предложена Андерсом Цельсием в 1742 г.
Шкала Фаренгейта
В Англии и, в особенности, в США используется шкала Фаренгейта. Ноль градусов Цельсия — это 32 градуса Фаренгейта, а 100 градусов Цельсия — 212 градусов Фаренгейта.
В настоящее время принято следующее определение шкалы Фаренгейта: это температурная шкала, 1 градус которой (1 °F) равен 1/180 разности температур кипения воды и таяния льда при атмосферном давлении, а точка таяния льда имеет температуру +32 °F. Температура по шкале Фаренгейта связана с температурой по шкале Цельсия (t °С) соотношением t °С = 5/9 (t °F — 32), t °F = 9/5 t °С + 32. Предложена Г. Фаренгейтом в 1724 году.
Шкала Реомюра
Предложена в 1730 году Р. А. Реомюром, который описал изобретённый им спиртовой термометр.
Единица — градус Реомюра (°Ré), 1 °Ré равен 1/80 части температурного интервала между опорными точками — температурой таяния льда (0 °Ré) и кипения воды (80 °Ré)
1 °Ré = 1,25 °C.
В настоящее время шкала вышла из употребления, дольше всего она сохранялась во Франции, на родине автора.
Энергия теплового движения при абсолютном нуле
Когда материя охлаждается, многие формы тепловой энергии и связанные с ней эффекты одновременно уменьшаются по величине. Вещество переходит от менее упорядоченного состояния к более упорядоченному.
… современное понятие абсолютного нуля не есть понятие абсолютного покоя, наоборот, при абсолютном нуле может быть движение — и оно есть, но это есть состояние полного порядка …П. Л. Капица[40]
Газ превращается в жидкость и затем кристаллизуется в твёрдое тело (гелий и при абсолютном нуле остаётся в жидком состоянии при атмосферном давлении). Движение атомов и молекул замедляется, их кинетическая энергия уменьшается. Сопротивление большинства металлов падает из-за уменьшения рассеяния электронов на колеблющихся с меньшей амплитудой атомах кристаллической решётки. Таким образом даже при абсолютном нуле электроны проводимости движутся между атомами со скоростью Ферми порядка 106 м/с.
Температура, при которой частицы вещества имеют минимальное количество движения, сохраняющееся только благодаря квантовомеханическому движению — это температура абсолютного нуля (Т = 0К).
Температуры абсолютного нуля достичь невозможно. Наиболее низкая температура (450±80)⋅10−12К конденсата Бозе-Эйнштейна атомов натрия была получена в 2003 г. исследователями из МТИ[51]. При этом пик теплового излучения находится в области длин волн порядка 6400 км, то есть примерно радиуса Земли.
Температура и излучение
Излучаемая телом энергия пропорциональна четвёртой степени его температуры. Так, при 300 К с квадратного метра поверхности излучается до 450 ватт. Этим объясняется, например, ночное охлаждение земной поверхности ниже температуры окружающего воздуха. Энергия излучения абсолютно чёрного тела описывается законом Стефана — Больцмана
Переходы из разных шкал
| Шкала | Условное обозначение | из Цельсия (°C) | в Цельсий |
|---|---|---|---|
| Фаренгейт | (°F) | [°F] = [°C] × 9⁄5 + 32 | [°C] = ([°F] − 32) × 5⁄9 |
| Кельвин | (K) | [K] = [°C] + 273,15 | [°C] = [K] − 273,15 |
| Ранкин (Rankin) | (°R) | [°R] = ([°C] + 273,15) × 9⁄5 | [°C] = ([°R] − 491,67) × 5⁄9 |
| Делиль (Delisle) | (°Д или °De) | [°De] = (100 − [°C]) × 3⁄2 | [°C] = 100 − [°De] × 2⁄3 |
| Ньютон (Newton) | (°N) | [°N] = [°C] × 33⁄100 | [°C] = [°N] × 100⁄33 |
| Реомюр (Réaumur) | (°Re, °Ré, °R) | [°Ré] = [°C] × 4⁄5 | [°C] = [°Ré] × 5⁄4 |
| Рёмер (Rømer) | (°Rø) | [°Rø] = [°C] × 21⁄40 + 7,5 | [°C] = ([°Rø] − 7,5) × 40⁄21 |
Сравнение температурных шкал
| Описание | Кельвин | Цельсий | Фаренгейт | Ранкин | Делиль | Ньютон | Реомюр | Рёмер |
|---|---|---|---|---|---|---|---|---|
| Абсолютный нуль | 0 | −273,15 | −459,67 | 0 | 559,725 | −90,14 | −218,52 | −135,90 |
| Температура таяния смеси Фаренгейта (соль, лёд и хлорид аммония)[52] | 255,37 | −17,78 | 0 | 459,67 | 176,67 | −5,87 | −14,22 | −1,83 |
| Температура замерзания воды (Нормальные условия) | 273,15 | 0 | 32 | 491,67 | 150 | 0 | 0 | 7,5 |
| Средняя температура человеческого тела¹ | 309,75 | 36,6 | 98,2 | 557,9 | 94,5 | 12,21 | 29,6 | 26,925 |
| Температура кипения воды (Нормальные условия) | 373,15 | 100 | 212 | 671,67 | 0 | 33 | 80 | 60 |
| Плавление титана | 1941 | 1668 | 3034 | 3494 | −2352 | 550 | 1334 | 883 |
| Солнце² | 5800 | 5526 | 9980 | 10440 | −8140 | 1823 | 4421 | 2909 |
¹ Нормальная средняя температура человеческого тела — +36,6 °C ±0,7 °C, или +98,2 °F ±1,3 °F. Приводимое обычно значение +98,6 °F — это точное преобразование в шкалу Фаренгейта принятого в Германии в XIX веке значения +37 °C. Однако это значение не входит в диапазон нормальной средней температуры тела человека, поскольку температура разных частей тела разная[53].
² Некоторые значения в этой таблице являются округлёнными. Например, температура поверхности Солнца равняется 5800 кельвинам очень приближённо. Однако для остальных температурных шкал уже дан точный результат перевода 5800 кельвинов в данную шкалу.
Характеристика фазовых переходов
Для описания точек фазовых переходов различных веществ используют следующие значения температуры:
- Температура плавления
- Температура кипения
- Тройная точка
- Температура Дебая (Характеристическая температура)
- Температура Кюри
- Температура Нееля
Психология восприятия
Как показывают результаты многочисленных экспериментов, ощущение холода или тепла зависит не только от температуры и влажности окружающей среды, но и от настроения. Так, если испытуемый чувствует себя одиноким, например, находится в помещении с людьми, которые не разделяют его взглядов или ценностей, или просто находится далеко от других людей, то для него комната становится холоднее, и наоборот[54].
Интересные факты
- Самая высокая температура, созданная человеком, ~ 10⋅1012 К (что сравнимо с температурой Вселенной в первые секунды её жизни) была достигнута в 2010 году при столкновении ионов свинца, ускоренных до околосветовых скоростей. Эксперимент был проведён на Большом адронном коллайдере[55].
- Самая высокая теоретически возможная температура — планковская температура. Более высокая температура по современным физическим представлениям не может существовать, так как придание дополнительной энергии системе, нагретой до такой температуры, не увеличивает скорости частиц, а только порождает в столкновениях новые частицы, при этом число частиц в системе растёт, а также растёт и масса системы. Можно считать, что это температура «кипения» физического вакуума. Она примерно равна 1,41679(11)⋅1032 K (примерно 142 нониллиона K).
- Солнечное ядро имеет температуру около 15 000 000 K.
- При очень низкой температуре, полученной в 1995 году Эриком Корнеллом и Карлом Виманом из США при охлаждении атомов рубидия удалось получить конденсат Бозе-Эйнштейна[56][57]. Температура была выше абсолютного нуля на 170 миллиардных долей кельвина (1,7⋅10−7 K).
- Самой низкой температурой, полученной в эксперименте, является температура в 50 пикокельвинов (5⋅10−11 K), полученная группой из Стенфордского университета в 2015 году[58].
- Рекордно низкая температура на поверхности Земли −89,2 °С была зарегистрирована на советской внутриконтинентальной научной станции Восток, Антарктида (высота 3488 м над уровнем моря) 21 июля 1983 года[59][60]. В июне 2018 года появилась информация о температуре −98 °С, зарегистрированной в Антарктиде[61].
- 9 декабря 2013 года на конференции Американского геофизического союза группа американских исследователей сообщила о том, что 10 августа 2010 года температура воздуха в одной из точек Антарктиды опускалась до −135,8 °F (−93,2 °С). Данная информация была выявлена в результате анализа спутниковых данных НАСА[62]. По мнению выступавшего с сообщением Т. Скамбоса (англ. Ted Scambos) полученное значение не будет зарегистрировано в качестве рекордного, поскольку определено в результате спутниковых измерений, а не с помощью термометра[63].
- Рекордно высокая температура воздуха вблизи поверхности земли +56,7 ˚C была зарегистрирована 10 июля 1913 года на ранчо Гринленд в долине Смерти (штат Калифорния, США)[64][65].
- Семена высших растений сохраняют всхожесть после охлаждения до −269 °C[66].
См. также
Примечания
- ↑ В качестве реперной точки 10-я Генеральная конференция по мерам и весам в 1954 году приняла тройную точку воды, приписав ей точное значение температуры 273,16 К по определению.
- ↑ Физика. Большой энциклопедический словарь / Гл. ред. А. М. Прохоров. — М.: Большая Российская энциклопедия, 1998. — С. 741. — 944 с.
- ↑ The SI brochure Архивная копия от 26 апреля 2006 на Wayback Machine Описание СИ на сайте Международного бюро мер и весов
- ↑ 1 2 ГОСТ 8.417-2002. Государственная система обеспечения единства измерений. Единицы величин. Дата обращения: 3 декабря 2018. Архивировано 20 сентября 2018 года.
- ↑ Жилин П. А., Рациональная механика сплошных сред, 2012, с. 84.
- ↑ Температурное поле. БСЭ, 3-е изд., 1976, т. 25. Дата обращения: 27 марта 2015. Архивировано 2 апреля 2015 года.
- ↑ Татьяна Данина. Механика тел. — Litres, 2017-09-05. — 163 с. — ISBN 9785457547490. Архивировано 26 апреля 2018 года.
- ↑ Трусделл К., Термодинамика для начинающих, 1970, с. 117.
- ↑ Жилин П. А., Рациональная механика сплошных сред, 2012, с. 48.
- ↑ Физика. Большой энциклопедический словарь, 1998, с. 751.
- ↑ Залевски К., Феноменологическая и статистическая термодинамика, 1973, с. 11–12.
- ↑ Вукалович М. П., Новиков И. И., Термодинамика, 1972, с. 11.
- ↑ Зоммерфельд А., Термодинамика и статистическая физика, 1955, с. 11.
- ↑ Клаузиус Р., Механическая теория тепла, 1934.
- ↑ Каратеодори К., Об основах термодинамики, 1964.
- ↑ Борн М., Критические замечания по поводу традиционного изложения термодинамики, 1964.
- ↑ Базаров И. П., Термодинамика, 2010, с. 57.
- ↑ Гухман А. А., Об основаниях термодинамики, 1986.
- ↑ Леонова В. Ф., Термодинамика, 1968.
- ↑ Базаров И. П., Термодинамика, 2010, с. 29, 58, 127, 171.
- ↑ Кубо Р., Термодинамика, 1970, с. 20–21.
- ↑ Гиббс Дж. В., Термодинамика. Статистическая механика, 1982, с. 93.
- ↑ Guggenheim E. A., Thermodynamics, 1986, p. 15.
- ↑ Callen H. B., Thermodynamics and an Introduction to Thermostatistics, 1986, p. 35.
- ↑ Falk G., Jung H., Axiomatik der Thermodynamik, 1959, p. 156.
- ↑ Дьярмати И., Неравновесная термодинамика, 1974, с. 26.
- ↑ 1 2 Jou D. e. a., Extended Irreversible Thermodynamics, 2010, p. 48.
- ↑ Белоконь Н. И., Основные принципы термодинамики, 1968, с. 10.
- ↑ Базаров И. П., Термодинамика, 2010, с. 62.
- ↑ Абсолютная температура. БСЭ, 3-е изд., 1969, т. 1. Дата обращения: 27 марта 2015. Архивировано 21 февраля 2015 года.
- ↑ Пригожин И., Кондепуди Д., Современная термодинамика, 2002, с. 23, 83, 86.
- ↑ Сорокин В. С., Макроскопическая необратимость и энтропия. Введение в термодинамику, 2004, с. 60.
- ↑ Отрицательная температура. БСЭ, 3-е изд., 1975, т. 19. Дата обращения: 27 марта 2015. Архивировано 2 апреля 2015 года.
- ↑ Ландау Л. Д., Лифшиц Е. М., Статистическая физика. Часть 1, 2002, с. 262.
- ↑ 1 2 3 4 Поулз Д., Отрицательные абсолютные температуры, 1964.
- ↑ Базаров И. П., Термодинамика, 2010, с. 136–148.
- ↑ Tisza L., Generalized Thermodynamics, 1966, p. 125.
- ↑ Ландау Л. Д., Лифшиц Е. М., Статистическая физика. Часть 1, 2002, с. 261.
- ↑ Базаров И. П., Термодинамика, 2010, с. 137–138.
- ↑ 1 2 Капица П. Л. Свойства жидкого гелия // Природа. — Наука, 1997. — № 12. Архивировано 21 февраля 2016 года.
- ↑ Шахмаев Н. М. и др. Физика: Учебник для 10 класса общеобразовательных учреждений. — М.: Просвещение, 1996. — С. 21. — 240 с. — ISBN 5090067937.
- ↑ Платиновый термометр сопротивления — основной прибор МТШ-90. Дата обращения: 5 мая 2010. Архивировано 8 июня 2010 года.
- ↑ Лазерная термометрия. Дата обращения: 5 мая 2010. Архивировано 8 июня 2010 года.
- ↑ Температура // Большая российская энциклопедия : [в 35 т.] / гл. ред. Ю. С. Осипов. — М. : Большая российская энциклопедия, 2004—2017.
- ↑ Электронвольт // Физическая энциклопедия / Гл. ред. А. М. Прохоров. — М.: Большая Российская энциклопедия, 1998. — Т. 5. Стробоскопические приборы — Яркость. — С. 545. — 760 с. — ISBN 5-85270-101-7.
- ↑ http://physics.nist.gov/cuu/Constants/Table/allascii.txt Архивная копия от 8 декабря 2013 на Wayback Machine Fundamental Physical Constants — Complete Listing
- ↑ Conversion factors for energy equivalents. Дата обращения: 17 февраля 2021. Архивировано 26 января 2021 года.
- ↑ Реперные точки МТШ-90. Дата обращения: 5 мая 2010. Архивировано 17 сентября 2011 года.
- ↑ Разработка нового определения кельвина. Дата обращения: 5 мая 2010. Архивировано 8 июня 2010 года.
- ↑ Д. А. Паршин, Г. Г. Зегря. Критическая точка. Свойства вещества в критическом состоянии. Тройная точка. Фазовые переходы II рода. Методы получения низких температур. Статистическая термодинамика. Лекция 11. Санкт-Петербургский академический университет. Дата обращения: 2 июня 2011. Архивировано из оригинала 3 декабря 2012 года.
- ↑ Belle Dumé. Bose-Einstein condensates break temperature record (англ.). Physics World (12 сентября 2003). Дата обращения: 24 июля 2013. Архивировано 25 июля 2013 года.
- ↑ Фаренгейта шкала : [арх. 15 июня 2022] // Большая российская энциклопедия : [в 35 т.] / гл. ред. Ю. С. Осипов. — М. : Большая российская энциклопедия, 2004—2017.
- ↑ О различных измерениях температуры тела Архивная копия от 26 сентября 2010 на Wayback Machine (англ.)
- ↑ Тальма Лобель, 2014, с. 24.
- ↑ BBC News — Large Hadron Collider (LHC) generates a 'mini-Big Bang'. Дата обращения: 15 ноября 2010. Архивировано 15 ноября 2010 года.
- ↑ Всё про всё. Рекорды температуры. Дата обращения: 16 декабря 2009. Архивировано 25 сентября 2013 года.
- ↑ Чудеса науки. Дата обращения: 16 декабря 2009. Архивировано из оригинала 1 декабря 2012 года.
- ↑ Where is the coldest experiment on Earth? (англ.). Дата обращения: 23 февраля 2020. Архивировано 23 февраля 2020 года.
- ↑ Самая низкая температура на поверхности Земли. National Geographic Россия. Дата обращения: 9 декабря 2013. Архивировано из оригинала 13 декабря 2013 года.
- ↑ World: Lowest Temperature (англ.). Arizona State University. Дата обращения: 9 декабря 2013. Архивировано из оригинала 16 июня 2010 года.
- ↑ Учёные зафиксировали в Антарктиде самую низкую температуру на планете. Дата обращения: 27 июня 2018. Архивировано 27 июня 2018 года.
- ↑ NASA-USGS Landsat 8 Satellite Pinpoints Coldest Spots on Earth (англ.). NASA. Дата обращения: 10 декабря 2013. Архивировано 12 декабря 2013 года.
- ↑ Antarctica sets low temperature record of -135.8 degrees (англ.). FoxNews. Дата обращения: 10 декабря 2013. Архивировано 11 декабря 2013 года.
- ↑ Старый температурный рекорд оспорен. Компьюлента. Дата обращения: 30 ноября 2013. Архивировано из оригинала 3 декабря 2013 года.
- ↑ Press Release No. 956 (англ.). World Meteorological Organizayion. Дата обращения: 30 ноября 2013. Архивировано из оригинала 6 апреля 2016 года.
- ↑ Imshenetsky A. A. Biological effects of extreme environment conditions // Foundations of Space Biology and Medicine (англ.). — Washington, D. C.: Scientific and Technical Information Office, National Aeronautics and Space Administration, 1975. — Vol. 1. Space as a habitat. — P. 277. Архивировано 12 августа 2024 года.
Литература
- Callen H. B. Thermodynamics and an Introduction to Thermostatistics (англ.). — 2nd ed. — N. Y. e. a.: John Wiley, 1986. — XVI + 493 p. — ISBN 0471862568, 9780471862567.
- Falk G., Jung H. Axiomatik der Thermodynamik (нем.) // Flügge S. (ed.). Encyclopedia of Physics / Flügge S. (Hrsg.). Handbuch der Physik. — Springer-Verlag, 1959. — Vol. III/2. Principles of Thermodynamics and Statistics / Band III/2. Prinzipien der Thermodynamik und Statistik, S. 119–175.
- Guggenheim E. A. Thermodynamics: An Advanced Treatment for Chemists and Physicists. — 8th ed. — Amsterdam: North-Holland, 1986. — XXIV + 390 p. — ISBN 0444869514, 9780444869517.
- Jou D., Casas-Vázquez J., Lebon G. Extended Irreversible Thermodynamics (англ.). — 4th ed. — N. Y.—Dordrecht—Heidelberg—London: Springer, 2010. — XVIII + 483 p. — ISBN 978-90-481-3073-3. — doi:10.1007/978-90-481-3074-0.
- Tisza Laszlo. Generalized Thermodynamics. — Cambridge (Massachusetts) — London (England): The M.I.T. Press, 1966. — XI + 384 p.
- Базаров И. П. Термодинамика. — 5-е изд. — СПб.—М.—Краснодар: Лань, 2010. — 384 с. — (Учебники для вузов. Специальная литература). — ISBN 978-5-8114-1003-3.
- Белоконь Н. И. Основные принципы термодинамики. — М.: Недра, 1968. — 112 с.
- Борн М. Критические замечания по поводу традиционного изложения термодинамики // Развитие современной физики. — М.: Наука, 1964. — С. 223—256.
- Вукалович М. П., Новиков И. И. Термодинамика. — М.: Машиностроение, 1972. — 671 с.
- Гиббс Дж. В. Термодинамика. Статистическая механика / Отв. ред. Д. Н. Зубарев. — М.: Наука, 1982. — 584 с. — (Классики науки).
- Гухман А. А. Об основаниях термодинамики. — Алма-Ата: Изд-во АН КазССР, 1947. — 106 с.
- Гухман А. А. Об основаниях термодинамики. — М.: Энергоатомиздат, 1986. — 384 с.
- Дьярмати И. Неравновесная термодинамика. Теория поля и вариационные принципы. — М.: Мир, 1974. — 304 с.
- Жилин П. А. Рациональная механика сплошных сред. — 2-е изд. — СПб.: Изд-во Политехн. ун-та, 2012. — 584 с. — ISBN 978-5-7422-3248-3.
- Залевски К. Феноменологическая и статистическая термодинамика: Краткий курс лекций / Пер. с польск. под. ред. Л. А. Серафимова. — М.: Мир, 1973. — 168 с.
- Зоммерфельд А. Термодинамика и статистическая физика / Пер. с нем.. — М.: Изд-во иностр. лит-ры, 1955. — 480 с.
- Каратеодори К. Об основах термодинамики // Развитие современной физики. — М.: Наука, 1964. — С. 3—22.
- Клаузиус Р. Механическая теория тепла // Второе начало термодинамики. — М.—Л.: Гостехиздат, 1934. — С. 70—158.
- Кубо Р. Термодинамика. — М.: Мир, 1970. — 304 с.
- Ландау Л. Д., Лифшиц Е. М. Статистическая физика. Часть 1. — 5-е изд. — М.: Физматлит, 2002. — 616 с. — (Теоретическая физика в 10 томах. Том 5). — ISBN 5-9221-0054-8.
- Леонова В. Ф. Термодинамика. — М.: Высшая школа, 1968. — 159 с.
- Поулз Д. Отрицательные абсолютные температуры и температуры во вращающихся системах координат // Успехи физических наук. — Российская академия наук, 1964. — Vol. 84, № 4. — С. 693—713.
- Пригожин И., Кондепуди Д. Современная термодинамика. От тепловых двигателей до диссипативных структур / Пер. с англ. — М.: Мир, 2002. — 462 с.
- Рудой Ю. Г. Математическая структура равновесной термодинамики и статистической механики. — М. — Ижевск: Институт компьютерных исследований, 2013. — 368 с. — ISBN 978-5-4344-0159-3.
- Сивухин Д. В. Термодинамика и молекулярная физика. — Москва: «Наука», 1990.
- Сорокин В. С. Макроскопическая необратимость и энтропия. Введение в термодинамику. — М.: ФИЗМАТЛИТ, 2004. — 174 с. — ISBN 5-9221-0507-8.
- Спасский Б. И. История физики Ч.I. — Москва: «Высшая школа», 1977.
- Тальма Лобель. Теплая чашка в холодный день: Как физические ощущения влияют на наши решения = Sensation The New Science of Physical Intelligence. — М.: Альпина Паблишер, 2014. — 259 с. — ISBN 978-5-9614-4698-2.
- Трусделл К. Термодинамика для начинающих // Механика. Периодический сборник переводов иностранных статей. — М.: Мир, 1970. — № 3 (121), с. 116—128.
- Физика. Большой энциклопедический словарь / Гл. ред. А. М. Прохоров. — М.: Большая Российская энциклопедия, 1998. — 944 с. — ISBN 5-85270-306-0.
Ссылки
- Current map of global surface temperatures (англ.)
- Miller, J. Cooling molecules the optoelectric way (англ.) // Physics Today : magazine. — 2013. — Vol. 66, no. 1. — P. 12—14. — doi:10.1063/pt.3.1840. — . Архивировано 15 мая 2016 года.













![{\displaystyle T\equiv \left[\left({\frac {\partial S}{\partial U}}\right)_{\{x_{i}\}}\right]^{-1},}](https://wikimedia.org/api/rest_v1/media/math/render/svg/3199aedd04aecf0811bc8ef796f064be37d4cbac)























