Теория молекулярных орбиталей
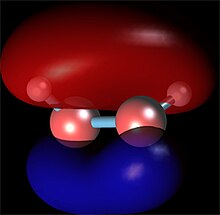
Теория молекулярных орбиталей (МО) даёт представление о распределении электронной плотности и объясняет свойства молекул.
Описание
В этой теории квантовомеханические зависимости для атома распространены на более сложную систему — молекулу. Молекула рассматривается как целое, а не как совокупность сохранивших индивидуальность атомов. В молекуле (как и в атоме) имеются дискретные энергетические состояния отдельных электронов (молекулярные орбитали) с их самосогласованным движением в поле друг друга и всех ядер молекулы.
Предполагается, что все электроны данной молекулы (как и в атоме) распределяются по соответствующим орбиталям. Состояние электрона в атоме описывается одноэлектронной волновой функцией ψ, являющейся решением уравнения Шрёдингера. Волновая функция ψ, зависящая от четырёх квантовых чисел, имеющая конкретный математический вид и удовлетворяющая условию нормировки и однозначности называется молекулярной орбиталью (МО) (по аналогии с атомной). Каждая орбиталь характеризуется своим набором квантовых чисел, отражающих свойства электронов в данном энергетическом состоянии. В отличие от одноцентровых орбиталей атомов, орбитали молекул многоцентровые, то есть молекулы имеют общие орбитали для двух или более атомных ядер. Каждая молекулярная орбиталь обладает определённой энергией, приближённо характеризующейся соответствующим потенциалом ионизации.
По аналогии с атомными s-, p-, d-, f- орбиталями молекулярные орбитали обозначают греческими буквами σ-, π-, δ-, φ-. МО образуются при комбинировании атомных орбиталей при достаточном сближении. Совокупность МО молекулы с указанием её типа и количеством электронов на ней даёт электронную конфигурацию молекулы. Существует 3 типа молекулярных орбиталей: связывающие, разрыхляющие и несвязывающие. Электроны на связывающих молекулярных орбиталях упрочняют связь, на разрыхляющих как бы дестабилизируют (расшатывают). Молекула является устойчивой лишь в том случае, если число электронов на связывающих орбиталях превышает число электронов на разрыхляющих. Электроны, находящиеся на несвязывающих молекулярных орбиталях, участия в образовании химической связи не принимают. Из n исходных атомных орбиталей возникает n МО. Так, при образовании двухатомной молекулы H2 из атомов водорода Н из их s-орбиталей возникают две двухцентровые МО — одна энергетически более выгодная (связывающая σsсв), другая менее выгодная (разрыхляющая σsразр), чем исходные атомные орбитали. На связывающей МО электрон большую часть времени пребывает между ядрами (повышается электронная плотность), способствуя их химическому связыванию. На разрыхляющей же МО электрон большую часть времени находится за ядрами, вызывая отталкивание ядер друг от друга.[1].
Характер распределения электронов по МО определяет порядок (кратность) связи, её энергию, межъядерные расстояния (длина связи), магнитные свойства молекул и др. Заполнение молекулярных орбиталей подчиняется тем же правилам, что и заполнение атомных: принципу энергетической выгодности, принципу Паули, правилу Хунда, правилу Клечковского. В общепринятом приближении молекулярная орбиталь рассматривается как линейная комбинация атомных орбиталей (приближение МО ЛКАО).
Кратность связи в теории молекулярных орбиталей определяется выражением
где и — суммарные количества электронов на связывающих и разрыхляющих орбиталях соответственно.[1]
Примеры
Рассмотрим применение метода к двухатомной молекуле водорода H2. У отдельного атома водорода есть 1s орбиталь с одним электроном, имеющим энергию Е. В молекуле из двух атомов водородов орбитали отдельных атомов преобразуются в две: связывающую и разрыхляющую. При этом связывающая находится по энергии ниже 1s орбитали водорода на величину ΔE, разрыхляющая выше 1s орбитали на ΔE. Тогда энергия электрона связывающей орбитали будет равна E — ΔE, а разрыхляющей E + ΔE. Сумма энергии этих двух орбиталей (E — ΔE) + (E + ΔE) = 2E, будет равна сумме энергии двух 1s орбиталей двух отдельных атомов водорода. То есть закон сохранения энергии выполняется (что и должно быть).
Другим примером применения метода молекулярных орбиталей может служить рассмотрение молекулы кислорода . Молекула кислорода состоит из двух атомов кислорода, конфигурация основного состояния 2s2 2p4.
s-орбитали образуют две молекулярные орбитали — их сумма преобразуется по полносимметричному представлению в данной группе симметрии (группа D∞h, представление Σg+, её энергия), разность — по представлению Σu+.
p-орбитали образуют шесть молекулярных орбиталей. Две из них преобразуются по представлениям типа Σ+ (разрыхляющая нечётная, связывающая чётная. Обе образованы p-орбиталями с нулевой проекцией орбитального момента). Четыре из них — по двумерным представлениям типа П (здесь наоборот, связывающие орбитали нечётные относительно инверсии).
В итоге получаем такую конфигурацию молекулы — (σ)2 (σ*)2 (σ)2 (π)4 (π*)2, которая порождает основной терм 3Σg- — то есть основное состояние этой молекулы — триплетное, что и подтверждается многочисленными экспериментами (например, кислород парамагнитен). Согласно ММО, кратность связи в молекуле кислорода равна , то есть связь двойная.
Преимущества
По сравнению с методом валентных схем имеет следующие преимущества:
- Позволяет описывать химическую связь в электронодефицитных молекулах (диборан), молекулярных радикалах (монооксид азота), молекулярных ионах (нитрозил, нитроил, гидразоний, оксигенил), гипервалентных соединениях (соединения благородных газов).
- Объясняет образование молекул с многоцентровыми орбиталями. Например, в азотной кислоте азот имеет степень окисления +5, хотя предельное число связей не может быть больше числа валентных орбиталей (то есть 4). Это противоречие разрешается исходя из модели трёхцентровой двухэлектронной связи.
- Описывает водородную связь как частный случай ковалентной: через модель делокализации электронной плотности и образование трёхцентровых четырёхэлектронных связей (например, -H•••[F-H•••F]-).
Когда обнаружилась способность благородных газов образовывать соединения, некоторые учёные были склонны считать, что электроны распариваются на следующий энергетический уровень и образуются нормальные двухцентровые двухэлектронные связи. Однако энергия на распаривание слишком велика, и она не покрылась бы энергией, выделившейся в результате образования химических связей. Оказывается, образуются трёхцентровые четырёхэлектронные связи. Модель МО ЛКАО позволяет объяснить образование химической связи в такого рода соединениях.
Энергию МО в молекуле либо определяют экспериментально (спектроскопически и др.), либо рассчитывают методами квантовой механики и квантовой химии (чисто теоретическими и полуэмпирическими).
См. также
Примечания
Литература
- Фудзинага С. Метод молекулярных орбиталей. М.: Мир, 1983. 462 с.
- Дьюар М. Теория молекулярных орбиталей в органической химии. М.: Мир, 1972. 592 с.
- Дяткина М. Е. Основы теории молекулярных орбиталей. М.: Наука, 1975. 190 с.
- Волков А. И. Метод молекулярных орбиталей М.: Новое знание, 2006. 136 с. ISBN 5-94735-107-2
- Дьюар М., Догерти Р. Теория возмущений молекулярных орбиталей в органической химии. М.: Мир, 1970. 695 c.
- Базилевский М. В. Метод молекулярных орбит и реакционная способность органических молекул. М.: Химия, 1969. 304 с.
- Орчин М., Джаффе Г. Разрыхляющие орбитали. М.: Мир, 1969. 112 с.
- Приседский В. В. Молекулярные орбитали (Учебное пособие к изучению блока «Химическая связь» в курсах химии для студентов химических специальностей). — Донецк: ДонНТУ, 2009. — 42 с. Архивная копия от 19 сентября 2013 на Wayback Machine
- Java molecular orbital viewer shows orbitals of hydrogen molecular ion.
- The orbitron, a visualization of all atomic, and some molecular and hybrid orbitals
- xeo Visualizations of some atomic and molecular atoms
- Simulations of molecules with electrons caught in molecular orbital (Simulations run on PC only.)
- OrbiMol Molecular orbital database.












