Тетерин (белок)
Те́терин, или костномозговой стромальный клеточный антиген 2, (англ. Tetherin; bone marrow stromal cell antigen 2; HM1.24; CD317) — мембранный белок, фактор рестрикции (ингибитор) вирусных инфекций, включая ВИЧ[1][2]. Продукт гена человека BST2.
Структура
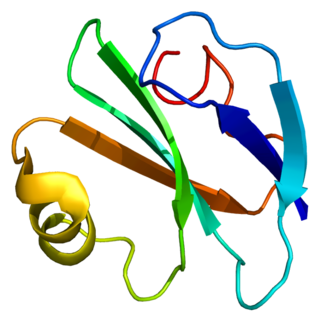
Существует как димерный белок, мономеры соединены друг с другом дисульфидными связями. Мутации белка по цистеинам, образующим межмолекулярную связь, приводят к функциональной инактивации белка[3].
Зрелый мономер (образующийся после отщепления C-концевого пептида длиной 19 аминокислот) состоит из 161 аминокислоты; молекулярная масса — 30-36 кДа. Относится ко второму типу интегральных мембранных белков, с топологией, позволяющей заякоривание обоих концов молекулы в липидных бислоях. Содержит N-концевой цитоплазматический домен, трансмембранный домен и C-концевой внеклеточный домен coiled-coil, к конечному аминокислотному остатку которого (серин-161) ковалентно прикреплён гликозилфосфотидилинозитоловый якорь (GPI anchor)[3]. C-концевой внеклеточный домен содержит 2 участка гликозилирования и 3 цистеина, участвующих в образовании межмолекулярной дисульфидной связи.
Функции
Тетерин ингибирует выделение дочерних вирусных частиц из заражённой клетки. Был открыт как белок, который ингибирует выделение дочерних вирусных частиц ВИЧ-1 в отсутствие вирусного белка Vpu, в определённых рестриктивных типах клеток (HeLa, Jurkat, мононуклеарные клетки периферической крови)[1][2]. Позднее было обнаружено, что тетерин ингибирует выделение из заражённой клетки и других ретровирусов (например, ВИЧ-2, вирус иммунодефицита обезьян [ВИО]), а также аренавирусов (например, вирус Ласса, вызывающий лихорадку Ласса), филовирусов (например, вирус Марбург, вирус Эбола)[4][5][6][7] и герпесвируса, ассоциированного с саркомой Капоши (KSHV)[8].
Когда созревшие вирионы отпочковываются от клеточной мембраны, один мембранный домен тетерина встраивается в мембрану вирусной частицы, а другой остаётся на клеточной мембране, удерживая вирион на поверхности клетки, таким образом, препятствуя выделению зрелых вирусных частиц во внеклеточную среду и предотвращая заражение новых клеток[9][10].
Экспрессия тетерина индуцируется интерфероном[1][2].
Вирусные белки-антагонисты тетерина
Геномы ряда вирусов кодируют белки-антагонисты тетерина, подавляющие его антивирусную активность и, следовательно, стимулирующие выделение вирусных частиц из заражённой клетки. Например, у двух групп лентивирусов приматов, 1) ВИЧ-1/ВИО шимпанзе и 2) ВИО большой пятнистоносой обезьяны, усатой обезьяны и обезьяны мона, таким белком является Vpu[1][2]. У большинства других ВИО антагонистом служит белок Nef. У ВИЧ-2 в качестве антагониста функционирует белок Env. Кроме того, антагонистами тетерина являются белок К5 вируса KSHV[8] и гликопротеин вируса Эбола[5]. Белок Vpu вызывает снижение экспрессии тетерина на поверхности клетки[11]. Предполагается, что этот эффект опосредован, по крайней мере, тремя механизмами: 1) нарушением мембранного транспорта вновь синтезированного тетерина, 2) подавлением рециклизации тетерина, 3) прямой интернализацией тетерина с клеточной поверхности. Однако в некоторых клеточных линиях (CEMx174, H9) взаимодействие Vpu и тетерина не приводит к уменьшению экспрессии тетерина на поверхности клетки, несмотря на наблюдаемое стимулирование выделения вирусных частиц из клетки[12]. Это указывает на существование альтернативных механизмов антагонизма активности тетерина со стороны Vpu. Кроме того, Vpu активирует внутриклеточную деградацию тетерина, опосредованную β-TrCP2[13].
См. также
- Кластер дифференцировки
- АPOBEC3
Примечания
- ↑ 1 2 3 4 Neil S.J., Zang T., Bieniasz P.D. Tetherin inhibits retrovirus release and is antagonized by HIV-1 Vpu (англ.) // Nature : journal. — 2008. — January (vol. 451, no. 7177). — P. 425—430. — doi:10.1038/nature06553. — PMID 18200009.
- ↑ 1 2 3 4 van Damme N, Goff D, Katsura C, Jorgensen RL, Mitchell R, Johnson MC, Stephens EB, Guatelli J (2008) The interferon-induced protein BST-2 restricts HIV-1 release and is downregulated from the cell surface by the viral Vpu protein. Cell Host Microbe 3, 245-252
- ↑ 1 2 Andrew A.J., Miyagi E., Kao S., Strebel K. The formation of cysteine-linked dimers of BST-2/tetherin is important for inhibition of HIV-1 virus release but not for sensitivity to Vpu (англ.) // BioMed Central[англ.] : journal. — 2009. — Vol. 6. — P. 80. — doi:10.1186/1742-4690-6-80. — PMID 19737401. — PMC 2754425.
- ↑ Jouvenet, N., Neil, S.J.D., Bess, C., Johnson, M.C., Virgen, C.A., Simon, S.M., Bieniasz, P.D., 2009. Broad-spectrum inhibition of retroviral and filoviral particle release by tetherin. J. Virol. 83, 1837–1844
- ↑ 1 2 Kaletsky, R.L., Francica, J.R., Agrawal-Gamse, C., Bates, P., 2009. Tetherin-mediated restriction of filovirus budding is antagonized by the Ebola glycoprotein. Proc. Natl. Acad. Sci. U. S. A. 106, 2886–2891
- ↑ Sakuma T., Noda T., Urata S., Kawaoka Y., Yasuda J. Inhibition of Lassa and Marburg virus production by tetherin (англ.) // Journal of Virology[англ.] : journal. — 2009. — March (vol. 83, no. 5). — P. 2382—2385. — doi:10.1128/JVI.01607-08. — PMID 19091864. — PMC 2643706.
- ↑ Thaczuk D. Tetherin: a newly discovered host cell protein that inhibits HIV replication. NAM AIDS Map (11 февраля 2008). Архивировано из оригинала 27 мая 2010 года.
- ↑ 1 2 Mansouri, M., Viswanathan, K., Douglas, J.L., Hines, J., Gustin, J., Moses, A.V., Früh, K., 2009. Molecular mechanism of BST2/tetherin downregulation by K5/MIR2 of Kaposi's sarcoma-associated herpesvirus. J. Virol. 83, 9672–9681
- ↑ Perez-Caballero, D., Zang, T., Ebrahimi, A., McNatt, M.W., Gregory, D.A., Johnson, M.C., Bieniasz, P.D., 2009. Tetherin inhibits HIV-1 release by directly tethering virions to cells. Cell 139, 499–511
- ↑ Ученые объяснили механизм действия интерферона на ВИЧ. Дата обращения: 21 декабря 2012. Архивировано 25 марта 2013 года.
- ↑ Iwabu Y., Fujita H., Kinomoto M., Kaneko K., Ishizaka Y., Tanaka Y., Sata T., Tokunaga K. HIV-1 accessory protein Vpu internalizes cell-surface BST-2/tetherin through transmembrane interactions leading to lysosomes (англ.) // Journal of Biological Chemistry : journal. — 2009. — December (vol. 284, no. 50). — P. 35060—35072. — doi:10.1074/jbc.M109.058305. — PMID 19837671. — PMC 2787367.
- ↑ Miyagi, E., Andrew, A.J., Kao, S., Strebel, K., 2009. Vpu enhances HIV-1 virus release in the absence of BST-2 cell surface down-modulation and intracellular depletion. Proc. Natl. Acad. Sci. U. S. A. 106, 2869–2873
- ↑ Mangeat B., Gers-Huber G., Lehmann M., Zufferey M., Luban J., Piguet V. HIV-1 Vpu neutralizes the antiviral factor Tetherin/BST-2 by binding it and directing its beta-TrCP2-dependent degradation (англ.) // PLOS Pathogens : journal. — 2009. — September (vol. 5, no. 9). — P. e1000574. — doi:10.1371/journal.ppat.1000574. — PMID 19730691. — PMC 2729927.
Литература
- Furuya Y., Takasawa S., Yonekura H., et al. Cloning of a cDNA encoding rat bone marrow stromal cell antigen 1 (BST-1) from the islets of Langerhans. (англ.) // Gene[англ.] : journal. — Elsevier, 1996. — Vol. 165, no. 2. — P. 329—330. — doi:10.1016/0378-1119(95)00540-M. — PMID 8522202.
- Ohtomo T., Sugamata Y., Ozaki Y., et al. Molecular cloning and characterization of a surface antigen preferentially overexpressed on multiple myeloma cells. (англ.) // Biochemical and Biophysical Research Communications[англ.] : journal. — 1999. — Vol. 258, no. 3. — P. 583—591. — doi:10.1006/bbrc.1999.0683. — PMID 10329429.