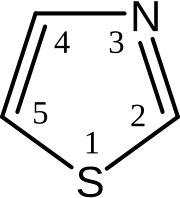
Тиазол
| Тиазол | |
|---|---|
 | |
| Общие | |
| Хим. формула | C3H3SN |
| Физические свойства | |
| Молярная масса | 85,13 г/моль |
| Плотность | 1,198 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | −33 °C[1] |
| • кипения | 117-118 °C |
| Оптические свойства | |
| Показатель преломления | 1,5969 |
| Классификация | |
| Рег. номер CAS | 288-47-1 |
| PubChem | 9256 |
| Рег. номер EINECS | 206-021-3 |
| SMILES | |
| InChI | |
| ChEBI | 43732 |
| ChemSpider | 8899 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Тиазол — гетероциклическое соединение, аналог тиофена, содержащий вместо CH-группы в положении 3 атом азота.
Физические и химические свойства
Тиазол представляет собой бесцветную жидкость с запахом пиридина. Тиазол растворим в воде и в органических растворителях.
Как и молекулы других азолов, молекула тиазола обладает гетероароматической 6π-электронной системой. По своим химическим свойствам тиазол приближается к пиридину и тиофену. Тиазол вступает в реакции электрофильного замещения, но его реакционноспособность снижается вследствие N-протонирования или комплексообразования с кислотами Льюиса. Однако в отсутствие кислот Льюиса реакции электрофильного замещения, в частности, нитрование в среде уксусного ангидрида и бромирование в бензоле, идут в положение 5 по механизму образования σ-комплекса. При этом реакционноспособность уменьшается в ряду 5- > 2- > 4-положение.
Также возможно протекание реакций по илидному механизму, например, реакция изотопного обмена:

Тиазол вступает также в реакции нуклеофильного замещения. Легче всего замещение идёт в положение 2 по механизму реакции Чичибабина, например, замещение атома водорода на аминогруппу и реакции металлирования.
Окисление тиазола протекает по атому азота с образованием N-оксидов. Тиазол устойчив к восстановителям в т. ч. к водороду в момент выделения и в присутствии катализаторов. В то же время он реагирует с сильными восстановителями: никель Ренея разрушает молекулу тиазола с десульфуризацией и образованием алифатических соединений, а борогидрид натрия NaBH4 превращает его в тетрагидротиазол.
Получение и применение
Синтез тиазола и его производных осуществляется из аминотиолов и из тиоамидов по общей схеме:

Некоторые производные тиазола являются лекарственными препаратами: 2-сульфаниламидотиазол (норсульфазол) и 2-(N-о-карбоксибензоилсульфанил)амидотиазол (фталазол). Тиазолидиновый цикл является структурными фрагментом молекулы пенициллина и его полусинтетических аналогов. Цикл тиазола входит в состав тиамина.
Некоторые окрашенные производные тиазола являются красителями.
Примечания
- ↑ Bradley J., Williams A., Andrew S.I.D. Lang Jean-Claude Bradley Open Melting Point Dataset // (unknown type) — 2014. — doi:10.6084/M9.FIGSHARE.1031637.V2
Литература
- Зефиров Н.С. и др. т.4 Пол-Три // Химическая энциклопедия. — М.: Большая Российская Энциклопедия, 1995. — 639 с. — 20 000 экз. — ISBN 5-85270-092-4.
- О. Я. Нейланд. Органическая химия. — М.: Высшая школа, 1990. — 751 с. — 35 000 экз. — ISBN 5-06-001471-1.














