
Моле́кула — электрически нейтральная частица, образованная из двух или более связанных атомов.

Органи́ческая хи́мия — раздел химии, изучающий структуру, свойства и методы синтеза соединений углерода с другими химическими элементами, относящихся к органическим соединениям. Первоначальное значение термина органическая химия подразумевало изучение только соединений углерода растительного и животного происхождения. По этой причине ряд углеродсодержащих соединений традиционно не относят к органическим, а рассматривают как неорганические соединения. Условно можно считать, что структурным прототипом органических соединений являются углеводороды.

Ро́берт Са́ндерсон Ма́лликен — американский физик и химик, профессор, лауреат Нобелевской премии по химии (1966).

Алке́ны — ациклические непредельные углеводороды, содержащие одну двойную связь между атомами углерода, образующие гомологический ряд с общей формулой CnH2n.
Ква́нтовая хи́мия — направление теоретической химии, рассматривающее строение и свойства химических соединений, реакционную способность, кинетику и механизм химических реакций на основе квантовой механики. Разделами квантовой химии являются: квантовая теория строения молекул, квантовая теория химических связей и межмолекулярных взаимодействий, квантовая теория химических реакций и реакционной способности и др. Она занимается рассмотрением химических и физических свойств веществ на атомарном уровне. Вследствие того, что сложность изучаемых объектов во многих случаях не позволяет находить явные решения уравнений, описывающих процессы в химических системах, применяют приближенные методы расчета. С квантовой химией неразрывно связана вычислительная химия — дисциплина, использующая математические методы квантовой химии, адаптированные для создания специальных компьютерных программ, используемых для расчета молекулярных свойств, амплитуды вероятности нахождения электронов в атомах, симуляции взаимодействия молекул.
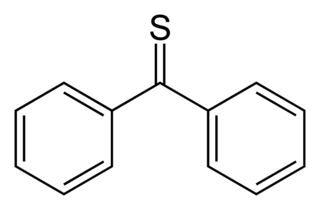
Тиокето́ны (тионы) — тиокарбонильные аналоги кетонов, в которых карбонильный кислород замещен двухвалентной серой, с общей формулой R'R''C=S, где R — углеводородные радикалы.
Химическая связь — взаимодействие атомов, обусловливающее устойчивость молекулы или кристалла как целого. Химическая связь определяется взаимодействием между заряженными частицами. Современное описание химической связи проводится на основе квантовой механики. Основные характеристики химической связи — прочность, длина, полярность, устойчивость.

Теория молекулярных орбиталей (МО) даёт представление о распределении электронной плотности и объясняет свойства молекул.

Вале́нтность — способность атомов образовывать определённое количество химических связей, которые образует атом, или число атомов, которое может присоединить или заместить атом данного элемента.

Ко́мплексные соедине́ния или координацио́нные соедине́ния — это соединения, которые образуются в результате присоединения к данному иону, называемому комплексообразователем, нейтральных молекул или других ионов, называемых лигандами. Теория комплексных соединений была предложена в 1893 г. А. Вернером.
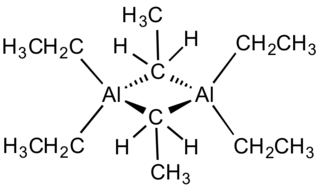
Металлоорганические соединения (МОС) — органические соединения, в молекулах которых существует связь атома металла с атомом/атомами углерода. Цианиды, карбиды, а в некоторых случаях и карбонилы металлов, также содержащие связь металл—углерод, считают неорганическими соединениями. К металлоорганическим соединениям иногда относят органические соединения бора, кремния, фосфора, мышьяка, селена и теллура, поскольку строение и свойства органических соединений с участием этих элементов во многих аспектах сходны с химией родственных им металлорганических соединений алюминия, германия и др. ; однако более точным в этом случае является более общий термин элементорганические соединения, получивший распространение в России и странах бывшего СССР.

Гибридиза́ция орбита́лей — процесс смешения различных атомных орбиталей центрального атома многоатомной молекулы с возникновением одинаковых орбиталей, эквивалентных по своим правилам. Угол между гибридными орбиталями при sp3-гибридизации равен 109.5°, при sp2 — 120°, при sp — 180°.

Ароматические соединения (арены) — циклические органические соединения, которые имеют в своём составе ароматическую систему. Основными отличительными свойствами являются повышенная устойчивость ароматической системы и, несмотря на ненасыщенность, склонность к реакциям замещения, а не присоединения.

Тиоальдегиды — сераорганические соединения, аналоги альдегидов, в которых атом кислорода замещен атомом серы. Тиоальдегиды очень реакционноспособны и обычно циклоолигомеризуются в момент получения.

Пи-связь (π-связь) — ковалентная связь, образующаяся перекрыванием атомных p-орбиталей. В отличие от сигма-связи, осуществляемой перекрыванием s-орбиталей вдоль линии соединения атомов, пи-связи возникают при перекрывании p-орбиталей по обе стороны от линии соединения атомов. Считается, что пи-связь реализуется в кратных связях — двойная связь состоит из одной сигма- и одной пи-связи, тройная — из одной сигма- и двух ортогональных пи-связей.

Подгру́ппа ци́нка — химические элементы 12-й группы периодической таблицы химических элементов. В группу входят цинк Zn, кадмий Cd и ртуть Hg. На основании электронной конфигурации атома к этой же группе относится и искусственно синтезированный элемент коперниций Cn, эксперименты с отдельными атомами которого начали проводиться совсем недавно.

Теория валентных связей — приближённый квантовохимический расчётный метод, основанный на представлении о том, что каждая пара атомов в молекуле удерживается вместе при помощи одной или нескольких общих электронных пар.
Основания — химические соединения, способные образовывать ковалентную связь с протоном либо с вакантной орбиталью другого химического соединения. В узком смысле, под основаниями понимают осно́вные гидроксиды — сложные вещества, при диссоциации которых в водных растворах отщепляется только один вид анионов — гидроксид-ионы OH−.
Сопряжение связей — это явление выравнивания связей и зарядов в реальной молекуле по сравнению с несуществующей идеальной структурой этой молекулы. Происходит из-за взаимодействия между собой электронных систем атомов. За счёт сопряжения происходит изменение длины кратных и одинарных связей, что в свою очередь вызывает геометрическое изменение строения молекулы. Главным признаком сопряжения является распределение электронной плотности по всей системе. Системы, в которых происходит сопряжение, называются сопряжёнными системами, которые делятся на открытые и циклические. Чтобы сопряжение произошло, необходимо, чтобы все электронные системы находились в одной плоскости для взаимодействия друг с другом, и для образования плоского σ-скелета. Если этого не происходит из-за структурного строения молекулы, то говорят о пространственных препятствиях сопряжению.

Тиоацетон (диметилтиокетон) — сераорганическое соединение с формулой (CH3)2CS, простейший представитель тиокетонов.















