Трифторид мышьяка
| Трифторид мышьяка | |||
|---|---|---|---|
| |||
| Общие | |||
| Систематическое наименование | Трифторид мышьяка | ||
| Традиционные названия | Трифторид мышьяка, трёхфтористый мышьяк | ||
| Хим. формула | AsF3 | ||
| Рац. формула | AsF3[1] | ||
| Физические свойства | |||
| Состояние | бесцветная жидкость с неприятным запахом | ||
| Молярная масса | 131,92 г/моль | ||
| Плотность | 2,660; 2,7315; 3,01 г/см³ | ||
| Энергия ионизации | 12,84 эВ[4] | ||
| Термические свойства | |||
| Температура | |||
| • плавления | -5,94; -5,90 °C | ||
| • кипения | 56,3; 57,8; 62,2 °C | ||
| Мол. теплоёмк. | 126,4 Дж/(моль·К) | ||
| Энтальпия | |||
| • образования | -957 кДж/моль | ||
| Оптические свойства | |||
| Показатель преломления | 1,364 | ||
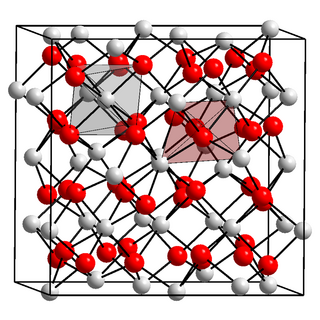
| Структура | |||
| Дипольный момент | 8,6E−30 Кл·м[4] | ||
| Классификация | |||
| Рег. номер CAS | 7784-35-2 | ||
| PubChem | 24571 | ||
| Рег. номер EINECS | 232-060-0 | ||
| SMILES | |||
| InChI | |||
| RTECS | CG5775000 | ||
| ChemSpider | 22975 | ||
| Безопасность | |||
| Предельная концентрация | 0,5 мг/м³[2] | ||
| ЛД50 | 12 мг/кг[3] | ||
| Токсичность | При длительном контакте вызывает поражение ЦНС | ||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
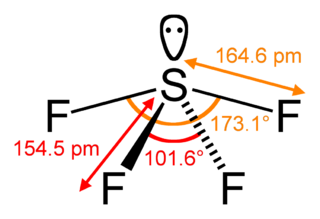
Трифтори́д мышьяка́ — бинарное неорганическое соединение мышьяка и фтора с формулой AsF3, бесцветная токсичная жидкость с неприятным запахом, разлагается в воде.
Получение
- Действием фтористого водорода на триоксид мышьяка:
- Действием фторсульфоновой кислоты на триоксид мышьяка:
Физические свойства
Трифторид мышьяка — бесцветная подвижная жидкость, дымит на воздухе, разлагается водой.
Растворяется в этаноле, диэтиловом эфире, бензоле.
Химические свойства
- Реагирует с водой:
- Окисляется концентрированной азотной кислотой:
- Реагирует с щелочами с образованием гидроарсенита натрия:
- Реагирует с оксидом кремния (разъедает стекло):
- С фторидами щелочных металлов образует комплексные соли:
Применение
Токсичность
Как мышьяксодержащее вещество, фторид мышьяка(III) явно ядовит.
Примечания
- ↑ name=https://docs.cntd.ru_Arsenic trifluoride
- ↑ name=https://docs.cntd.ru_ГОСТ (недоступная ссылка) 12.1.005. ССБТ. Общие санитарно-гигиенические требования к воздуху рабочей зоны
- ↑ name=https://docs.cntd.ru_ГОСТ (недоступная ссылка) 12.1.007. ССБТ. Вредные вещества. Классификация и общие требования безопасности
- ↑ 1 2 David R. Lide, Jr. Basic laboratory and industrial chemicals (англ.): A CRC quick reference handbook — CRC Press, 1993. — ISBN 978-0-8493-4498-5
Литература
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1992. — Т. 3. — 639 с. — ISBN 5-82270-039-8.
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 3-е изд., испр. — Л.: Химия, 1971. — Т. 2. — 1168 с.
- Лидин Р.А. и др. Химические свойства неорганических веществ: Учеб. пособие для вузов. — 3-е изд., испр. — М.: Химия, 2000. — 480 с. — ISBN 5-7245-1163-0.








![{\displaystyle {\mathsf {AsF_{3}+5KF\ {\xrightarrow {}}\ K[AsF_{4}]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/44e611b1f945556503c56b6a26c22aac55ae8c00)