Ке́львин — единица термодинамической температуры в Международной системе единиц (СИ), одна из семи основных единиц СИ. Предложена в 1848 году. Определяется через значение постоянной Больцмана: 1,380 649⋅10−23 Дж/К. До 2019 года определялся как 1 / 273,16 части термодинамической температуры тройной точки воды. Начало шкалы совпадает с абсолютным нулём.

Температу́ра — скалярная физическая величина, характеризующая термодинамическую систему и количественно выражающая интуитивное понятие о различной степени нагретости тел.

Термодинами́ческая фа́за — гомогенная часть гетерогенной системы, ограниченная поверхностью раздела. Менее строго, но более наглядно фазой называют гомогенную часть системы, отделенную от остальных частей видимой поверхностью раздела, на которой скачком меняются какие-либо характеристики фазы, например плотность, состав, оптические свойства. При этом совокупность отдельных гомогенных частей системы, обладающих одинаковыми свойствами, считается одной фазой. Каждая фаза системы характеризуется собственным уравнением состояния.

Агрега́тное состоя́ние вещества — физическое состояние вещества, зависящее от соответствующего сочетания температуры и давления. Изменение агрегатного состояния может сопровождаться скачкообразным изменением свободной энергии, энтропии, плотности и других физических величин.
Фа́зовый перехо́д в термодинамике — переход вещества из одной термодинамической фазы в другую при изменении внешних условий. С точки зрения движения системы по фазовой диаграмме при изменении её интенсивных параметров, фазовый переход происходит, когда система пересекает линию, разделяющую две фазы. Поскольку разные термодинамические фазы описываются различными уравнениями состояния, всегда можно найти величину, которая скачкообразно меняется при фазовом переходе.

Сублима́ция, возго́нка — переход вещества из твёрдого состояния сразу в парообразное, минуя стадию плавления и кипения. Поскольку при возгонке изменяется удельный объём вещества и поглощается энергия, возгонка является фазовым переходом первого рода.

Жи́дкость — вещество, находящееся в жидком агрегатном состоянии, занимающем промежуточное положение между твёрдым и газообразным состояниями.

Азеотро́пная смесь — смесь двух или более жидкостей с таким составом, который не меняется при кипении, то есть составы равновесных жидкой и паровой фаз совпадают.

Эвте́ктика — нонвариантная точка в системе из n компонентов, в которой находятся в термодинамическом равновесии n твёрдых фаз и жидкая фаза. Эвтектическая композиция представляет собой жидкий раствор, кристаллизующийся при наиболее низкой температуре для сплавов данной системы. Соответственно, температура плавления сплава эвтектического состава — также самая низкая, по сравнению со сплавами другого состава для данной системы компонентов. Это явление как раз и отражает этимология термина.

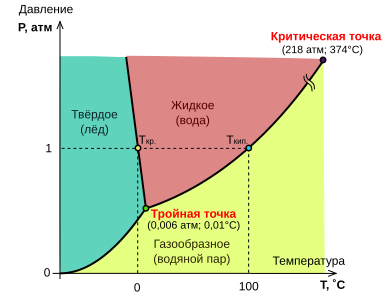
Тройна́я то́чка в однокомпонентной системе — точка схождения кривых двухфазных равновесий на плоской P—T-фазовой диаграмме, соответствующая устойчивому равновесию трёх фаз. Тройная точка нонвариантна, т. е. не допускает изменения ни одного из характеризующих её параметров состояния — ни температуры, ни давления. Индивидуальные вещества могут иметь несколько стабильных кристаллических фаз и вследствие этого несколько тройных точек. В системе, способной к образованию N фаз, число возможных тройных точек равно  . Например, для серы известны четыре фазы — две твёрдые, жидкая и газообразная — и четыре тройные точки, одна из которых метастабильная.
. Например, для серы известны четыре фазы — две твёрдые, жидкая и газообразная — и четыре тройные точки, одна из которых метастабильная.
Пра́вило фаз — соотношение, связывающее число компонентов, фаз и термодинамических степеней свободы в равновесной термодинамической системе. Роль правила фаз особенно велика при рассмотрении гетерогенных равновесий в многофазных многокомпонентных системах.

Вла́жность — показатель содержания воды в физических телах или средах. Для измерения влажности используются различные единицы, часто внесистемные.

Критическая точка фазового равновесия — точка на диаграмме состояния веществ, соответствующая критическому состоянию, то есть конечная точка кривой сосуществования фаз, в котором две фазы, находящиеся в термодинамическом равновесии, становятся тождественными по своим свойствам. В частности, с приближением к критическому состоянию различия в плотности, составе и других свойствах сосуществующих фаз, а также теплота фазового перехода и межфазное поверхностное натяжение уменьшаются, а в критической точке равны нулю. В окрестности критической точки наблюдаются критические явления.

Водяной пар — газообразное агрегатное состояние воды. Не имеет цвета, вкуса и запаха. Водяной пар — в чистом виде или в составе влажного газа, — находящийся в термодинамическом равновесии с поверхностью влажного вещества, называют равновесным водяным паром.
Фа́зовая диагра́мма — графическое отображение равновесного состояния бесконечной физико-химической системы при условиях, отвечающих координатам рассматриваемой точки на диаграмме.

Климатическая камера — камера, позволяющая точно моделировать агрессивное воздействие окружающей среды и применяемая в научно-исследовательских учреждениях, разрабатывающих оборудование для машиностроения, а также оборонной и авиационной промышленности, предполагает наличие высокоточного измерительного прибора для контроля влажности и температуры воздуха.
Аморфный лёд — вода в состоянии твёрдого аморфного вещества, у которого молекулы воды расположены случайным образом, наподобие атомов в обычном стекле. Чаще всего в природе лёд находится в поликристаллическом состоянии. Аморфный лёд отличается тем, что у него отсутствует дальний порядок кристаллической структуры.

Лёд III — тетрагональная кристаллическая разновидность водного льда. Можно получить при охлаждении воды до −23 °C и давлении 300 МПа. Его плотность больше, чем у воды, но он наименее плотный из всех разновидностей льда в зоне высоких давлений. Плотность жидкой фазы при том же давлении около 1,12 г/см³.

H, s-диагра́мма — диаграмма теплофизических свойств жидкости и газа, показывающая характер изменения различных свойств, в зависимости от параметров состояния. В основном большое применение получили h, s-диаграммы воды и водяного пара, так как в качестве рабочего тела в теплотехнике чаще всего применяются именно вода и водяной пар, из-за их сравнительной дешевизны и доступности, причём наиболее пристальное внимание оказывается именно той части диаграммы, в которой вода в парообразном состоянии, так как в жидком состоянии она практически несжимаема.

Фа́зовая диагра́мма воды — графическое отображение равновесного состояния фаз воды. Строится в системе координат температура—давление.