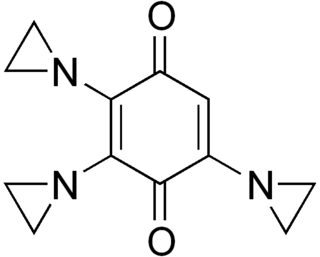
Урамустин
| Урамустин | |
|---|---|
 | |
| Химическое соединение | |
| ИЮПАК | 5-[бис(2-хлорэтил)амино]-1H-пиримидин-2,4-дион |
| Брутто-формула | C8H11Cl2N3O2 |
| Молярная масса | 252.097 г/моль |
| CAS | 66-75-1 |
| PubChem | 6194 |
| DrugBank | DB00791 |
| Состав | |
| Классификация | |
| АТХ | L01AD08 |
| Фармакокинетика | |
| Связывание с белками плазмы | 5% |
| Метаболизм | печёночный |
| Экскреция | почечная |
| Способы введения | |
| внутривенно | |
| Другие названия | |
| Допан | |
Урамустин, иначе называемый хлорэтиламиноурацил, урацил мустард, допан — в настоящее время уже устаревший цитостатический противоопухолевый химиотерапевтический лекарственный препарат алкилирующего типа действия. Производное одновременно бис-β-хлорэтиламина и нуклеотида урацила.
Фармакологическое действие
Устаревший цитостатический противоопухолевый препарат алкилирующего типа. Производное одновременно бис-β-хлорэтиламина и урацила. Подобно многим другим цитостатическим агентам, угнетает костномозговое кроветворение и вызывает тошноту и рвоту.
Урамустин оказывает своё противоопухолевое действие, алкилируя ДНК преимущественно в злокачественных клетках, которые гораздо активнее здоровых клеток захватывают урацил (и, соответственно, урамустин) вследствие их повышенной потребности в нуклеотидах для построения новых нуклеиновых кислот (биосинтез новой ДНК является необходимой частью процесса митотического деления клеток). Повреждение ДНК, вызванное урамустином, приводит к апоптозу повреждённой клетки.
Историческое значение
Комбинация урамустина с 5-фторурацилом — также противоопухолевым производным урацила с другим механизмом действия — являющимся не алкилирующим агентом, а антиметаболитом, антагонистом пиримидинов — была исторически одним из первых успешных примеров применения комбинированной химиотерапии, или полихимиотерапии. Избирательное антимитотическое действие как урамустина, так и 5-фторурацила преимущественно на опухолевую ткань, а не на нормальные быстро делящиеся клетки, основано на одном и том же факте — повышенной потребности опухолевых клеток в урациле и их склонности к повышенному его захвату и утилизации. Именно это и послужило теоретической основой для создания подобного режима полихимиотерапии, получившего специальное название УМ-ФУ (УраМустин + ФторУрацил). Позднее к этому режиму был также добавлен мелфалан) — такой режим получил специальное название УММ-ФУ (УраМустин, Мелфалан, 5-ФторУрацил).
Комбинация урамустина, опционально мелфалана и 5-фторурацила с успехом использовалась в период с 1964 по 1971 в медицинском центре Йельского университета для лечения рака яичников — злокачественной опухоли, обладающей одной из наиболее высоких химиочувствительностей среди всех солидных опухолей человека. Полихимиотерапия комбинацией УМ-ФУ или УММ-ФУ опционально предлагалась больным женщинам с гистологически верифицированной III—IV стадией рака яичников (то есть фактически умирающим, «безнадёжно больным» по тогдашним понятиям женщинам). При этом урамустин назначался перорально в дозе 1 мг/кг. 5-Фторурацил назначался внутривенно в дозе 5 мг/кг в течение 5 дней подряд каждые 4 недели. Мелфалан опционально назначался в дозе 1 мг/кг внутривенно 2 дня подряд (в те же дни, что и фторурацил) также с интервалом 4 недели. Из 185 женщин с поздними стадиями рака яичников, проходивших лечение в медицинском центре Йельского университета, 76 пациенток дали согласие на проведение им полихимиотерапии по протоколу УМ-ФУ или УММ-ФУ. Из этих 76 пациенток 35 имели объективно измеримые признаки сохраняющейся активности заболевания после проведённого хирургического или лучевого лечения. Пятнадцать пациенток (42 %) из них показали наличие объективного эффекта, длившегося от 3 до 95 месяцев, с уменьшением размеров опухолевых масс и исчезновением признаков асцита или гидроторакса. Медиана продолжительности жизни в этой подгруппе пациенток (то есть ответивших регрессом опухоли на химиотерапию УМ-ФУ или УММ-ФУ) составляла 41 месяц, что для запущенного рака яичников, как опухоли весьма быстро растущей и размножающейся, очень долго. Двадцать пациенток показали отсутствие какого-либо объективного эффекта при лечении урамустином, мелфаланом и 5-фторурацилом. Медиана выживаемости в этой подгруппе, как и в подгруппе больных, отказавшихся от активной химиотерапии и получавших лишь паллиативную терапию, составляла всего 18 месяцев. Три пациентки, получавшие УММ-ФУ, в период терапии заболели острым миелоидным лейкозом, что, в принципе, является давно известным побочным эффектом алкилирующих препаратов, таких, как урамустин и мелфалан.
Исследователи Йельского университета сделали на основании этих наблюдений вывод, что режимы полихимиотерапии УМ-ФУ (урамустин, 5-фторурацил) и УММ-ФУ (урамустин, мелфалан, 5-фторурацил) являются эффективным методом сдерживания и контроля прогрессии запущенного метастатического рака яичников и способны увеличивать продолжительность жизни больных с поздними стадиями рака яичников, уменьшать опухолевую массу и ликвидировать либо уменьшать асцит и/или гидроторакс. Однако открытие доксорубицина (адриамицина), а затем и производных платины привело к созданию новых, более эффективных режимов полихимиотерапии метастатического рака яичников. Вследствие этого урамустин вышел из употребления и ныне недоступен (не производится и не поставляется). А режимы полихимиотерапии УМ-ФУ и УММ-ФУ в настоящее время представляют лишь сугубо исторический интерес.[1]
Исторические показания к применению
Во времена, когда урамустин активно применялся в онкологии, показаниями к его применению служили преимущественно злокачественные заболевания лимфоидной ткани, такие, как лимфогранулематоз, хронический миелолейкоз, хронический лимфолейкоз. Также урамустин применялся в лечении лимфосарком и саркомы мягких тканей.[2] В сочетании с 5-фторурацилом и опционально мелфаланом (режимы УМ-ФУ и УММ-ФУ) он применялся также при раке яичников.
Наблюдение за пациентом с диффузной крупноклеточной лимфомой, который после всего лишь одного 3-дневного курса монохимиотерапии урамустином дал полную ремиссию заболевания, продолжавшуюся 35 лет, стимулировало авторов одной статьи 1999 года опубликовать ретроспективные данные об их опыте лечения урамустином пациентов с различными гематологическими заболеваниями в период между 1958 и 1970 годами. Авторами было показано, что суммарные дозы урамустина у этих больных были сравнимы с суммарными дозами мехлоретамина, однако различались режимы дозирования и пути введения. При применении урамустина реже встречалась серьёзная (III—IV степени) и неприемлемая гематологическая токсичность и реже наблюдалось развитие вторичных опухолей и лейкозов, по сравнению с применением мехлоретамина (что подтверждает известное ещё со времени создания урамустина мнение о его меньшей токсичности по сравнению с мехлоретамином). Применяя современные, значительно более строгие по сравнению с тогдашними, методы и критерии для оценки клинического ответа на химиотерапию к ретроспективному анализу историй болезни тех пациентов, которые получали урамустин, авторы статьи обнаружили, что общий процент опухолевой регрессии в группе из 94 пациентов с неходжкинскими лимфомами составлял 69,2 % (из них 23,4 % полных клинико-гематологических ремиссий). В группе из 62 пациентов с лимфогранулематозом, общий процент опухолевой регрессии составлял 69,4 % (9,7 % полных клинико-гематологических ремиссий). В группе из 39 пациентов с хроническим лимфолейкозом частота полных или частичных клинико-гематологических ремиссий составляла 74 % (из них 7,7 % именно полных ремиссий). Основным побочным эффектом терапии урамустином было угнетение костномозгового кроветворения, особенно тромбоцитопения. На основании этого ретроспективного анализа авторы статьи сделали вывод, что урамустин является эффективным и недорогим средством пероральной химиотерапии ряда злокачественных опухолей лимфоидной системы (таких, как лимфома, лимфогранулематоз, хронический лимфолейкоз), и что, видимо, данный препарат зря был снят с производства и нуждается в переоценке с современных позиций и возможной разработке схем комбинированной химиотерапии с его участием.[3]
Побочные явления
Угнетение костномозгового кроветворения (лейкопения, тромбоцитопения, анемия), тошнота и рвота, снижение аппетита.
Ссылки
- ↑ Kohorn EI.Uracil mustard and 5-fluorouracil combination chemotherapy: a historic record. Conn Med. 2013 Aug;77(7):433-6. Дата обращения: 3 октября 2017. Архивировано 2 февраля 2014 года.
- ↑ Berry DH, Sutow WW, Vietti TJ, Fernbach DJ, Sullivan MP, Haggard ME, Lane DM. Evaluation of uracil mustard in children with Hodgkin’s disease, lymphosarcoma, and soft tissue sarcoma. J Clin Pharmacol New Drugs. 1972 Apr;12(4):169-73. Дата обращения: 3 октября 2017. Архивировано 22 мая 2016 года.
- ↑ Kennedy BJ, Torkelson JL, Torlakovic E. Uracil mustard revisited. Cancer. 1999 May 15;85(10):2265-72. Дата обращения: 3 октября 2017. Архивировано 3 июня 2016 года.