Феноловый красный
| Феноловый красный | |
|---|---|
  | |
 | |
| Общие | |
| Традиционные названия | Феноловый красный |
| Хим. формула | C19H14O5S1 |
| Физические свойства | |
| Молярная масса | 354,38 г/моль |
| Классификация | |
| Рег. номер CAS | 143-74-8 |
| PubChem | 4766 |
| Рег. номер EINECS | 205-609-7 |
| SMILES | |
| InChI | |
| ChEBI | 31991 |
| ChemSpider | 4602 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Феноловый красный (фенолсульфофталеин, фенолрот, сульфенталь) — кислотно-основный индикатор, изменяющий окраску от жёлтой (в кислой среде) до красной (в щелочной). Нашёл применение также в медицине, где используется для определения парциальных функций почек.
Синтез
Первоначально перемешивают кристаллы фенола, с фталевым ангидридом в соотношении 1:3. Затем очень медленно добавляют серную кислоту до тех пор, пока смесь полностью не пропитается кислотой, при этом её регулярно перемешивают. Далее смесь нагревают до появлении клубов белого дыма. После добавления воды феноловый красный выпадает в виде осадка[1].
Свойства
Феноловый красный представляет собой мелкодисперсный порошок тёмно-красного цвета, устойчив в воздухе. Кристаллы его имеют ромбическую форму и характерный запах. Умеренно растворим в воде, хорошо растворим в спирте и ацетоне, так в 1 л воды растворяется 0,77 г фенолрота, а в 1 л этанола растворяется целых 2,9 г этого вещества[2].
Как индикатор обладает способностью изменять свою окраску в зависимости от состояния среды, в которой находится. Так, например, в кислой среде имеет желтоватую окраску, а в щелочной среде — ярко-красную (некоторые учёные сравнивают этот цвет с цветом фуксии). Переход от жёлтой окраски в красную осуществляется в интервале pH от 6,8 до 8,4.[3]
| Феноловый красный | |
|---|---|
| (pH индикатор) | |
| Нижний предел | Верхний предел |
| pH 6.8 | pH 8.4 |
| yellow | fuchsia |
Применение
В аналитической химии
В аналитической химии феноловый красный используют, как и многие другие кислотно-основные индикаторы, для нахождения точки эквивалентности при титровании растворов. Перед началом титрования в исследуемый раствор добавляют несколько капель фенолового красного и начинают по каплям добавлять титрант. Как только раствор вслед за индикатором изменяет свой цвет, титрование прекращают, этот момент приблизительно и есть точка эквивалентности.
В медицине
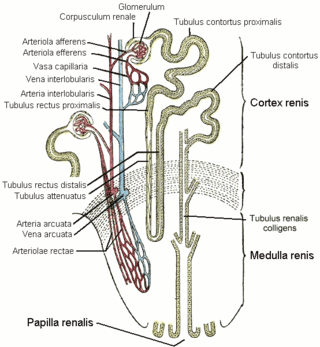
В медицинской практике известно использование фенолрота для определения почечной канальцевой секреции и определения функции проксимальных почечных канальцев. Данная методика известна как проба с фенолротом (феноловым красным)[4]. Суть её в том, что фенолрот избирательно секретируется в проксимальных канальцах за первые часы, не накапливаясь в тканях. Её проводят следующим образом. Сначала обследуемый выпивает определённое количество жидкости (от 400 мл, если речь идёт о детях[5], до 1 л — взрослые). Через 20—30 минут пациент опорожняет мочевой пузырь, после чего ему вводят внутримышечно 6 мг фенолрота, который предварительно растворяют в 1 мл стерильного физиологического раствора. Далее производится сбор мочи в течение 2 часов. У здорового ребёнка за первый час выделяется 40—60 % введённого фенолрота, за второй — 20—25 %. Всего за 2 ч выделяется 60—85 % введённого количества краски. Скорость выведения фенолрота снижается при нарушении функции канальцев, а последнее наблюдается при пиелонефрите.
В микробиологии
В микробиологии феноловый красный иногда используют для приготовления жидких питательных сред[6][7] для дифференциации различных микроорганизмов. Для этого сперва готовят раствор того или иного углевода, добавляют в него феноловый красный и заселяют микроорганизмы. Микроорганизмы способны ферментировать определённые углеводы, при этом меняется кислотность среды, что и улавливает индикатор.
В 1954 году известный американский вирусолог Джонас Солк[8] разработал так называемую цветную пробу для обнаружения вирусов в исследуемом материале. В основе данной методики лежала следующая особенность: в незаражённых тканевых культурах клетки выделяют продукты метаболизма, которые подкисляют среду, и феноловый красный, добавленный в среду, окрашивает её в жёлтый цвет. Если же исследуемый материал содержит вирус, то при добавлении его в тканевую культуру вирус проникает в клетки и убивает их, процессы метаболизма при этом останавливаются, клетки перестают выделять продукты метаболизма, и среда в этом случае сохраняет красный цвет[9][10].
Примечания
- ↑ Химические реактивы (реагенты): Феноловый красный (ТУ 6-09-3070-84). Дата обращения: 14 октября 2011. Архивировано 27 октября 2013 года.
- ↑ Merck Index, 11th ed., 7213 Phenolsulfonphtalein
- ↑ Индикаторы: Феноловый красный (фенолсульфофталеин). Дата обращения: 14 октября 2011. Архивировано 11 января 2010 года.
- ↑ Чиж А. С. Нефрология в терапевтической практике Архивная копия от 19 августа 2010 на Wayback Machine
- ↑ Клинико-лабораторное исследование: Определение секреторной функции проксимального отдела нефрона; Определение функции дистального отдела нефрона. Дата обращения: 16 октября 2011. Архивировано из оригинала 5 декабря 2014 года.
- ↑ Бульонные среды с феноловым красным (БФК). Дата обращения: 14 октября 2011. Архивировано 4 июня 2010 года.
- ↑ Питательная среда с бриллиантовым зелёным и феноловым красным сухая (среда для выделения сальмонелл-ПД). Дата обращения: 15 октября 2011. Архивировано из оригинала 25 августа 2011 года.
- ↑ Основы ветеринарной вирусологии. Дата обращения: 15 октября 2011. Архивировано 20 декабря 2011 года.
- ↑ Основы вирусологии. Дата обращения: 15 октября 2011. Архивировано из оригинала 15 ноября 2011 года.
- ↑ Общая вирусология | Симптомы болезней. Лечение болезней. Профилактика заболеваний. Дата обращения: 15 октября 2011. Архивировано из оригинала 6 декабря 2014 года.
Ссылки
- [www.xumuk.ru/spravochnik/2069.html Феноловый красный // «Xumuk»: Мини-справочник по химическим веществам]