Моле́кула — электрически нейтральная частица, образованная из двух или более связанных атомов.

Немета́ллы — химические элементы, как правило, не обладающие свойствами металлов. Занимают правый верхний угол Периодической системы элементов Менделеева и обычно отделены линией (лесенкой). Количество неметаллов составляет 22-23 элемента, в зависимости от классификации.

Краси́тели — химические соединения, обладающие способностью интенсивно поглощать и преобразовывать энергию электромагнитного излучения в видимой и в ближних ультрафиолетовой и инфракрасной областях спектра и применяемые для придания этой способности другим телам. Термин «краситель» своим происхождением обязан А. Е. Порай-Кошицу и было введено им в научную терминологию в 1908 году.

Фено́лы — органические соединения ароматического ряда, в молекулах которых гидроксильные группы OH− связаны с атомами углерода ароматического кольца.

Митохо́ндрия — двумембранная сферическая или эллипсоидная органелла диаметром обычно около 1 микрометра. Характерна для большинства эукариотических клеток, как автотрофов, так и гетеротрофов. Энергетическая станция клетки; основная функция — окисление органических соединений и использование освобождающейся при их распаде энергии для генерации электрического потенциала, синтеза АТФ и термогенеза. Эти три процесса осуществляются за счёт движения электронов по электронно-транспортной цепи белков внутренней мембраны. Количество митохондрий в клетках различных организмов существенно отличается: так, одноклеточные зелёные водоросли и трипаносомы имеют лишь одну гигантскую митохондрию, тогда как ооцит и амёба Chaos chaos содержат 300 000 и 500 000 митохондрий соответственно; у кишечных анаэробных энтамёб и некоторых других паразитических простейших митохондрии отсутствуют. В специализированных клетках органов животных содержатся сотни и даже тысячи митохондрий.

Окисли́тельно-восстанови́тельные реа́кции (ОВР), также редокс — химические реакции, протекающие с изменением степеней окисления атомов, входящих в состав реагирующих веществ, реализующиеся путём перераспределения электронов между атомом-окислителем (акцептором) и атомом-восстановителем (донором).
Химическая связь — взаимодействие атомов, обусловливающее устойчивость молекулы или кристалла как целого. Химическая связь определяется взаимодействием между заряженными частицами. Современное описание химической связи проводится на основе квантовой механики. Основные характеристики химической связи — прочность, длина, полярность, устойчивость.

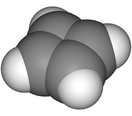
Бутадие́н-1,3  — ненасыщенный углеводород, простейший представитель сопряжённых диеновых углеводородов.
— ненасыщенный углеводород, простейший представитель сопряжённых диеновых углеводородов.

Ковале́нтная связь — химическая связь, образованная перекрытием (обобществлением) пары валентных электронных облаков. Обеспечивающие связь электронные облака (электроны) называются общей электронной парой.
Лига́нд — атом, ион или молекула, связанные с другим атомом (акцептором) с помощью донорно-акцепторного взаимодействия. Понятие применяется в химии комплексных соединений, обозначая присоединенные к одному или нескольким центральным (комплексообразующим) атомам металла частицы.

Свободные радикалы в химии — частицы, содержащие один или несколько неспаренных электронов на внешней электронной оболочке. Свободные радикалы бывают твёрдыми, жидкими и газообразными веществами и могут существовать от очень короткого до очень долгого времени. Радикалы могут быть не только нейтральными, но и ионными, а также иметь более одного неспаренного электрона. Свободные радикалы обладают парамагнитными свойствами и являются очень реакционноспособными частицами.

Аромати́чность — особое свойство некоторых химических соединений, благодаря которому сопряжённое кольцо ненасыщенных связей проявляет аномально высокую стабильность; большую чем та, которую можно было бы ожидать только при одном сопряжении.
Мезомерный эффект — смещение электронной плотности химической связи по π-связям. Объясняется теорией химического резонанса.

Ароматические соединения (арены) — циклические органические соединения, которые имеют в своём составе ароматическую систему. Основными отличительными свойствами являются повышенная устойчивость ароматической системы и, несмотря на ненасыщенность, склонность к реакциям замещения, а не присоединения.

Термин стэкинг в супрамолекулярной химии относится к такому расположению ароматических молекул, которое напоминает расположение монет в стопке и поддерживается ароматическими взаимодействиями. Наиболее популярный пример такого расположения наблюдается в последовательных парах оснований ДНК. Стэкинг также часто наблюдается в белках, когда два относительно неполярных кольца имеют перекрывающиеся π-орбитали. Точная природа таких взаимодействий остаётся предметом обсуждений.
Хиноны — полностью сопряжённые циклогексадиеноны и их аннелированные аналоги. Существуют два класса хинонов: пара-хиноны с пара-расположением карбонильных групп (1,4-хиноны) и орто-хиноны с орто-расположением карбонильных групп (1,2-хиноны). Благодаря способности к обратимому восстановлению до двухатомных фенолов некоторые производные пара-хинонов участвуют в процессах биологического окисления в качестве коферментов ряда оксидоредуктаз.
Ко второ́му пери́оду периоди́ческой систе́мы относятся элементы второй строки периодической системы химических элементов. Строение периодической таблицы основано на строках для иллюстрации повторяющихся (периодических) трендов в химических свойствах элементов при увеличении атомного числа: новая строка начинается тогда, когда химические свойства повторяются, что означает, что элементы с аналогичными свойствами попадают в один и тот же вертикальный столбец. Второй период содержит больше элементов, чем предыдущий, в него входят: литий, бериллий, бор, углерод, азот, кислород, фтор и неон. Данное положение объясняется современной теорией строения атома.
Аннулены — моноциклические углеводороды без боковых цепей в углеродном скелете, содержащие максимально возможное число некумулированных двойных связей общей формулы CnHn или CnHn+1. В систематической номенклатуре аннулены с семью и выше углеродными атомами именуются как [n]аннулены, например, [9]аннулен - циклонона-1,3,5,7-тетраен.

Цис-транс-изомерия или геометрическая изомерия — один из видов стереоизомерии: заключается в возможности расположения заместителей по одну или по разные стороны плоскости двойной связи или неароматического цикла. Все геометрические изомеры относятся к диастереомерам, так как не являются зеркальными отражениями друг друга. Цис- и транс-изомеры встречаются как среди органических соединений, так и среди неорганических. Понятия цис и транс не используются в случае конформеров, двух геометрических форм, легко переходящих друг в друга, вместо них используются обозначения «син» и «анти».
Сопряжение связей — это явление выравнивания связей и зарядов в реальной молекуле по сравнению с несуществующей идеальной структурой этой молекулы. Происходит из-за взаимодействия между собой электронных систем атомов. За счёт сопряжения происходит изменение длины кратных и одинарных связей, что в свою очередь вызывает геометрическое изменение строения молекулы. Главным признаком сопряжения является распределение электронной плотности по всей системе. Системы, в которых происходит сопряжение, называются сопряжёнными системами, которые делятся на открытые и циклические. Чтобы сопряжение произошло, необходимо, чтобы все электронные системы находились в одной плоскости для взаимодействия друг с другом, и для образования плоского σ-скелета. Если этого не происходит из-за структурного строения молекулы, то говорят о пространственных препятствиях сопряжению.