Ами́ды — производные кислородсодержащих кислот, в которых гидроксильная группа кислотного остатка заменена аминогруппой. Амиды также можно рассматривать как ацилпроизводные аминов. Соединения с одним, двумя или тремя ацильными заместителями у атома азота называются первичными, вторичными и третичными амидами соответственно. Вторичные амиды также называют имидами.
Ами́ны — органические соединения, являющиеся производными аммиака, в молекуле которого один или несколько атомов водорода замещены на углеводородные радикалы. По числу замещённых атомов водорода различают соответственно первичные (замещён один атом водорода), вторичные (замещены два атома из трёх) и третичные амины (замещены все три атома). Выделяют также четвертичные аммониевые соединения вида R4N+X-.

Просты́е эфи́ры — органические вещества, имеющие формулу R-O-R', где R и R' — алкильные, арильные или другие заместители. Простые эфиры являются летучими жидкостями с приятным запахом. Благодаря своей химической инертности и особым сольватационным свойствам они широко используются как растворители в промышленности и лаборатории.

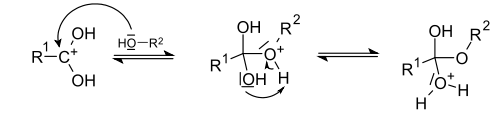
Сло́жные эфи́ры, или эсте́ры , — производные кислородных кислот, имеющих общую формулу RkE(=O)l(OH)m, где l ≠ 0, формально являющиеся продуктами замещения атомов водорода в гидроксилах —OH кислотной функции на углеводородный остаток ; рассматриваются также как ацилпроизводные спиртов. В номенклатуре IUPAC к сложным эфирам относят также ацилпроизводные халькогенидных аналогов спиртов.

Альдеги́ды — класс органических соединений, содержащих альдегидную группу (-CHO). ИЮПАК определяет альдегиды как вещества вида R-CHO, в которых карбонильная группа связана с одним атомом водорода и одной группой R.
Кисло́ты — химические соединения, способные отдавать катион водорода, либо соединения, способные принимать электронную пару с образованием ковалентной связи.

Растворитель — вещество, способное растворять другие твёрдые, жидкие или газообразные вещества, не изменяя их химически. Как правило, при атмосферном давлении и комнатной температуре растворитель является жидким веществом. Соответственно, в растворах, представляющих собой смеси жидкого и твёрдого либо жидкого и газообразного вещества, растворителем считается жидкий компонент. В смесях жидких веществ растворителем считается тот компонент, который присутствует в значительно большем количестве, либо произвольным образом.
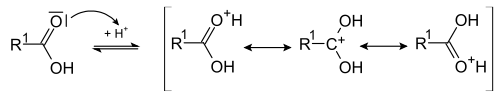
Карбо́новые кисло́ты — класс органических соединений, молекулы которых содержат одну или несколько функциональных карбоксильных групп COOH. Кислотные свойства объясняются тем, что данная группа может сравнительно легко отщеплять протоны. За редкими исключениями карбоновые кислоты являются слабыми. Например, у уксусной кислоты CH3COOH константа диссоциации равна 1,75⋅10−5. Ди- и трикарбоновые кислоты более сильные, чем монокарбоновые кислоты.

Ацетоуксусный эфир, также этиловый эфир ацетоуксусной кислоты, этилацетоацетат — органическое соединение, сложный эфир, бесцветная подвижная жидкость со своеобразным нерезким запахом. Растворяется в воде, смешивается с этанолом и диэтиловым эфиром.

Хлорангидри́д карбо́новой кислоты́ (ацилхлорид) — производное карбоновой кислоты, в которой гидроксильная группа -OH в карбоксильной группе -COOH заменена на атом хлора. Общая формула R-COCl. Первый представитель с R=H не существует, хотя смесь CO и HCl в реакции Гаттермана — Коха ведёт себя подобно хлорангидриду муравьиной кислоты.
Восстановление, в химии, — это процесс, в результате которого:
- частица принимает один или несколько электронов;
- происходит понижение степени окисления какого-либо атома в данной частице;
- органическое вещество теряет атомы кислорода и (или) приобретает атомы водорода.

Нитрозосоединения — органические, содержащие одну или несколько нитрозогрупп —N=O, связанных с атомами углерода (C-нитрозосоединения), азота (N-нитрозосоединения — нитрозамины, R2N-N=O) или кислорода (O-нитрозосоединения — органические нитриты, сложные эфиры азотистой кислоты), серы (нитрозотиолы, RS-N=O). Под нитрозосоединениями обычно подразумевают C-нитрозосоединения. Можно рассматривать эти соединения, как углеводородные производные нитрозила. Известны и неорганические нитрозильные соединения, как с металлами (M-N=O) так и с неметаллами (например, Cl-N=O, NO-ClO4).
Ката́лиз — избирательное ускорение одного из возможных термодинамически разрешённых направлений химической реакции под действием катализатора(ов), который, согласно теории промежуточных соединений, многократно вступает в промежуточное химическое взаимодействие с участниками реакции и восстанавливает свой химический состав после каждого цикла промежуточных химических взаимодействий.

Гидроксид-ион — отрицательно заряженный ион гидроксида OH−.
Реакции нуклеофильного замещения — реакции замещения, в которых атаку осуществляет нуклеофил — реагент, несущий неподеленную электронную пару. Уходящая группа в реакциях нуклеофильного замещения называется нуклеофуг.

Нитроэфиры (O-нитросоединения, органические нитраты) — органические соединения, содержащие одну или несколько групп -О-NO2, соединённых ковалентной связью с атомом углерода, сложные эфиры азотной кислоты и спиртов.

Альдольная конденсация — химическая реакция между двумя молекулами альдегида или кетона в присутствии кислоты или основания с образованием альдоля, а в некоторых случаях — продукта дегидратации альдоля.

Ацилали (от ацил- и альдегид) — сложные диэфиры гем-диолов общей формулы (RCOO)2CR1R2, формально являющиеся продуктами этерификации гидратированных альдегидов или кетонов карбоновыми кислотами. Иногда ацилалями также называют сложные эфиры гемиацеталей общей формулы (RCOO)(R3O)CR1R2.
Электрофил — реагент или молекула, имеющая свободную орбиталь на внешнем электронном уровне. Как правило такие реагенты являются акцепторами пары электронов при образовании химической связи с нуклеофилом, являющимся донором электронной пары и вытесняет уходящую группу в виде положительно заряженной частицы. Все электрофилы являются кислотами Льюиса.

Сульфиновые кислоты (сульфикислоты) — класс кислородсодержащих органических кислот средней силы с общей формулой RSO(OH), где R — алкильный или арильный радикал. Являются твёрдыми малоустойчивыми веществами, в природе встречаются крайне редко. Образуют устойчивые соли — сульфинаты.
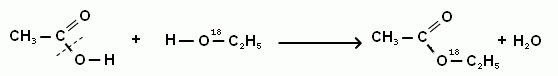
![{\displaystyle {\mathsf {RCOOH+R'OH\ {\xrightarrow[{}]{H^{+}}}\ RCOOR'+H_{2}O}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/b17f90d032efe6f8fa4e9b88affd0ca0b11f4947)