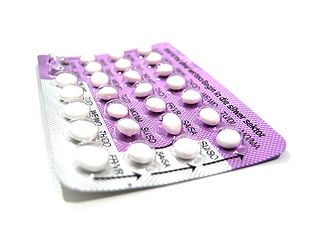
Этинилэстрадиол/этоногестрел
| Этинилэстрадиол/этоногестрел | |
|---|---|
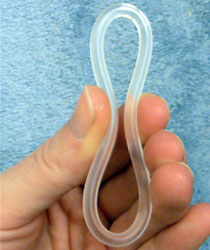 Сдавленное вагинальное кольцо «НоваРинг» | |
| Химическое соединение | |
| PubChem | 9960701 |
| Состав | |
| |
| Классификация | |
| Фармакол. группа | Эстрогены, гестагены; их гомологи и антагонисты в комбинациях |
| АТХ | G02BB01 |
Этинилэстрадиол/этоногестрел, выпускаемый под торговым наименованием «НоваРинг» (англ. NuvaRing) и другими, — интравагинальный контрацептив, вагинальное кольцо с комбинацией эстрогена и гестагена[англ.]. «НоваРинг» выпускает фармкомпания Merck (ранее Schering-Plough, ранее Organon). Зарегистрирован как лекарственное средство в 2001 году.
Состав и форма выпуска
Гибкое кольцо из гипоаллергенного этинилвинилацетата вводится во влагалище и ежедневно высвобождает 15 мкг этинилэстрадиола и 120 мкг этоногестрела[англ.] (первичный активный метаболит высокоселективного прогестагена дезогестрела) в течение 21 дня с перерывом в 7 дней[1].
Влагалищный путь введения гормонов обеспечивает стабильный гормональный фон без пиков и падений в течение дня[2], что даёт более регулярный цикл с меньшим количеством межменструальных выделений, по сравнению даже с таблетками, содержащими 15 мкг этинилэстрадиола. Влагалищный путь введения обеспечивает конфиденциальность метода[2].
- этоногестрел 11,7 мг
- этинилэстрадиол 2,7 мг
- другие ингредиенты: этилена винилацетата сополимер (28 % — винилацетат); этилена винилацетата сополимер (9 % — винилацетат); магния стеарат; вода очищенная.
Механизм действия
Как и все комбинированные гормональные контрацептивы, NuvaRing работает в основном путём предотвращения овуляции. В профинасированных производителем исследованиях, опубликованных до 2004 года, также утверждалось, что «НоваРинг» способствует сгущению слизи и следовательно снижает риск возникновения инфекционных заболеваний[3].
Побочные эффекты
Наиболее частыми побочными эффектами были: головная боль (6,6 %), тошнота (2,8 %), вагинит (0,6 %) и набор веса (4,9 %). В инструкции к кольцу описаны все возможные побочные эффекты.
В исследовании[4] было показано, что возможно применение вагинальных колец повышает риск тромбоза вен в 6,5 раз по сравнению с теми, кто не пользуется гормональными средствами контрацепции и в 1,9 раз по сравнению с женщинами, применяющими пероральные гормональные контрацептивы.
Противопоказания
Противопоказания к применению НоваРинга аналогичны противопоказаниям для других комбинированных оральных контрацептивов:
- Тромбоз в настоящее время и в анамнезе
- Тяжёлые заболевания печени
- Мигрень, сопровождающаяся очаговой неврологической симптоматикой
- Гормонзависимая опухоль или подозрение на неё
- Аллергия к любому из компонентов препарата
- Влагалищные кровотечения неясной этиологии
- Опущение половых органов
Примечания
- ↑ Свод практических рекомендация по применению средств контрацепции — второе издание и обновление 2008 г. Дата обращения: 23 марта 2012. Архивировано 19 марта 2012 года.
- ↑ 1 2 Руководство по контрацепции /под ред. Прилепской В. Н., 2006. ISBN 5-98322-192-2. Стр. 141—148.
- ↑ Медицинские критерии приемлемости для использования методов. Третье издание. ВОЗ,2004. Дата обращения: 16 июля 2010. Архивировано 26 марта 2010 года.
- ↑ Lidegaard, Øjvin; Øjvind Lidegaard, Lars Hougaard Nielsen, Charlotte Wessel Skovlund, and Ellen Løkkegaard. Venous thrombosis in users of non-oral hormonal contraception: follow-up study, Denmark 2001-10 (англ.) // BMJ : journal. — 2012. — May (vol. 344). — P. 1—9. — doi:10.1136/bmj.e2990. — PMID 22577198. Архивировано 29 октября 2013 года.
Литература
- Руководство по контрацепции /под ред. Прилепской В. Н., 2006. ISBN 5-98322-192-2. Стр. 141—148.
Ссылки
- Сайт Энциклопедии лекарств РЛС (rlsnet.ru). Описание препарата НоваРинг.
- Русскоязычный сайт производителя НоваРинга https://web.archive.org/web/20100328021515/http://www.surprizovnet.ru/choosecontraceptive/oneformonth/Default.aspx
- Свод практических рекомендаций по применению средств контрацепции/ВОЗ, 2005 http://www.who.int/making_pregnancy_safer/documents/9241562846index/ru/index.html
- Медицинские критерии приемлемости использования методов контрацепции. — ВОЗ,2004. http://whqlibdoc.who.int/publications/2004/9241562668_rus.pdf