
Ферме́нты, или энзи́мы , — обычно сложные белковые соединения, РНК (рибозимы) или их комплексы, ускоряющие химические реакции в живых системах. Каждый фермент, свернутый в определённую структуру, ускоряет соответствующую химическую реакцию: реагенты в такой реакции называются субстратами, а получающиеся вещества — продуктами. Ферменты специфичны к субстратам: АТФ-аза катализирует расщепление только АТФ, а киназа фосфорилазы фосфорилирует только фосфорилазу.
Трансфера́зы (КФ2) — отдельный класс ферментов, катализирующих перенос функциональных групп и молекулярных остатков от одной молекулы к другой. Широко распространены в растительных и животных организмах, участвуют в превращениях углеводов, липидов, нуклеиновых и аминокислот.

Аскорби́новая кислота́ (от др.-греч. ἀ «не-» + лат. scorbutus «цинга») — органическое соединение с формулой C6H8O6, является одним из основных веществ в человеческом рационе, которое необходимо для нормального функционирования соединительной и костной ткани. Выполняет биологические функции восстановителя и кофермента некоторых метаболических процессов, является антиоксидантом.

Глутаматдегидрогена́за, также L-глутамат: NAD-оксидоредуктаза — фермент, из семейства оксидоредуктаз аминокислот, катализирующий обратимую реакцию превращения L-глутаминовой кислоты в α-кетоглутаровую. Фермент присутствует как в прокариотических организмах, так и в эукариотических митохондриях.

Никотинамидадениндинуклеоти́д — кофермент, имеющийся во всех живых клетках. NAD представляет собой динуклеотид и состоит из двух нуклеотидов, соединённых своими фосфатными группами. Один из нуклеотидов в качестве азотистого основания содержит аденин, другой — никотинамид.
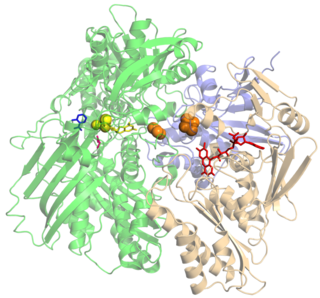
Ксантиноксидаза (ксантиноксидоредуктаза, КФ 1.17.3.2) — молибден-содержащая оксидоредуктаза, фермент, катализирующий окисление гипоксантина в ксантин и ксантина в мочевую кислоту:
- гипоксантин + O2 + H2O <-> ксантин + H2O2
- ксантин + O2 + H2O <-> мочевая кислота + H2O2
Оксидоредукта́зы (КФ1) — отдельный класс ферментов, катализирующих лежащие в основе биологического окисления реакции, сопровождающиеся переносом электронов с одной молекулы на другую.
Дыхательная цепь переноса электронов, также электрон-транспортная цепь (сокр. ЭТЦ, англ. ETC, Electron transport chain) — система трансмембранных белков и переносчиков электронов, необходимых для поддержания энергетического баланса. ЭТЦ поддерживает баланс за счёт переноса электронов и протонов из НАД∙Н и ФАДН2 в акцептор электронов. В случае аэробного дыхания акцептором может быть молекулярный кислород (О2). В случае анаэробного дыхания акцептором могут быть NO3−, NO2−, Fe3+, фумарат, диметилсульфоксид, сера, SO42−, CO2 и т. д. ЭТЦ у прокариот локализована в ЦПМ, у эукариот — на внутренней мембране митохондрий. Переносчики электронов расположены в порядке уменьшения сродства к электрону, то есть по своему окислительно-восстановительному потенциалу, где у акцептора самое сильное сродство к электрону. Поэтому транспорт электрона на всём протяжении цепи протекает самопроизвольно с выделением энергии. Выделение энергии в межмембранное пространство при переносе электронов происходит ступенчато, в виде протона (H+). Протоны из межмембранного пространства попадают в протонную помпу, где наводят протонный потенциал. Протонный потенциал преобразуется АТФ-синтазой в энергию химических связей АТФ. Сопряжённая работа ЭТЦ и АТФ-синтазы носит название окислительного фосфорилирования.

Окисли́тельное фосфорили́рование — метаболический путь, при котором энергия, образовавшаяся при окислении питательных веществ, запасается в митохондриях клеток в виде АТФ. Хотя различные формы жизни на Земле используют разные питательные вещества, АТФ является универсальным соединением, в котором запасается энергия, необходимая для других метаболических процессов. Почти все аэробные организмы осуществляют окислительное фосфорилирование. Вероятно, широкому распространению этого метаболического пути способствовала его высокая энергетическая эффективность по сравнению с анаэробным брожением.

Цитохром-c-оксида́за (цитохромоксидаза) или цитохром-c-кислород:оксидоредуктаза, также известная как цитохром aa3 и комплекс IV — терминальная оксидаза аэробной дыхательной цепи переноса электронов, которая катализирует перенос электронов с цитохрома с на кислород с образованием воды. Цитохромоксидаза присутствует во внутренней мембране митохондрий всех эукариот, где её принято называть комплекс IV, а также в клеточной мембране многих аэробных бактерий.

НАДФH-оксидаза, или NADPH-оксидаза (NOX) — клеточный мембрано-связанный мультимолекулярный ферментный комплекс, локализующийся на плазматической мембране и в некоторых органеллах. Особенно обогащены этим ферментом фагоцитарные клетки, такие как макрофаги. Эти оксидазы участвуют в клеточной противомикробной защитной системе, а также в клеточной пролиферации, дифференцировке и регуляции экспрессии генов. Существует целая группа НАДФH-оксидаз, которые различаются по составу субъединиц, клеточной специфичности, регуляции и другим параметрам.
NADPH-оксидаза 4 (NOX4) — тип NADPH-оксидазы, клеточной мембранной оксидоредуктазы, образующей супероксидный радикал при переносе электрона с NADPH на кислород. В отличие от других, форм, требующих для активации образования мультибелкового комплекса с несколькими цитозольными белками, является конститутивно активной.

Аскорбат натрия — натриевая соль аскорбиновой кислоты. Представляет собой твёрдый кристаллический порошок белого или желтоватого цвета без запаха. В природе встречается в цитрусовых и многих овощах в виде l-(+)-энантиомера.
Оксиредуктазы — ферменты, катализирующие реакции окисления и восстановления с субстратами A и B. Среди основных выделяют: оксидазы, анаэробные дегидрогеназы. В 1976 году все ферменты были разделены на классы в соответствие с катализируемыми реакциями.

Лакказа — фермент, относящийся к оксидазам. Катализирует ряд реакций окисления ароматических и неароматических соединений. Содержит медь, связанную имидазольными группами гистидина. Встречается во многих микроорганизмах, грибах, растениях. Лакказы из различных организмов могут существенно отличаться по своим свойствам.

Ацил-КоА-дегидрогеназа жирных кислот с очень длинной цепью — один из нескольких митохондриальных ферментов из семейства ацил-КоА-дегидрогеназы. Систематическое название Ацил-КоА-дегидрогеназы жирных кислот с очень длинной цепью: Электрон-переносящий флавопротеин 2,3-оксидоредуктаза. Относится к FАD-зависимым ферментам, где простетической группой служит FAD. Ген, кодирующий фермент у человека — ACADVL локализован на 17-ой хромосоме.

Митохондриа́льный ма́трикс или просто ма́трикс — ограниченное внутренней мембраной пространство, расположенное внутри митохондрий. Слово «матрикс» происходит из того, что эта среда является намного более вязкой по сравнению с более водянистой цитоплазмой. В состав матрикса входит множество веществ, включая ферменты, митохондриальную ДНК (кольцевая), рибосомы, малые органические молекулы, нуклеотидные коферменты и неорганические ионы. Ферменты матрикса содействуют реакциям биохимических процессов, в ходе которых синтезируется АТФ, таких как цикл трикарбоновых кислот, окислительное фосфорилирование, окисление пирувата и бета-окисление жирных кислот.
Транслоказы — отдельный класс ферментов, катализирующих перенос ионов или молекул через мембраны или их разделение в мембранах. Этот класс ферментов сформировался из ранее принадлежащих другим классам ферментов.

L-гулонолактоноксидаза — фермент из группы оксидоредуктаз, который вырабатывает витамин С, но не функционирует у обезьян, морских свинок, костистых рыб, некоторых семейств летучих мышей и воробьиных. Фермент катализирует последнюю стадию биосинтеза аскорбиновой кислоты.

Дегидроаскорбиновая кислота (ДГК) представляет собой окисленную форму аскорбиновой кислоты. Он активно импортируется в эндоплазматический ретикулум клеток через переносчики глюкозы. Он задерживается там путем восстановления обратно до аскорбата глутатионом и другими тиолами. Свободный химический радикал семидегидроаскорбиновой кислоты (SDA) также принадлежит к группе окисленных аскорбиновых кислот.















