
Ма́рганец — химический элемент 7-й группы четвёртого периода периодической системы химических элементов Д. И. Менделеева с атомным номером 25.

Окси́д (синонимы: о́кисел, о́кись) — бинарное соединение химического элемента с кислородом в степени окисления −2, в котором сам кислород связан только с менее электроотрицательным элементом. Химический элемент кислород по электроотрицательности второй после фтора, поэтому к оксидам относятся почти все соединения химических элементов с кислородом. К исключениям относятся, например, дифторид кислорода OF2.
Неоргани́ческие (минера́льные) кисло́ты — неорганические вещества, обладающие комплексом физико-химических свойств, которые присущи кислотам. Вещества кислотной природы известны для большинства химических элементов за исключением щелочных и щёлочноземельных металлов.

Азо́тная кислота́ (химическая формула — HNO3; лат. Acidum nitricum, azoticum) — сильная химическая неорганическая кислота, отвечающая высшей степени окисления азота (+5).

Анили́н (аминобензол, фениламин) — органическое соединение с формулой C6H5NH2, простейший ароматический амин. Представляет собой бесцветную маслянистую жидкость с характерным запахом, немного плотнее воды и плохо в ней растворим, хорошо растворяется в органических растворителях. На воздухе быстро окисляется и приобретает красно-бурую окраску. Ядовит. Название «анилин» происходит от названия одного из растений, содержащих индиго — Indigofera anil (современное международное название растения — Indigofera suffruticosa).

Гидроксилами́н (аминóл, гидроксиами́н, NH2OH) — неорганическое соединение, бесцветные кристаллы, легко растворимые в воде с образованием гидрата NH2ОН·Н2О.
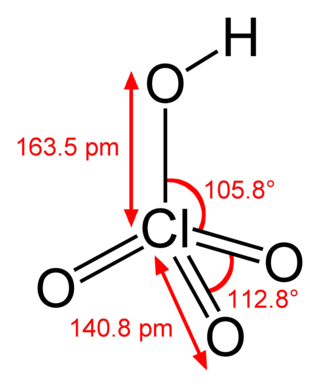
Хло́рная кислота́ (хим. формула — HClO4) — сильная одноосновная кислота.

Адипи́новая кислота́  — двухосновная предельная карбоновая кислота. Обладает всеми химическими свойствами, характерными для карбоновых кислот.
— двухосновная предельная карбоновая кислота. Обладает всеми химическими свойствами, характерными для карбоновых кислот.
Окси́ды азо́та — неорганические бинарные соединения азота с кислородом.

Азо́тистая кислота HNO2 — слабая одноосновная кислота, существует только в разбавленных водных растворах, окрашенных в слабый голубой цвет, и в газовой фазе. Кислота весьма токсична (в больших концентрациях). Соли азотистой кислоты называются нитритами или азотистокислыми. Нитриты гораздо более устойчивы, чем HNO2, многие из них - токсичны, канцерогенны.

Окси́д азо́та(V), химическая формула  — высший оксид азота.
— высший оксид азота.

Оксид азота(III) (азотистый ангидрид, сесквиоксид азота) N2O3 — жидкость синего цвета (при н. у.), бесцветный ядовитый газ (при стандартных условиях), в твёрдом виде — синеватого цвета. Устойчив только при температурах ниже −4 °C. Без примесей NO2 и NO азотистый ангидрид (O=N—O—N=O) существует только в твёрдом виде.

Оксид азота (IV) (диоксид азота, двуокись азота) NO2 — бинарное неорганическое соединение азота с кислородом. Представляет собой ядовитый газ красно-бурого цвета с резким неприятным запахом или желтоватую жидкость.

Нитриты — соли азотистой кислоты HNO2, например, нитрит натрия NaNO2, нитрит кальция Ca(NO2)2. Известны нитриты щелочных, щелочноземельных, 3d-металлов, а также нитриты свинца и серебра.

Хлорид нитрозила — красный газ, токсичен, с удушливым запахом. Обычно наблюдается как продукт процесса разложения царской водки — смеси соляной и азотной кислот. Из оксид-галогенидов азота известны также фторид нитрозила NOF и бромид нитрозила NOBr. В ряду NOF—NOCl—NOBr устойчивость оксогалогенидов уменьшается, а NOI не удалось получить.
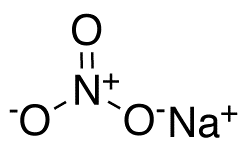
Нитра́т на́трия (азотноки́слый на́трий, натриевая селитра, чилийская селитра, натронная селитра) — натриевая соль азотной кислоты с формулой NaNO3. Бесцветные прозрачные кристаллы с ромбоэдрической или тригональной кристаллической решеткой без запаха. Вкус — резкий солёный. Применяется очень широко и является незаменимым в промышленности соединением.

Аминосульфоновая кислота (Сульфаминовая кислота, моноамид серной кислоты, амидосерная кислота) — кислота, формула которой NH2SO2OH (также NH2SO3H). Производные этой кислоты называют сульфаматами.

Нитрат бериллия — химическое соединение с формулой Be(NO3)2. Представляет собой среднюю соль бериллия и азотной кислоты.
Соединение существует в виде кристаллогидратов различного состава, безводный нитрат не выделен. Из водных растворов при добавлении концентрированной HNO3 выделяется обычно тетрагидрат Be(NO3)2•4H2O (или [Be(H2O)4](NO3)2), кристаллы которого расплываются на воздухе. Известны также тригидрат Be(NO3)2•3H2O (кристаллизующийся, в частности, из растворов, содержащих 54 % HNO3) и дигидрат Be(NO3)2•2Н20.

Изопропилнитрит — нерастворимая в воде желтоватая маслянистая жидкость.

Нитра́т мочеви́ны — азотнокислая соль мочевины, образующаяся при реакции мочевины и азотной кислоты. Обладает взрывчатыми свойствами.




























