
Со́ли — сложные вещества, состоящие из катионов металлов и анионов кислотных остатков. ИЮПАК определяет соли как химические соединения, состоящие из катионов и анионов. Есть ещё одно определение: солями называют вещества, которые могут быть получены при взаимодействии кислот и оснований с выделением воды.
Неоргани́ческая хи́мия — раздел химии, связанный с изучением строения, реакционной способности и свойств всех химических элементов и их неорганических соединений. Эта область охватывает все химические соединения, за исключением органических веществ. Различия между органическими и неорганическими соединениями, содержащими углерод, являются по некоторым представлениям произвольными. Неорганическая химия изучает химические элементы и образуемые ими простые и сложные вещества. Обеспечивает создание материалов новейшей техники. Число известных на 2013 г. неорганических веществ приближается к 500 тысячам.
Сте́пень окисле́ния — вспомогательная условная величина для записи процессов окисления, восстановления и окислительно-восстановительных реакций. Она указывает на состояние окисления отдельного атома молекулы и представляет собой лишь удобный метод учёта переноса электронов: она не является истинным зарядом атома в молекуле.

Аналити́ческая хи́мия — наука, развивающая теоретические основы химического анализа веществ и материалов и разрабатывающая методы идентификации, обнаружения, разделения и определения химических элементов и их соединений, а также методы установления химического состава веществ. Проведение химического анализа в настоящее время заключается в получении информации о составе и природе вещества.
Кисло́ты — химические соединения, способные отдавать катион водорода, либо соединения, способные принимать электронную пару с образованием ковалентной связи.
Неоргани́ческие (минера́льные) кисло́ты — неорганические вещества, обладающие комплексом физико-химических свойств, которые присущи кислотам. Вещества кислотной природы известны для большинства химических элементов за исключением щелочных и щёлочноземельных металлов.

Ио́н — атом или группа из нескольких атомов, которая имеет электрический заряд.
Катио́н — положительно заряженный ион. Характеризуется величиной положительного электрического заряда: например, NH4+ — однозарядный катион аммония, Ca2+ — двухзарядный катион кальция. В электрическом поле, катионы притягиваются к отрицательному электроду — катоду.
Гидрокси́ды — неорганические соединения, содержащие гидроксильную группу  . Известны гидроксиды почти всех химических элементов; некоторые из них встречаются в природе в виде минералов.
. Известны гидроксиды почти всех химических элементов; некоторые из них встречаются в природе в виде минералов.
Хими́ческий исто́чник то́ка — источник тока, в котором энергия протекающих в нём химических реакций непосредственно превращается в электрическую энергию.

Ионная связь — сильная химическая связь между атомами существенно отличающимися между собой по электроотрицательности.
Амфоте́рность — способность некоторых химических веществ и соединений проявлять в зависимости от условий как кислотные, так и осно́вные свойства.

Иониты — твёрдые нерастворимые вещества, способные обменивать свои ионы на ионы из окружающего их раствора. Обычно это синтетические органические смолы, имеющие кислотные или щелочные группы. Иониты разделяются на катиониты, поглощающие катионы, аниониты, поглощающие анионы, и амфотерные иониты, обладающие обоими этими свойствами. Широко применяются иониты для опреснения вод, в аналитической химии для разделения веществ методом хроматографии, в химической технологии. Иониты распространены в природе, в частности, в почве содержатся катиониты, которые предохраняют катионы необходимых растениям элементов от вымывания водой и обменивают их на ионы водорода выделяемой растениями кислоты, таким образом способствуя питанию растений. В зависимости от природы матрицы различают неорганические и органические иониты.

Ко́мплексные соедине́ния или координацио́нные соедине́ния — это соединения, которые образуются в результате присоединения к данному иону, называемому комплексообразователем, нейтральных молекул или других ионов, называемых лигандами. Теория комплексных соединений была предложена в 1893 г. А. Вернером.

Цвиттер-ион — молекула, которая, являясь в целом электронейтральной, в своей структуре имеет функциональные группы, несущие как отрицательный, так и положительный заряды. Их иногда называют внутримолекулярными солями и, иногда, (ошибочно) ионными диполярными соединениями. Некоторые химики относят к цвиттер-ионам лишь соединения с зарядами на несоседних атомах, поскольку существуют также соединения с зарядами на соседних атомах. Цвиттер-ионные соединения высокополярны и поэтому, как правило, обладают хорошей растворимостью в полярных растворителях и слабой — в большинстве органических неполярных растворителей.
Тео́рии кисло́т и основа́ний — совокупность фундаментальных физико-химических представлений, описывающих природу и свойства кислот и оснований. Все они вводят определения кислот и оснований — двух классов веществ, реагирующих между собой. Задача теории — предсказание продуктов реакции между кислотой и основанием и возможности её протекания, для чего используются количественные характеристики силы кислоты и основания. Различия между теориями лежат в определениях кислот и оснований, характеристики их силы и, как следствие — в правилах предсказания продуктов реакции между ними. Все они имеют свою область применимости, каковые области частично пересекаются.
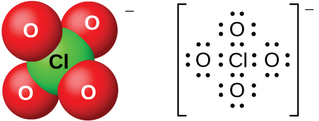
Перхлора́ты — группа химических соединений, соли или сложные эфиры хлорной кислоты. Соли металлов, неметаллов, гидразина, гидроксиламина и аммония относятся к неорганическим производным хлорной кислоты, а эфиры и соли органических соединений — к органическим производным хлорной кислоты.
Аммо́ниевые соедине́ния содержат положительно заряженный атом азота, ковалентно связанный с органическими радикалами и (или) водородом, и ионно — с анионом. Простейшие неорганические аммониевые соединения — гидрат аммиака и соли аммония. Аммониевые соединения входят в большой класс ониевых соединений.
Амфотерные (амфолитные) поверхностно-активные вещества (ПАВ) (англ. ampholitic surfactant или англ. zwitterionic surfactant) — поверхностно-активные вещества, способные быть донорами или акцепторами протона в зависимости от значения pH раствора. Представляют собой соединения, которые в водных растворах в зависимости от значения рН среды по-разному ионизируются и действуют — в кислом растворе проявляют свойства катионных ПАВ, а в щелочном растворе — анионных ПАВ. Примером амфотерного сурфактанта может служить алкилбетаин RCH[N+(CH3)3]COO-. К амфотерным сурфактантам относятся также природные полимеры: белки и нуклеиновые кислоты.

Сульфа́ты — соли серной кислоты H2SO4, а также (в органической химии) сложные эфиры серной кислоты —диалкилсульфаты R−O−SO2−O−R и алкилсульфаты Н−O−SO2−O−R.









