
Изолейцин (сокращённо Ile или I; 2-амино-3-метилпентановая кислота) — это алифатическая α-аминокислота, имеющая химическую формулу HO2CCH(NH2)CH(CH3)CH2CH3 и входящая в состав всех природных белков. Является незаменимой аминокислотой, что означает, что изолейцин не может синтезироваться в организме человека и должен поступать в него с пищей. Участвует в энергетическом обмене. При недостаточности ферментов, катализирующих декарбоксилирование изолейцина, возникает кетоацидоз.
Биохи́мия — наука о химическом составе живых клеток и организмов, а также о лежащих в основе их жизнедеятельности химических процессах. Термин «биохимия» эпизодически употреблялся с середины XIX века, в классическом смысле он был предложен и введён в научную среду в 1903 году немецким химиком Карлом Нейбергом.

Ци́кл трикарбо́новых кисло́т (сокр. ЦТК, цикл Кре́бса, цитра́тный цикл, цикл лимо́нной кислоты́) — центральная часть общего пути катаболизма, циклический биохимический процесс, в ходе которого ацетильные остатки (СН3СО-) окисляются до диоксида углерода (CO2). При этом за один цикл образуется 2 молекулы CO2, 3 НАДН, 1 ФАДH2 и 1 ГТФ (или АТФ). Электроны, находящиеся на НАДН и ФАДH2, в дальнейшем переносятся на дыхательную цепь, где в ходе реакций окислительного фосфорилирования образуется АТФ.
Аммонификáция — процесс разложения азотсодержащих органических соединений в результате их ферментативного гидролиза под действием аммонифицирующих микроорганизмов с образованием токсичных для человека конечных продуктов — аммиака, сероводорода, а также первичных и вторичных аминов при неполной минерализации продуктов разложения:
- трупных ядов, например: путресцин и кадаверин;
- ароматических соединений, например: скатол, индол — образуются в результате дезаминирования и декарбоксилирования аминокислоты триптофана;
- серосодержащих аминокислот, например: цистеина, цистина и метионина, — приводит к выделению сероводорода, тиолов, диметилсульфоксида.

Фенилалани́н — ароматическая альфа-аминокислота. Существует в двух оптически изомерных формах l и d и в виде рацемата. По химическому строению соединение можно представить как аминокислоту аланин, в которой один из атомов водорода замещён фенильной группой.

Тирози́н — ароматическая альфа-аминокислота. Существует в двух оптически изомерных формах — L и D и в виде рацемата (DL). По строению соединение отличается от аминокислоты фенилаланина наличием фенольной гидроксильной группы в пара-положении бензольного кольца.
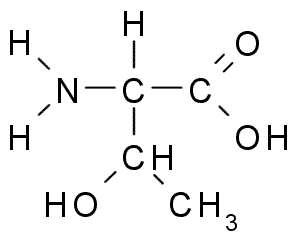
Треони́н — гидроксиаминокислота; молекула содержит два хиральных центра, что обусловливает существование четырёх оптических изомеров: L- и D-треонина (3D), а также L- и D-аллотреонина (3L).

Сери́н — гидроксиаминокислота, существует в виде двух оптических изомеров — L и D.

Гистиди́н — гетероциклическая альфа-аминокислота, одна из 20 протеиногенных аминокислот. По современным представлениям также является незаменимой кислотой как для детей, так и для взрослых.
Диффузная эндокринная система — отдел эндокринной системы, представленный рассеянными в различных органах эндокринными клетками (апудоцитами), продуцирующими агландулярные гормоны. ДЭС — эволюционно древнее и крупнейшее звено эндокринной системы животных и человека. Клетки ДЭС получают информацию из внешней и внутренней среды организма. В ответ на неё они реагируют выделением биогенных аминов и пептидных гормонов.

Путресци́н (от лат. puter — гнилой, гниющий), также 1,4-диаминобутан (ИЮПАК) — органическое соединение, с формулой H2N(CH2)4NH2; относится к группе биогенных аминов.
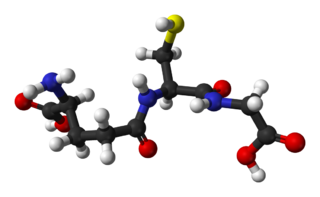
Глутатион — это трипептид γ-глутамилцистеинилглицин. Глутатион содержит необычную пептидную связь между аминогруппой цистеина и карбоксильной группой боковой цепи глутамата. Значение глутатиона в клетке определяется его антиоксидантными свойствами. Фактически глутатион не только защищает клетку от токсичных свободных радикалов, но и в целом определяет окислительно-восстановительные характеристики внутриклеточной среды.
Птомаи́ны, или тру́пные я́ды — термин, использовавшийся для обозначения биогенных диаминов, получающихся в результате гнилостных процессов — частичного разложения белка и декарбоксилирования его аминокислот. Основные птомаины — путресцин и кадаверин, а также спермидин, спермин и нейрин. Имеют характерный отвратительный «сладковатый» запах. Однако острая токсичность птомаинов сравнительно невелика: путресцин — 2000 мг/кг, кадаверин — 2000 мг/кг, спермидин и спермин — 600 мг/кг; токсичность нейрина выше — 30 мг/кг.
Декарбоксилирование аминокислот — процесс отщепления карбоксильной группы аминокислот в виде CO2.

Тирамин, β-(n-оксифенил)-этиламин, HO-C6H4-CH2-CH2-NH2, органическое вещество из группы биогенных аминов. Тирамин найден в спорынье, гниющих тканях, сыре. Отсюда и его название (от греч. tyros – сыр). Физиологически активен (в связи с сосудосуживающим действием повышает кровяное давление, влияет на процессы возбуждения и торможения в нервной системе) и токсичен. Образуется из аминокислоты тирозина под действием бактериальных декарбоксилаз, в частности при гнилостных процессах в кишечнике млекопитающих животных и человека. Обезвреживание избыточного тирамина в живом организме осуществляется в результате его окисления ферментом моноаминоксидазой (МАО).

Витамин B6, или адермин — собирательное название производных 3-гидрокси-2-метилпиридинов, обладающих биологической активностью пиридоксина — собственно пиридоксин, пиридоксаль, пиридоксамин, а также их фосфаты, среди которых наиболее важен пиридоксальфосфат.
Биомолекулы — это органические соединения, которые синтезируются живыми организмами. В состав биомолекул включают белки, полисахариды, нуклеиновые кислоты, а также более мелкие компоненты обмена веществ. Как правило, биомолекулы состоят из атомов углерода, водорода, азота, кислорода, фосфора и серы. Другие элементы входят в состав биологически значимых веществ значительно реже.
Апудоци́ты (APUD-клетки) — диффузно расположенные секретирующие клетки, способные поглощать аминокислоты-предшественницы и производить из них активные амины и/или низкомолекулярные пептиды с помощью реакции декарбоксилирования.
Вторичные метаболиты — органические вещества, синтезируемые организмом, но не участвующие в росте, развитии или репродукции.
Непротеиногенные аминокислоты — аминокислоты, которые не участвуют в биосинтезе белка. Непротеиногенные аминокислоты часто не входят в состав непатогенных и «нормальных» белков человека, не следует их путать с нестандартными аминокислотами, которые образуются непосредственно при синтезе белка или в результате различных ковалентных модификаций молекулярных структур протеиногенных (кодируемых) аминокислот в составе белков, например, гидроксипролина, десмозина или аллизина. Однако они могут входить в состав некоторых небольших молекул или пептидов, синтез которых является нерибосомальным. Химически синтезированные аминокислоты можно назвать неприродными аминокислотами. Многие из них являются токсинами и ингибиторами ферментов разнообразных метаболических реакций. Известно свыше 400 природных аминокислот и, возможно, больше тысячи их комбинаций. Неприродные аминокислоты могут быть синтетически получены из их нативных аналогов с помощью модификаций, таких как алкилирование аминогруппы, замещение боковой цепи, циклизация за счёт удлинения структурных связей и изостерических замен в аминокислотном остове.










