Гидроксиды рутения
Гидроксиды рутения — неорганические соединения рутения, содержащие гидроксильные группы –OH:
- Гидроксид рутения(II) Ru(OH)2
- Гидроксид рутения(III) Ru(OH)3
- Гидроксид рутения(IV) Ru(OH)4
Гидроксиды рутения — неорганические соединения рутения, содержащие гидроксильные группы –OH:

Гидрокси́д ка́лия — неорганическое соединение с химической формулой KOH. Бесцветные, очень гигроскопичные кристаллы, но гигроскопичность меньше, чем у гидроксида натрия. Водные растворы KOH имеют сильнощелочную реакцию. Получают электролизом растворов хлорида калия (KCl), применяют в производстве жидких мыльных средств, для получения различных соединений калия.

Гидрокси́д на́трия — неорганическое химическое соединение, являющееся самой распространённой щёлочью. В год в мире производится и потребляется около 57 миллионов тонн едкого натра.
Щёлочи — гидроксиды щелочных, щелочноземельных металлов и таллия. К щелочам относятся хорошо растворимые в воде основания. При электролитической диссоциации щёлочи образуют анионы OH− и катион металла.
Гидрокси́ды — неорганические соединения, содержащие гидроксильную группу 
Перехо́дные мета́ллы (перехо́дные элеме́нты) — элементы побочных подгрупп Периодической системы химических элементов Д. И. Менделеева, в атомах которых появляются электроны на d- и f-орбиталях. В общем виде электронное строение переходных элементов можно представить следующим образом: 

Гидрокси́ды ме́ди — название ряда химических соединений меди.
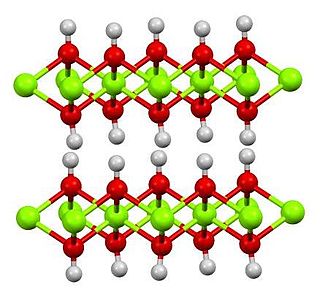
Гидрокси́д ма́гния — неорганическое вещество, осно́вный гидроксид металла магния, имеет формулу Mg(OH)2. Слабое малорастворимое основание.
Гидрокси́ды желе́за — название ряда химических соединений железа, амфотерных гидроксидов.

Гидрокси́д бери́ллия — амфотерный гидроксид, имеющий химическую формулу Be(OH)2. При стандартных условиях представляет собой гелеобразное белое вещество, практически нерастворимое в воде. Вместе с тем, он хорошо растворяется в разбавленных минеральных кислотах. Гидроксид бериллия получают в виде геля при обработке солей бериллия гидроксидами щелочных металлов или гидролизом нитрида или фосфида бериллия.

Гидроксид марганца(II) — неорганическое соединение, гидроксид металла марганца с формулой Mn(OH)2, серые кристаллы, не растворимые в воде.
Гидроксид рутения(II) — неорганическое соединение, гидроксид металла рутения с формулой Ru(OH)2, коричневый осадок, не растворяется в воде.
Гидроксид рутения(III) — неорганическое соединение, гидроксид металла рутения с формулой Ru(OH)3, чёрный осадок, не растворяется в воде.

Бромид рутения(III) — неорганическое соединение, соль металла рутения и бромистоводородной кислоты с формулой RuBr3, чёрные кристаллы, растворяется в холодной воде.

Иодид рутения(III) — неорганическое соединение, соль металла рутения и иодистоводородной кислоты с формулой RuI3, чёрные кристаллы.
Гидроксид-оксид европия(III) — неорганическое соединение, окись-гидроксид европия с формулой EuO(OH), белые кристаллы, не растворяется в воде.
Гидроксид иридия(III) — неорганическое соединение, гидроксид иридия с формулой Ir(OH)3, порошок, цвета от жёлто-зелёного до синевато-чёрного, не растворяется в воде.
Гидроксид иридия(IV) — неорганическое соединение, гидроксид иридия с формулой Ir(OH)4 (IrO2·2H2O), синевато-чёрный порошок, не растворяется в воде.
Гидроксид-оксид лютеция — неорганическое соединение, окись-гидроокись лютеция с формулой LuO(OH), кристаллы, не растворяется в воде.
Оксид рутения(III) — неорганическое соединение, оксид металла рутения с формулой Ru2O3, чёрные кристаллы.
Гидроксид рутения(IV) — неорганическое соединение, гидроксид металла рутения с формулой Ru(OH)4, чёрное аморфное вещество, не растворяется в воде.