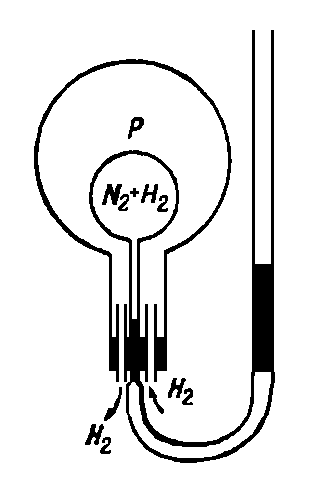Абсо́рбция — поглощение сорбата всем объёмом сорбента. Является частным случаем сорбции.
Моля́рный объём Vm — отношение объёма вещества к его количеству, численно равен объёму одного моля вещества. Термин «молярный объём» может быть применён к простым веществам, химическим соединениям и смесям. В общем случае он зависит от температуры, давления и агрегатного состояния вещества. Молярный объём также можно получить делением молярной массы M вещества на его плотность ρ: таким образом, Vm = V/n = M/ρ. Молярный объём характеризует плотность упаковки молекул в данном веществе. Для простых веществ иногда используется термин атомный объём.

Газ, или газообра́зное состоя́ние — одно из четырёх основных агрегатных состояний вещества, характеризующееся очень слабыми связями между составляющими его частицами, а также их большой подвижностью. Частицы газа почти свободно и хаотически движутся в промежутках между столкновениями, во время которых происходит резкое изменение характера их движения.

Жи́дкость — вещество, находящееся в жидком агрегатном состоянии, занимающем промежуточное положение между твёрдым и газообразным состояниями.
Идеа́льный газ — теоретическая модель, широко применяемая для описания свойств и поведения реальных газов при умеренных давлениях и температурах. В этой модели, во-первых, предполагается, что составляющие газ частицы не взаимодействуют друг с другом, то есть их размеры пренебрежимо малы, поэтому в объёме, занятом идеальным газом, нет взаимных неупругих столкновений частиц. Частицы идеального газа претерпевают столкновения только со стенками сосуда. Второе предположение: между частицами газа нет дальнодействующего взаимодействия, например, электростатического или гравитационного. Дополнительное условие упругих столкновений между молекулами и стенками сосуда в рамках молекулярно-кинетической теории приводит к термодинамике идеального газа.

Кислоро́дное отравле́ние, гиперокси́я — отравление, которое в острой форме возникает вследствие дыхания кислородосодержащими газовыми смесями при повышенном давлении. Отравление может возникнуть и при обычном давлении в случае длительного вдыхания смеси, содержащей более 60% кислорода. Отравление кислородом возможно при использовании кислородных аппаратов, регенеративных аппаратов, при использовании для дыхания искусственных газовых смесей, во время проведения кислородной рекомпрессии, а также вследствие превышения лечебных доз в процессе оксигенобаротерапии. При отравлении кислородом развиваются нарушения функций центральной нервной системы, органов дыхания и кровообращения.

Джон Дáльтон (Дэлтон) — английский физик и химик, метеоролог, естествоиспытатель и создатель химического атомизма. В 1794 году впервые провёл исследования и описал дефект зрения, которым страдал сам, — цветовую слепоту, позже названную в его честь дальтонизмом; открыл закон парциальных давлений (1801), закон равномерного расширения газов при нагревании (1802), закон растворимости газов в жидкостях. Установил закон кратных отношений (1803), обнаружил явление полимеризации на примере этилена и бутилена, ввёл понятие «атомный вес», первым рассчитал атомные веса (массы) ряда элементов и составил первую таблицу их относительных атомных масс, заложив тем самым количественные основы для древней атомной теории строения вещества.
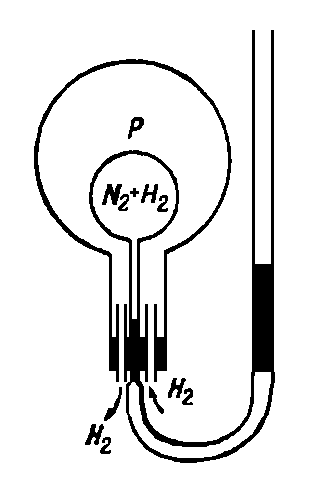
Парциа́льное давление — давление, оказываемое компонентом газовой смеси, при условии удаления других компонентов из занимаемого объёма, сохраняя этот объём и текущую температуру. Общее давление газовой смеси является суммой парциальных давлений её компонентов.

Зако́н де́йствующих масс устанавливает соотношение между массами реагирующих веществ в химических реакциях при равновесии, а также зависимость скорости химической реакции от концентрации исходных веществ. Закон действующих масс открыли в 1864—1867 годах норвежские ученые Като Гульдберг и Петер Вааге.
Акти́вность компонентов раствора — эффективная (кажущаяся) концентрация компонентов с учётом различных взаимодействий между ними в растворе, то есть с учётом отклонения поведения системы от модели идеального раствора.
Зако́ны Рау́ля — общее название открытых французским химиком Ф. М. Раулем в 1887 году количественных закономерностей, описывающих некоторые коллигативные свойства растворов.
Ректифика́ция — процесс разделения двойных или многокомпонентных смесей за счёт противоточного массообмена между паром и жидкостью. Ректификация — разделение жидких смесей на практически чистые компоненты, различающиеся температурами кипения, путём многократного частичного испарения жидкости и частичной конденсации паров.
Сорбция — поглощение твёрдым телом либо жидкостью различных веществ из окружающей среды. Поглощаемое вещество, находящееся в среде, называют сорбатом (сорбтивом), поглощающее твёрдое тело или жидкость — сорбентом.
Зако́н Ге́нри, Закон Генри — Дальтона — закон, по которому при постоянной температуре растворимость газа в данной жидкости прямо пропорциональна давлению этого газа над раствором. Закон пригоден лишь для идеальных растворов и невысоких давлений.
Уравне́ние Ван-дер-Ва́альса — уравнение, связывающее основные термодинамические величины в модели газа Ван-дер-Ваальса.
Законы Коновалова описывают процессы, протекающие в равновесных системах «жидкий раствор — пар» при различных температурах, давлениях и составах компонентов. Эти законы лежат в основе теории ректификации бинарных смесей.
Изохо́рный, или изохори́ческий проце́сс — термодинамический изопроцесс, который происходит при постоянном объёме. Для осуществления изохорного процесса в газе или жидкости достаточно нагревать или охлаждать вещество в сосуде неизменного объёма.
Конста́нта равнове́сия — величина, определяющая для данной химической реакции соотношение между термодинамическими активностями исходных веществ и продуктов в состоянии химического равновесия. Зная константу равновесия реакции, можно рассчитать равновесный состав реагирующей смеси, предельный выход продуктов, определить направление протекания реакции.

Закон Гей-Люссака — закон пропорциональной зависимости объёма газа от абсолютной температуры при постоянном давлении, названный в честь французского физика и химика Жозефа Луи Гей-Люссака, впервые опубликовавшего его в 1802 году.