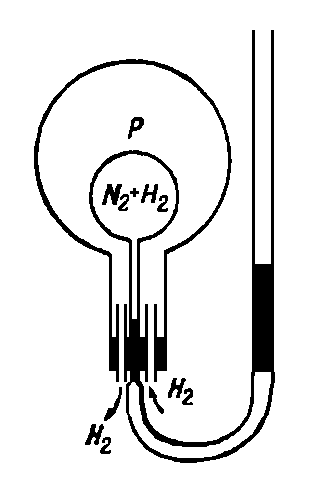Диокси́д углеро́да или двуо́кись углеро́да (также оксид углерода(IV), углеки́слый газ, у́гольный ангидри́д, углекислота́, формула — CO2) — химическое вещество, представляющее собой бинарное неорганическое соединение в форме кислотного оксида, молекула которого состоит из одного атома углерода и двух атомов кислорода.
Абсо́рбция — поглощение сорбата всем объёмом сорбента. Является частным случаем сорбции.

Раство́р — однородная (гомогенная) система, в состав которой входят молекулы двух или более типов, причём доля частиц каждого типа может непрерывно меняться в определённых пределах. От механической смеси раствор отличается однородностью, от химического соединения — непостоянством состава.

Азеотро́пная смесь — смесь двух или более жидкостей с таким составом, который не меняется при кипении, то есть составы равновесных жидкой и паровой фаз совпадают.

Дистилля́ция — процесс испарения жидкости с последующим охлаждением и конденсацией паров, который используется, прежде всего, для разделения жидких смесей и очистки выделяемых веществ. Основан на различии в температурах кипения компонентов смеси. В зависимости от состава разделяемой смеси и целей процесса, продуктами дистилляции могут быть как дистиллят, обогащённый более летучими (низкокипящими) компонентами, так и неотогнанный (кубовый) остаток, содержащий менее летучие (высококипящие) компоненты.
Парциа́льное давление — давление, оказываемое компонентом газовой смеси, при условии удаления других компонентов из занимаемого объёма, сохраняя этот объём и текущую температуру. Общее давление газовой смеси является суммой парциальных давлений её компонентов.

Зако́н де́йствующих масс устанавливает соотношение между массами реагирующих веществ в химических реакциях при равновесии, а также зависимость скорости химической реакции от концентрации исходных веществ. Закон действующих масс открыли в 1864—1867 годах норвежские ученые Като Гульдберг и Петер Вааге.
Акти́вность компонентов раствора — эффективная (кажущаяся) концентрация компонентов с учётом различных взаимодействий между ними в растворе, то есть с учётом отклонения поведения системы от модели идеального раствора.
Зако́ны Рау́ля — общее название открытых французским химиком Ф. М. Раулем в 1887 году количественных закономерностей, описывающих некоторые коллигативные свойства растворов.
Ректифика́ция — процесс разделения двойных или многокомпонентных смесей за счёт противоточного массообмена между паром и жидкостью. Ректификация — разделение жидких смесей на практически чистые компоненты, различающиеся температурами кипения, путём многократного частичного испарения жидкости и частичной конденсации паров.
Сорбция — поглощение твёрдым телом либо жидкостью различных веществ из окружающей среды. Поглощаемое вещество, находящееся в среде, называют сорбатом (сорбтивом), поглощающее твёрдое тело или жидкость — сорбентом.
Зако́н Ге́нри, Закон Генри — Дальтона — закон, по которому при постоянной температуре растворимость газа в данной жидкости прямо пропорциональна давлению этого газа над раствором. Закон пригоден лишь для идеальных растворов и невысоких давлений.

Ребризер — дыхательный аппарат, в котором углекислый газ, выделяющийся в процессе дыхания, поглощается химическим составом (химпоглотителем), затем смесь обогащается кислородом и подаётся на вдох. Русское название ребризера — Изолирующий дыхательный аппарат, (ИДА). Тот же самый принцип используется в аппаратах типа «кислородный изолирующий противогаз» (КИП), данные аппараты использовались в государственной противопожарной службе МВД.
Законы Вревского — законы, предложенные Михаилом Степановичем Вревским, описывающие зависимость состава равновесных жидкой и паровой фаз двойных систем от температуры (давления). Основываются на общих термодинамических соотношениях, устанавливающих условия равновесия в двухфазных системах, частным случаем которых является равновесие жидкость — пар. При выводе законов Вревского сделан ряд допущений, в частности предполагается, что поведение газовой фазы близко к поведению идеального газа. Поэтому законы Вревского справедливы только для области температур и давлений, значительно удалённой от критической точки равновесия жидкость — пар в данной системе.
Законы Коновалова описывают процессы, протекающие в равновесных системах «жидкий раствор — пар» при различных температурах, давлениях и составах компонентов. Эти законы лежат в основе теории ректификации бинарных смесей.

Алексей Васильевич Сторо́нкин (1916—1994) — советский физикохимик, основатель кафедры теории растворов химического факультета ЛГУ. Создатель школы термодинамики. Автор фундаментального труда «Термодинамика гетерогенных систем». Член ВКП(б) с 1945 года.

Рефракто́метр — инструмент, измеряющий показатель преломления света в среде.
Конста́нта равнове́сия — величина, определяющая для данной химической реакции соотношение между термодинамическими активностями исходных веществ и продуктов в состоянии химического равновесия. Зная константу равновесия реакции, можно рассчитать равновесный состав реагирующей смеси, предельный выход продуктов, определить направление протекания реакции.

Реальный раствор — гомогенная смесь двух или более компонентов, образование которой сопровождается тепловым эффектом и изменением объема. Это объясняется различной Ван-дер-Ваальсовой энергией межмолекулярного взаимодействия между однородными и разнородными молекулами.