
Хлори́д на́трия или хлористый натрий (NaCl) — натриевая соль соляной кислоты. Известен в быту под названием поваренной соли, основным компонентом которой и является. Хлорид натрия в значительном количестве содержится в морской воде. Встречается в природе в виде минерала галита и будучи растворëнным в водах естественных водоёмов, в некоторых таких водоёмах раствор насыщенный (рапа), как например в озере Баскунчак. Чистый хлорид натрия представляет собой бесцветные кристаллы, но с различными примесями его цвет может принимать голубой (электриды), фиолетовый, розовый, жёлтый или серый оттенок.

Бром — химический элемент 17-й группы четвёртого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 35.

Хлор — химический элемент 17-й группы третьего периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 17.

Со́ли — сложные вещества, состоящие из катионов металлов и анионов кислотных остатков. ИЮПАК определяет соли как химические соединения, состоящие из катионов и анионов. Есть ещё одно определение: солями называют вещества, которые могут быть получены при взаимодействии кислот и оснований с выделением воды.

Фтор — химический элемент 17-й группы второго периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 9.

Ма́гний — химический элемент 2-й группы третьего периода периодической системы химических элементов Д. И. Менделеева с атомным номером 12.

Ка́лий — химический элемент 1-й группы, четвёртого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 19.

Гидрокси́д на́трия — неорганическое химическое соединение, являющееся самой распространённой щёлочью. В год в мире производится и потребляется около 57 миллионов тонн едкого натра.
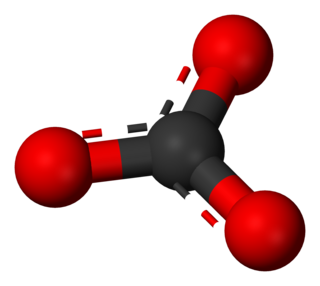
Карбона́ты — соли угольной кислоты (H2CO3), также (в органической химии) сложные эфиры угольной кислоты. Неорганические карбонаты подразделяются на средние, или просто карбонаты, содержащие анион СО32−, и кислые (гидрокарбонаты или бикарбонаты), содержащие анион НСО3−. Органические карбонаты имеют общую формулу R−O−С(O)−O−R, могут иметь ациклическое и циклическое строение.
Хими́ческая фо́рмула — условное обозначение химического состава и структуры соединений с помощью символов химических элементов, числовых и вспомогательных знаков. Химические формулы являются составной частью языка химии, на их основе составляются схемы и уравнения химических реакций, а также химическая классификация и номенклатура веществ. Одним из первых начал использовать их русский химик А. А. Иовский.

Хлори́д ка́лия — химическая неорганическая средняя калиевая соль соляной кислоты.

Ионная связь — сильная химическая связь между атомами существенно отличающимися между собой по электроотрицательности.
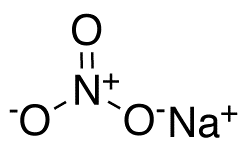
Нитра́т на́трия (азотноки́слый на́трий, натриевая селитра, чилийская селитра, натронная селитра) — натриевая соль азотной кислоты с формулой NaNO3. Бесцветные прозрачные кристаллы с ромбоэдрической или тригональной кристаллической решеткой без запаха. Вкус — резкий солёный. Применяется очень широко и является незаменимым в промышленности соединением.

Фторид натрия — неорганическое бинарное соединение с химической формулой NaF. Белое кристаллическое вещество.

Окси́д бери́ллия — бинарное химическое соединение бериллия и кислорода с химической формулой BeO, амфотерный оксид.

Фтори́д бери́ллия — бинарное неорганическое химическое соединение бериллия и фтора, химической формулой BeF2, бериллиевая соль фтористоводородной кислоты. Токсичен и канцерогенен, как и все соединения бериллия. Попадание пыли, содержащей галогениды, оксид и другие соединения бериллия, в лёгкие вызывает бериллиоз.

Фторид аммония — неорганическое соединение, соль аммония и фтористоводородной кислоты с формулой NH4F, бесцветные кристаллы, растворимые в воде, образует кристаллогидрат.

Молибдат натрия — неорганическое соединение, соль металла натрия и молибденовой кислоты с формулой Na2MoO4, белые кристаллы, растворимые в воде, образует кристаллогидраты.
Батарея на расплавах солей — это аккумулятор, в котором в качестве электролита используются расплавленные соли. Такие аккумуляторы обеспечивают как высокую плотность энергии, так и высокую удельную мощность. Традиционные неперезаряжаемые термальные батареи могут храниться в твёрдом состоянии при комнатной температуре в течение длительного периода времени до активировации путём нагрева. Перезаряжаемые жидкометаллические батареи используются для промышленного резервного питания, электромобилей и для хранения энергии в сети, чтобы сбалансировать прерывистые возобновляемые источники энергии, такие как солнечные батареи и ветрогенераторы.




















