
Ферме́нты, или энзи́мы , — обычно сложные белковые соединения, РНК (рибозимы) или их комплексы, ускоряющие химические реакции в живых системах. Каждый фермент, свернутый в определённую структуру, ускоряет соответствующую химическую реакцию: реагенты в такой реакции называются субстратами, а получающиеся вещества — продуктами. Ферменты специфичны к субстратам: АТФ-аза катализирует расщепление только АТФ, а киназа фосфорилазы фосфорилирует только фосфорилазу.
Коферме́нты, или коэнзи́мы — органические природные соединения небелковой природы, необходимые для осуществления каталитического действия ферментов. Коферменты вместе с функциональными группами аминокислотных остатков фермента формируют активный центр фермента, на котором происходит связывание с субстратом и образование активированного фермент-субстратного комплекса.

Иммуноферментный анализ — лабораторный иммунологический метод качественного или количественного определения различных низкомолекулярных соединений, макромолекул, вирусов и пр., в основе которого лежит специфическая реакция антиген-антитело. Выявление образовавшегося комплекса проводят с использованием фермента в качестве метки для регистрации сигнала. Теоретические основы ИФА опираются на современную иммунохимию и химическую энзимологию, знание физико-химических закономерностей реакции антиген-антитело, а также на основные принципы аналитической химии.

В биологии активный центр — это область фермента, где молекулы субстрата связываются и подвергаются химической реакции. Активный центр состоит из аминокислотных остатков, которые образуют временные связи с субстратом, и остатков, которые катализируют реакцию этого субстрата. Хотя активный центр занимает только ~ 10-20 % от объёма фермента он является наиболее важной частью, поскольку он непосредственно катализирует химическую реакцию. Обычно активный центр состоит из трех-четырех аминокислот, в то время как другие аминокислоты в белке необходимы для поддержания его третичной структуры.
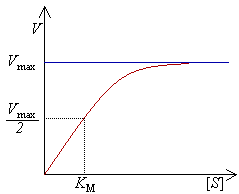
Уравне́ние Михаэ́лиса — Ме́нтен — уравнение наиболее известной модели ферментативной кинетики, описывает зависимость скорости реакции, катализируемой ферментом, от концентрации субстрата при определённых общепринятых допущениях. Уравнение названо в честь физикохимиков Леонора Михаэлиса и Мод Леоноры Ментен, опубликовавших в 1913 году статью, в которой они провели математический анализ ферментативной кинетики. Простейшая кинетическая схема, для которой справедливо уравнение Михаэлиса:


Ферментативный ингибитор — вещество, замедляющее протекание ферментативной реакции. Различают обратимые и необратимые ингибиторы.
Химическая кинетика или кинетика химических реакций — раздел физической химии, изучающий закономерности протекания химических реакций во времени, зависимости этих закономерностей от внешних условий, а также механизмы химических превращений.
Фосфатаза — фермент, который катализирует дефосфорилирование субстрата в результате гидролиза сложноэфирной связи фосфорной кислоты. При этом образуется фосфатный анион и молекула продукта с гидроксильной группой. По своему каталитическому и физиологическому действию фосфатаза является антагонистом фосфорилазы и киназы, которые присоединяют фосфатную группу к субстрату.

Комплемента́рность — взаимное соответствие молекул биополимеров или их фрагментов, обеспечивающее образование связей между пространственно взаимодополняющими (комплементарными) фрагментами молекул или их структурных фрагментов вследствие супрамолекулярных взаимодействий.
Протеа́зы, протеиназы, протеолитические ферменты — ферменты из класса гидролаз, которые расщепляют пептидную связь —СО—NH— между аминокислотами в белках. Делятся на две группы:
- экзопротеазы — выделяются организмом во внешнюю среду ;
- эндопротеазы — находятся внутри клеток.
Абзимы — каталитически активные антитела. В широком смысле термином «абзимы» обычно называют моноклональные каталитически активные антитела, обладающие свойствами ферментов — то есть катализирующие определённые химические реакции.
Протеинкина́зы — подкласс ферментов киназ (фосфотрансфераз). Протеинкиназы модифицируют другие белки путём фосфорилирования остатков аминокислот, имеющих гидроксильные группы или гетероциклической аминогруппы гистидина.
Каталитически совершенный фермент (catalytically perfect enzyme, kinetically perfect enzyme) — фермент, который совершает катализ настолько эффективно, что реакция происходит практически каждый раз, когда фермент встречает субстрат. Фактор kcat/Km для такого фермента имеет порядок от 108 до 109 M−1 с−1. Такая реакция лимитируется только скоростью диффузии субстрата.
β2-адренорецепторы — один из подтипов адренорецепторов. Эти рецепторы чувствительны в основном к адреналину, норадреналин действует на них слабо, так как эти рецепторы имеют к нему низкую аффинность.
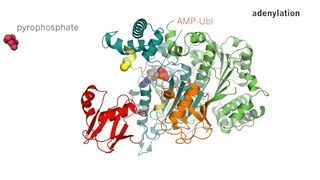
Ферментативный катализ — это увеличение скорости процесса с помощью биологической молекулы, «фермента». Большинство ферментов представляют собой белки, и большинство таких процессов представляют собой химические реакции. Внутри фермента катализ обычно происходит в локализованном центре, называемом активным центром.

Ферментати́вная кине́тика — зависимость скорости химической реакции от её условий — раздел биохимии, предметом которого являются химические реакции, катализируемые ферментами, изучающий закономерности течения во времени и механизм ферментативных реакций. Ферментативная кинетика занимается исследованием закономерностей влияния химической природы реагентов, количественным изучением эффектов варьирования условий (кинетики) той или иной химической реакции, а также измеряет её скорость. Изучение ферментов позволяет выявить каталитический механизм действия определённого фермента и контролировать его роль в процессе обмена веществ, способного замедлять (ингибировать) или ускорять (активировать) ход химической реакции. Таким образом, кинетические исследования позволяют не только определить сродство и специфичность связывания субстратов и ингибиторов к ферментам, но и найти максимальную скорость процесса, катализируемого специфическим ферментом, а также попутно решить многие другие задачи и возникающие проблемы. При этом, основная часть проблем ферментативной кинетики сводится к:
- анализу предполагаемых схем ферментативных реакций,
- выводу уравнений скорости, соответствующих этим схемам,
- сопоставлению полученных зависимостей с данными эксперимента.
Транскетолазы — группа ферментов пентозофосфатного пути и цикла Кальвина. Они катализирует две важные реакции, которые действуют в противоположных направлениях в этих двух путях.
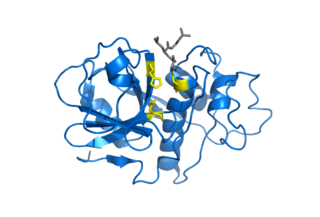
Цистеиновые протеазы, также известные, как цистеиновые эндопептидазы или тиоловые протеазы — группа протеолитических ферментов (эндопептидаз), расщепляющих белковые молекулы, на составляющие их аминокислоты, посредством гидролиза пептидной связи (протеолиза). В состав активного центра данных протеаз обязательно входит цистеин и их каталитическая активность зависит от сульфгидрильной или тиоловой группы (-SH-группа).
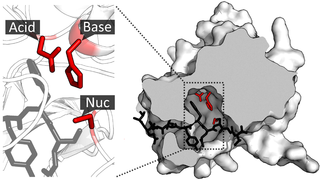
Каталитическая триада — это набор из трех скоординированных аминокислот, которые можно найти в активном центре некоторых ферментов. Каталитические триады чаще всего встречаются в ферментах гидролаз и трансфераз. Триада кислота-основание-нуклеофил является распространенным мотивом для образования нуклеофильного остатка для ковалентного катализа. Остатки образуют сеть реле заряда для поляризации и активации нуклеофила, который атакует субстрат, образуя ковалентный промежуточный продукт, который затем гидролизуется с высвобождением продукта и регенерацией свободного фермента. Нуклеофилом чаще всего является аминокислота серин или цистеин, но иногда треонин или даже селеноцистеин. Трехмерная структура фермента объединяет триадные остатки в точной ориентации, даже если они могут находиться далеко друг от друга в последовательности.
Ферментный промискуитет (неразборчивость) — это способность фермента катализировать случайную побочную реакцию в дополнение к своей основной реакции. Хотя ферменты являются чрезвычайно специфическими катализаторами, они часто могут выполнять побочные реакции в дополнение к своей основной природной каталитической активности. Побочная активность фермента обычно протекает медленнее по сравнению с основной деятельностью и находится под нейтральным отбором. Несмотря на то, что обычно эти активности физиологически нерелевантны, в условиях нового избирательного давления эти виды деятельности могут принести пользу, тем самым побуждая эволюцию ранее побочных активностей стать новым основным видом деятельности. Примером этого является хлоргидролаза атразина (кодируется atzA) Pseudomonas sр., произошедшая из меламиндезаминазы, которая имеет очень небольшую побочную активность в отношении атразина, химического вещества, созданного руками человека.










