Вещество́ — одна из форм материи, состоящая из фермионов или содержащая фермионы наряду с бозонами; обладает массой покоя, в отличие от некоторых типов полей, как, например, электромагнитное.

Моле́кула — электрически нейтральная частица, образованная из двух или более связанных атомов.

Физи́ческая хи́мия — раздел химии, наука об общих законах строения, структуры и превращения химических веществ. Исследует химические явления с помощью теоретических и экспериментальных методов физики. Наиболее обширный раздел химии.
Эле́ктроотрица́тельность (χ) — фундаментальное химическое свойство атома, количественная характеристика способности атома в молекуле смещать к себе общие электронные пары, то есть способность атомов притягивать к себе электроны других атомов. Самая высокая степень электроотрицательности у галогенов и сильных окислителей, а низкая — у активных металлов.
Неоргани́ческая хи́мия — раздел химии, связанный с изучением строения, реакционной способности и свойств всех химических элементов и их неорганических соединений. Эта область охватывает все химические соединения, за исключением органических веществ. Различия между органическими и неорганическими соединениями, содержащими углерод, являются по некоторым представлениям произвольными. Неорганическая химия изучает химические элементы и образуемые ими простые и сложные вещества. Обеспечивает создание материалов новейшей техники. Число известных на 2013 г. неорганических веществ приближается к 500 тысячам.
Сте́пень окисле́ния — вспомогательная условная величина для записи процессов окисления, восстановления и окислительно-восстановительных реакций. Она указывает на состояние окисления отдельного атома молекулы и представляет собой лишь удобный метод учёта переноса электронов: она не является истинным зарядом атома в молекуле.
Химическая связь — взаимодействие атомов, обусловливающее устойчивость молекулы или кристалла как целого. Химическая связь определяется взаимодействием между заряженными частицами. Современное описание химической связи проводится на основе квантовой механики. Основные характеристики химической связи — прочность, длина, полярность, устойчивость.
Хими́ческая фо́рмула — условное обозначение химического состава и структуры соединений с помощью символов химических элементов, числовых и вспомогательных знаков. Химические формулы являются составной частью языка химии, на их основе составляются схемы и уравнения химических реакций, а также химическая классификация и номенклатура веществ. Одним из первых начал использовать их русский химик А. А. Иовский.
Изоморфизм — свойство элементов замещать друг друга в структуре кристалла. Изоморфизм возможен при одинаковых координационных числах атомов, а в ковалентных соединениях при тождественной конфигурации связей. Степень совершенства изоморфизма определяется близостью межатомных расстояний, состоянием химической связи и строением электронной оболочки атомов.
Теория химического строения — учение о строении молекулы, описывающее все те её характеристики, которые в своей совокупности определяют химическое поведение данной молекулы. Сюда относятся: природа атомов, образующих молекулу, их валентное состояние, порядок и характер химической связи между ними, пространственное их расположение, характерное распределение электронной плотности, характер электронной поляризуемости электронного облака молекулы и т. д.

Вале́нтность — способность атомов образовывать определённое количество химических связей, которые образует атом, или число атомов, которое может присоединить или заместить атом данного элемента.

Ковале́нтная связь — химическая связь, образованная перекрытием (обобществлением) пары валентных электронных облаков. Обеспечивающие связь электронные облака (электроны) называются общей электронной парой.
Металли́ческая связь — химическая связь между атомами в металлическом кристалле, возникающая за счёт перекрытия (обобществления) их валентных электронов. Металлическая связь описывается многими физическими свойствами металлов, такими как прочность, пластичность, теплопроводность, удельное электрическое сопротивление и проводимость, непрозрачность и блеск.

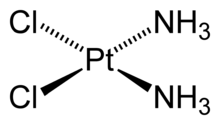
Ко́мплексные соедине́ния или координацио́нные соедине́ния — это соединения, которые образуются в результате присоединения к данному иону, называемому комплексообразователем, нейтральных молекул или других ионов, называемых лигандами. Теория комплексных соединений была предложена в 1893 г. А. Вернером.
Лига́нд — атом, ион или молекула, связанные с другим атомом (акцептором) с помощью донорно-акцепторного взаимодействия. Понятие применяется в химии комплексных соединений, обозначая присоединенные к одному или нескольким центральным (комплексообразующим) атомам металла частицы.

Кристалли́ческая структу́ра — такая совокупность атомов, в которой с каждой точкой кристаллической решётки связана определённая группа атомов, называемая мотивной единицей, причём все такие группы одинаковые по составу, строению и ориентации относительно решётки. Можно считать, что структура возникает в результате синтеза решётки и мотивной единицы, в результате размножения мотивной единицы группой трансляции.
Термин геометрическая координация используется в целом ряде смежных областей химии — химии/физики твердого тела и не только.
Координационная химия — раздел химии, в котором изучаются химические соединения, состоящие из центрального атома и связанных с ним молекул или ионов — лигандов.
Одноэлектронная химическая связь — это простейшая химическая связь, обуславливающая существование молекулярных соединений посредством кулоновского удерживания двух атомных ядер одним электроном. Главные отличительные черты одноэлектронной химической связи — это понижение полной энергии молекулярной системы по сравнению с энергией изолированных атомов и атомных фрагментов, из которых она образована, а также существенное перераспределение электронной плотности в области одноэлектронной химической связи по сравнению с простым наложением электронной плотности атома и атомного фрагмента, сближенных на расстоянии связи.
Вале́нтность стехиометри́ческая химического элемента — целое число от 1 до 8, характеризующее данный элемент и помогающее составлению правильных химических формул простых соединений с участием этого элемента.