Хром — химический элемент 6-й группы, четвёртого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 24.

Ма́рганец — химический элемент 7-й группы четвёртого периода периодической системы химических элементов Д. И. Менделеева с атомным номером 25.
Неоргани́ческие (минера́льные) кисло́ты — неорганические вещества, обладающие комплексом физико-химических свойств, которые присущи кислотам. Вещества кислотной природы известны для большинства химических элементов за исключением щелочных и щёлочноземельных металлов.

Триокси́д ксено́на XeO3 — белые или светло-голубые кристаллы. Получают гидролизом тетра- или гексафторида ксенона. В сухом виде чрезвычайно взрывоопасен, особенно при контакте с органикой.
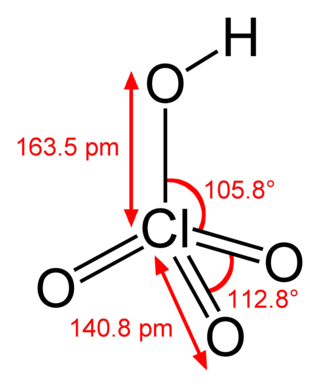
Хло́рная кислота́ (хим. формула — HClO4) — сильная одноосновная кислота.
Хроматы — соли хромовой кислоты H2CrO4. Устойчивы в нейтральной и щелочной среде, в кислой среде обратимо переходят в дихроматы — соли дихромовой кислоты H2Cr2O7.

Мангана́ты — соли нестойких, несуществующих в свободном состоянии кислородсодержащих кислот марганца в степенях окисления V, VI и VII и содержащие тетраэдрические анионы MnO43− (гипоманганаты), MnO42− (манганаты) и MnO4− (перманганаты) соответственно.

Тетрафтори́д ксено́на — соединение ксенона со фтором, представляющее собой при комнатной температуре бесцветные кристаллы со слабым желтоватым оттенком и чрезвычайно высокой химической активностью и агрессивностью. Самое устойчивое соединение ксенона. Чистый тетрафторид ксенона стабилен, однако во влажном воздухе гидролизуется с образованием оксифторидов ксенона.

Гексафтори́д ксено́на — XeF6, бинарное неорганическое химическое соединение ксенона с фтором, представляющее собой при комнатной температуре бесцветные кристаллы. Формально является высшим фторидом ксенона. Обладает чрезвычайно высокой химической активностью и агрессивностью.

Тетраокси́д ксено́на XeO4 — жёлтые кристаллы при температуре ниже −36 °C. XeO4 — соединение ксенона, в котором ксенон проявляет высшую степень окисления +8 (такую степень окисления ксенон может проявить только в соединении с кислородом, максимальная степень окисления со фтором равна +6, например, в гексафториде ксенона) и соответственно валентность, равную 8. Кроме него такую же степень окисления ксенон имеет в ксеноновой кислоте и её солях.

Нитриты — соли азотистой кислоты HNO2, например, нитрит натрия NaNO2, нитрит кальция Ca(NO2)2. Известны нитриты щелочных, щелочноземельных, 3d-металлов, а также нитриты свинца и серебра.
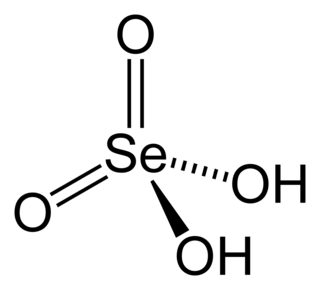
Селе́новая кислота́ — неорганическая кислота, состоящая из катиона водорода и аниона селената (SeO42-). Химическая формула  . Сильная кислота, токсична.
. Сильная кислота, токсична.

Дифторид ксенона XeF2 — твёрдое плотное кристаллическое соединение белого цвета, образованное атомами фтора и ксенона. Одно из самых устойчивых соединений ксенона.

Бромная кислота — сильная одноосновная кислота, с химической формулой HBrO4. Получена в 1964 г. окислением броматов дифторидом ксенона. Соли кислоты — перброматы. В чистом виде не выделена, хотя получены концентрированные растворы.

Тетрафтораммо́ний NF4+ — комплексный неорганический катион, представляющий собой аммоний, все четыре атома водорода в котором замещены фтором. Тетрафтораммоний является сильным окислителем и одним из немногих устойчивых соединений (и единственным бескислородным), в которых азот имеет степень окисления +5.

Диазониевые соли (ароматические диазосоединения) — соединения общей формулы R—N+≡N • X−, где R, как правило, арил или гетарил, а X- — анион (Cl−, NO3−, ОН− и др.), например, хлорид бензолдиазония C6H5N+≡N Cl-.
Соли диоксигенила (диоксигенильные соединения) — соли катиона кислорода O2+.

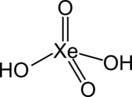
Ксено́новая кислота́ — очень неустойчивое химическое соединение с формулой  .
.

Сульфа́ты — соли серной кислоты H2SO4, а также (в органической химии) сложные эфиры серной кислоты —диалкилсульфаты R−O−SO2−O−R и алкилсульфаты Н−O−SO2−O−R.
Ксенаты — неорганические соли (ксенонистой кислоты), H2XeO4, не полученная в чистом виде. Существование щелочных ксенатов подтверждается инфракрасной спектроскопией, рентгенограммами порошковой дифракции и определением эквивалента окисления методом титрования hi-lo.