Протео́мика — область молекулярной биологии, посвящённая идентификации и количественному анализу белков. Термин «протеомика» был предложен в 1997 году. Совокупность всех белков клетки называют протеомом.

Аминокисло́ты, также аминокарбо́новые кисло́ты, АМК — органические соединения, в молекуле которых одновременно содержатся карбоксильные и аминные группы. Основные химические элементы аминокислот — это углерод (C), водород (H), кислород (O) и азот (N), хотя другие элементы также встречаются в радикале определенных аминокислот. Известны около 500 встречающихся в природе аминокислот . Аминокислоты могут рассматриваться как производные карбоновых кислот, в которых один или несколько атомов водорода заменены на аминогруппы.

Пептидная связь — вид амидной связи, возникающей при образовании белков и пептидов в результате взаимодействия α-аминогруппы (—NH2) одной аминокислоты с α-карбоксильной группой (—СООН) другой аминокислоты.

Белки́ — высокомолекулярные органические вещества, состоящие из альфа-аминокислот, соединённых в цепочку пептидной связью. В живых организмах аминокислотный состав белков определяется генетическим кодом, при синтезе в большинстве случаев используется 20 стандартных аминокислот. Множество их комбинаций определяет большое разнообразие свойств молекул белков. Кроме того, аминокислотные остатки в составе белка часто подвергаются посттрансляционным модификациям, которые могут возникать и до того, как белок начинает выполнять свою функцию, и во время его «работы» в клетке. Часто в живых организмах несколько молекул разных белков образуют сложные комплексы, например фотосинтетический комплекс и другие комплексы.
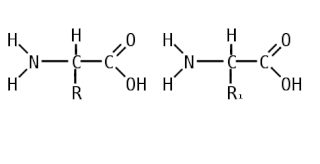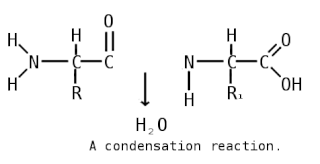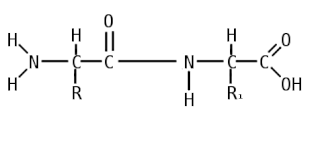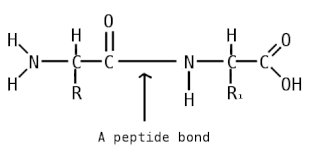
Пепти́ды — семейство веществ, молекулы которых построены из двух и более остатков аминокислот, соединённых в цепь пептидными (амидными) связями −C(O)NH−. Обычно подразумеваются пептиды, состоящие из  -аминокислот, однако термин не исключает пептидов, полученных из любых других аминокарбоновых кислот.
-аминокислот, однако термин не исключает пептидов, полученных из любых других аминокарбоновых кислот.
Химическая кинетика или кинетика химических реакций — раздел физической химии, изучающий закономерности протекания химических реакций во времени, зависимости этих закономерностей от внешних условий, а также механизмы химических превращений.
Ферме́нты пищеваре́ния, пищеварительные ферменты — ферменты, расщепляющие сложные компоненты пищи (полисахариды) до более простых веществ (олигосахаридов), которые затем всасываются в организм. В более широком смысле пищеварительными ферментами также называют все ферменты, расщепляющие крупные молекулы на мономеры или более мелкие части. Все ферменты желудочно-кишечного тракта относятся к гидролазам, что означает, что расщепление пищевых полимеров происходит всегда при участии молекулы воды.
Первичная структура биологической молекулы — точное обозначение атомной структуры и расположения химических связей между атомами. Для стандартного биополимера, в молекуле которого нет разветвлений и перекрестных связей понятие первичной структуры является синонимом последовательности остатков мономеров. Считается, что термин «первичная структура» был впервые употреблён Линнерстрёмом-Лангом в лекции Lane Medical Lectures в 1951 году.
Апудоци́ты (APUD-клетки) — диффузно расположенные секретирующие клетки, способные поглощать аминокислоты-предшественницы и производить из них активные амины и/или низкомолекулярные пептиды с помощью реакции декарбоксилирования.

Аланинаминопептидаза — мембранный белок, фермент, относящийся к классу пептидаз, или протеаз. Используется как маркёр почечных повреждений и играет роль в диагностике определённых болезней почек. Другие названия фермента: аминопептидаза M, микросомальная аминопептидаза, миелоидный гликопротеин плазматической мембраны CD13, gp150.

Интегрин бета-2 (CD18) — мембранный белок, гликопротеин из надсемейства интегринов, продукт гена ITGB2.

Интегрин бета-3 (CD61) — мембранный белок, гликопротеин из надсемейства интегринов, продукт гена ITGB3. Компонент гликопротеина IIb/IIIa, обеспечивающего агрегацию тромбоцитов.

Интегрин альфа-V — мембранный белок, гликопротеин из надсемейства интегринов, продукт гена ITGAV.

Интегрин альфа-5 — мембранный белок, гликопротеин из надсемейства интегринов, продукт гена ITGA5, альфа-субъединица интегрина α5β1 (VLA-5), одного из основных рецепторов фибронектина. Играет роль в межклеточных взаимодействиях.
Мари́я Моисе́евна Ботви́ник — советский учёный-химик, доктор химических наук, специалист в области химии белка, в частности, оксиаминокислот. Впервые в России синтезировала важнейшие оксиаминокислоты и их производные, значительно продвинула химию в решении вопроса о роли гидроксила в белке, механизмах действия ферментов.
N-Конец, также амино-конец — аминогруппа первой аминокислоты, с которой начинается молекула белка или пептид.
C-Конец, также карбоксильный конец — аминокислота, расположенная на одном из концов молекулы белка или пептида, обладающая свободной карбоксильной группой.

Смола Ванга — твердофазный носитель, предназначенный для синтеза пептидов и небольших молекул. Представляет собой полистирольные шарики диаметром 0,1 мм со степенью сшивки 1 % и загрузкой примерно 1 ммоль/г. Характерной особенностью данного носителя является то, что он содержит гидроксиметилфеноксильный линкер, что позволяет по окончании синтеза отщеплять продукты от носителя в более мягких условиях. Например, в синтезе пептидов становится возможным отщепление пептида под действием трифторуксусной кислоты, хотя ранее это можно было сделать только в присутствии плавиковой кислоты.

N,N'-Карбонилдиимидазол — органическое соединение, диимидазолид угольной кислоты. В органическом синтезе применяется как реагент для активации карбоксильных групп, для синтеза сложных эфиров, амидов, пептидов, альдегидов, кетонов и других соединений.
Остаток в биохимии и молекулярной биологии — структурная единица биополимера, состоящего из аминокислот и сахаров; часть мономера, которая остаётся неизменной после включения его в биополимер. Например, остатками принято называть аминокислотные звенья, входящие в состав пептида. Остатки уже не являются аминокислотами, так как в результате реакции конденсации, они утратили по одному атому водорода из аминогруппы и гидроксил, входящий в состав карбоксильной группы. Кроме того, остатками также считаются N-концевая и C-концевая аминокислоты пептида. Таким образом, остаток в биохимии можно определить, как ту часть молекулы, которая остаётся неизменной после отщепления от неё H+ и/или OH-.












