
Систе́ма комплеме́нта — комплекс защитных белков, постоянно присутствующих в крови. Это каскадная система протеолитических ферментов, предназначенная для гуморальной защиты организма от действия чужеродных агентов, она участвует в реализации иммунного ответа организма. Является важным компонентом как врождённого, так и приобретённого иммунитета. Выделяют три основных пути активации системы комплемента: классический, альтернативный и лектиновый. Для запуска классического пути комплемента необходима опсонизация чужеродной клетки антителами, а альтернативный и лектиновый пути могут активироваться в отсутствие антител. Поздние стадии у всех трёх путей активации системы комплемента одинаковы и включают образование мембраноатакующего комплекса, который нарушает целостность мембраны клетки-патогена и приводит к её гибели.

Цитохром — небольшой гем-содержащий белок, относится к классу цитохромов, содержит в структуре гем типа c. Выполняет в клетке две функции. С одной стороны, он является одноэлектронным переносчиком, свободно связанным с внутренней мембраной митохондрий, и необходимым компонентом дыхательной цепи. Он способен окисляться и восстанавливаться, но не связывает при этом кислород. С другой стороны, при определённых условиях он может отсоединяться от мембраны, переходить в раствор в межмембранном пространстве и активировать апоптоз. Такая двойственность связана со специфичными свойствами молекулы цитохрома c.

Никотинамидадениндинуклеоти́д — кофермент, имеющийся во всех живых клетках. NAD представляет собой динуклеотид и состоит из двух нуклеотидов, соединённых своими фосфатными группами. Один из нуклеотидов в качестве азотистого основания содержит аденин, другой — никотинамид.
Дыхательная цепь переноса электронов, также электрон-транспортная цепь (сокр. ЭТЦ, англ. ETC, Electron transport chain) — система трансмембранных белков и переносчиков электронов, необходимых для поддержания энергетического баланса. ЭТЦ поддерживает баланс за счёт переноса электронов и протонов из НАД∙Н и ФАДН2 в акцептор электронов. В случае аэробного дыхания акцептором может быть молекулярный кислород (О2). В случае анаэробного дыхания акцептором могут быть NO3−, NO2−, Fe3+, фумарат, диметилсульфоксид, сера, SO42−, CO2 и т. д. ЭТЦ у прокариот локализована в ЦПМ, у эукариот — на внутренней мембране митохондрий. Переносчики электронов расположены в порядке уменьшения сродства к электрону, то есть по своему окислительно-восстановительному потенциалу, где у акцептора самое сильное сродство к электрону. Поэтому транспорт электрона на всём протяжении цепи протекает самопроизвольно с выделением энергии. Выделение энергии в межмембранное пространство при переносе электронов происходит ступенчато, в виде протона (H+). Протоны из межмембранного пространства попадают в протонную помпу, где наводят протонный потенциал. Протонный потенциал преобразуется АТФ-синтазой в энергию химических связей АТФ. Сопряжённая работа ЭТЦ и АТФ-синтазы носит название окислительного фосфорилирования.

Окисли́тельное фосфорили́рование — метаболический путь, при котором энергия, образовавшаяся при окислении питательных веществ, запасается в митохондриях клеток в виде АТФ. Хотя различные формы жизни на Земле используют разные питательные вещества, АТФ является универсальным соединением, в котором запасается энергия, необходимая для других метаболических процессов. Почти все аэробные организмы осуществляют окислительное фосфорилирование. Вероятно, широкому распространению этого метаболического пути способствовала его высокая энергетическая эффективность по сравнению с анаэробным брожением.

Протеасо́ма — многобелковый комплекс, разрушающий ненужные или дефектные белки при помощи протеолиза до коротких пептидов. Эти пептиды затем могут быть расщеплены до отдельных аминокислот. Протеасомы присутствуют в клетках эукариот, архей и некоторых бактерий. В эукариотических клетках протеасомы содержатся и в ядре, и в цитоплазме. Деградация 80—90 % внутриклеточных белков происходит при участии протеасомы. Для того чтобы белок-мишень расщепился протеасомой, он должен быть помечен путём присоединения к нему маленького белка убиквитина. Реакция присоединения убиквитина катализируется ферментами убиквитинлигазами. Присоединение первой молекулы убиквитина к белку служит для убиквитинлигаз сигналом для дальнейшего присоединения молекул убиквитина. В результате к белку оказывается присоединена полиубиквитиновая цепь, которая связывается с протеасомой и обеспечивает расщепление белка-мишени. В целом вся эта система получила название убиквитин-зависимой деградации белка.

Цитохром-c-оксида́за (цитохромоксидаза) или цитохром-c-кислород:оксидоредуктаза, также известная как цитохром aa3 и комплекс IV — терминальная оксидаза аэробной дыхательной цепи переноса электронов, которая катализирует перенос электронов с цитохрома с на кислород с образованием воды. Цитохромоксидаза присутствует во внутренней мембране митохондрий всех эукариот, где её принято называть комплекс IV, а также в клеточной мембране многих аэробных бактерий.
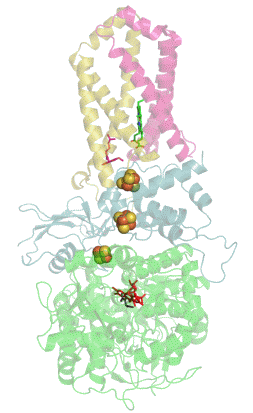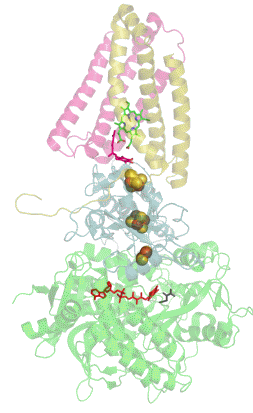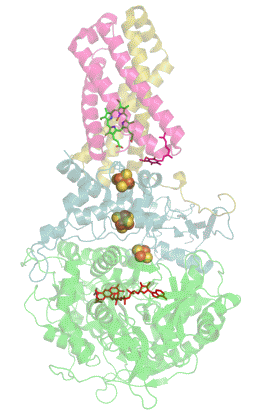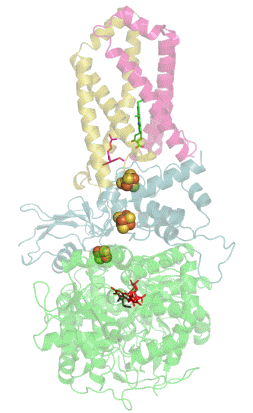
Сукцинатдегидрогеназа или сукцинат-убихинон-оксидорекдуктаза, также известная как комплекс II — белковый комплекс, расположенный во внутренней мембране митохондрий и мембранах многих прокариотических организмов. Одновременно участвует в цикле трикарбоновых кислот и дыхательной цепи переноса электронов.

Фотосисте́ма I, или пластоциани́н-ферредокси́н-оксидоредукта́за — второй функциональный комплекс электрон-транспортной цепи (ЭТЦ) хлоропластов. Он принимает электрон от пластоцианина и, поглощая световую энергию, формирует сильный восстановитель П700, способный через цепь переносчиков электронов осуществить восстановление НАДФ+. Таким образом, при участии ФСI синтезируется источник электронов (НАДФН) для последующих реакций восстановления углерода в хлоропластах в цикле Кальвина. Кроме того, ФСI может осуществлять циклический транспорт электронов, сопряжённый с синтезом АТФ, обеспечивая дополнительный синтез АТФ в хлоропластах.
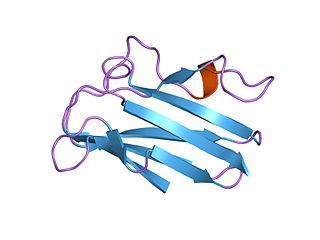
Пластоцианиновое/азуриновое семейство медьсвязывающих белков — семейство маленьких белков способных связывать один атом меди и характеризуемых сильным поглощением с пиком в области 600 нм, благодаря чему в восстановленном состоянии обычно окрашены в ярко-голубой цвет. Самые известные из членов этого класса белков — растительные пластоцианины, маленькие водорастворимые белки хлоропластов, переносящие электрон с цитохрома f, и состоящие в дальнем родстве с бактериальными белками азуринами, которые обмениваются электронами с цитохромом c551. В это же семейство включают белок амицианин из таких бактерий как Methylobacterium extorquens или Paracoccus versutus, способных расти на метиламине; аурацианины A и B из Chloroflexus aurantiacus; голубой медьсодержащий протеин из Alcaligenes faecalis; купредоксин из очистков Cucumis sativus (огурца); кузацианин из огурца; галоцианин, мембраносвязанный белок из Natronomonas pharaonis, псевдоазурин из Pseudomonas; рустицианин из Thiobacillus ferrooxidans; стеллацианин из Rhus vernicifera ; умецианин из корней Armoracia rusticana (хрен); и аллерген Ra3 из амброзии. Этот содержащийся в пыльце белок эволюционно близок перечисленным выше полипептидам, но по-видимому потерял способность связывать медь. Хотя в первичной структуре всех этих белков наблюдается заметное расхождение, участок связывания меди остаётся крайне консервативным.
Альтернати́вная оксида́за (AO) — фермент, обеспечивающий альтернативный транспорт электронов в митохондриях всех семенных растений, грибов, а также водорослей, некоторых простейших и ряда малоподвижных или прикреплённых животных. Гомологи этого белка были обнаружены в геномах многих бактерий. Биоинформатическими методами удалось выявить альтернативную оксидазу во всех царствах, кроме архей.

Цитохро́м-b6f-ко́мплекс, или пластохинолпластоцианинредукта́за — мультибелковый комплекс, который осуществляет окисление пластохинолов и восстановление белка пластоцианина, обеспечивая, таким образом, транспорт электронов между реакционными центрами фотосистемы I (ФСI) и фотосистемы II (ФСII). Он восстанавливает маленький водорастворимый белок пластоцианин, который переносит электрон к ФСII. Аналогичную реакцию катализирует цитохром-bc1-комплекс электрон-транспортной цепи митохондрий. Цитохром-b6f-комплекс присутствует в тилакоидной мембране хлоропластов растений, водорослей и цианобактерий. Он функционально объединяет две фотосистемы в единую цепь переноса электронов от воды к НАДФ+, то есть является участником нециклического потока электронов. Кроме того, цитохромный комплекс вовлечён в циклический транспорт электронов, осуществляемый фотосистемой I.

Цитохро́м-bс1-ко́мплекс или убихинол-цитохром с-оксидоредуктаза, или комплекс III — мультибелковый комплекс дыхательной цепи переноса электронов и важнейший биохимический генератор протонного градиента на мембране митохондрий. Этот мультибелковый трансмембранный комплекс кодируется митохондриальным и ядерным геномами.

Стигмателлин — мощный ингибитор сайта окисления хинола (Qout-сайта) цитохром-bc1-комплекса митохондрий и цитохром-b6f-комплекса в мембране тилакоидов.

Современные биологические исследования выявили убедительные доказательства того, что митохондриальные ферменты дыхательной цепи переноса электронов собраны в более крупные, супрамолекулярные структуры, называемые респирасомы, что кардинально отличается от стандартной теории о свободно плавающих во внутренней мембране митохондрий дискретных ферментах. Эти суперкомплексы функционально активны и необходимы для стабильной работы дыхательных комплексов.

НАДН-дегидрогена́зный ко́мплекс, также называемый ко́мплекс I или НАДН-убихино́н-оксидоредукта́за — первый мультибелковый комплекс дыхательной цепи переноса электронов. Множество копий комплекса расположены в мембранах прокариотических организмов, способных к кислородному дыханию и внутренних мембранах митохондрий эукариотических клеток. По отношению к белкам человека комплекс I часто называют НАДН-дегидрогеназой.

Ингибиторы белка NS5A относятся к классу противовирусных препаратов прямого действия. Они направлены на белок NS5A вируса гепатита C. Их развитие является кульминацией более глубокого понимания жизненного цикла вируса. Однако, их механизм действия сложен и не полностью изучен.

Класси́ческий пу́ть актива́ции систе́мы комплеме́нта — один из трёх путей активации системы комплемента, наряду с альтернативным путём и лектиновым путём. Классический путь запускают комплексы антиген-антитело, причём антитела должны принадлежать к классу IgG или IgM. После активации происходит сборка белкового комплекса C3-конвертазы (C4b2b), который разрезает белок комплемента C3. Один из фрагментов C3, C3b, связывается с C3-конвертазой, в результате чего образуется C5-конвертаза (C4b2b3b). C5-конвертаза разрезает компонент комплемента 5, после чего образовавшиеся белковые фрагменты привлекают фагоциты в очаг инфекции и способствуют поглощению клеток патогенов. C5-конвертаза также запускает финальные стадии каскада комплемента, которые завершаются формированием мембраноатакующего комплекса. Он формирует поры в мембране клетки микроорганизма, вызывая её лизис и гибель. Помимо микробных клеток, классический путь комплемента могут запускать апоптотические тельца и некротизированные клетки.

Кобицистат, продаваемый под торговой маркой Tybost, представляет собой лекарство для лечения инфекции, вызванной вирусом иммунодефицита человека (ВИЧ/СПИД). Его основной механизм действия заключается в ингибировании белков CYP3A человека.
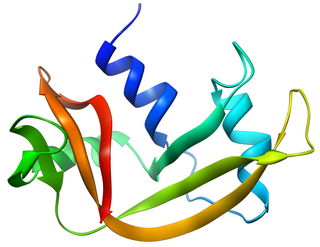
Рибонуклеазы поджелудочной железы — это пиримидин-специфичные эндонуклеазы, обнаруживаемые в большом количестве в поджелудочной железе некоторых млекопитающих и некоторых рептилий.


















