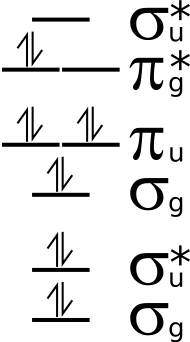А́томное ядро́ — центральная часть атома, в которой сосредоточена основная его масса. Ядро заряжено положительно, заряд ядра определяет химический элемент, к которому относят атом. Размеры ядер различных атомов составляют несколько фемтометров, что более чем в 10 тысяч раз меньше размеров самого атома. Атомные ядра изучает ядерная физика.

Физи́ческая хи́мия — раздел химии, наука об общих законах строения, структуры и превращения химических веществ. Исследует химические явления с помощью теоретических и экспериментальных методов физики. Наиболее обширный раздел химии.

Электронная конфигурация — формула расположения электронов по различным электронным оболочкам атома, химического элемента или молекулы.

Фосфоресценция — это особый тип фотолюминесценции. В отличие от флуоресцентного, фосфоресцентное вещество излучает поглощённую энергию не сразу. Большее время реэмиссии связано с «запрещёнными» энергетическими переходами в квантовой механике. Поскольку такие переходы в обычных материалах наблюдаются редко, реэмиссия поглощенного излучения проходит с более низкой интенсивностью и в течение длительного времени.

Фотолюминесценция — люминесценция (свечение), возбуждаемая светом разной длинной волны. Бывает двух типов, в зависимости от срока остаточного послесвечения: флуоресценция и фосфоресценция.

Вале́нтность — способность атомов образовывать определённое количество химических связей, которые образует атом, или число атомов, которое может присоединить или заместить атом данного элемента.

Фотохи́мия — раздел физической химии и химии высоких энергий — изучает превращения химических веществ, протекающие под действием электромагнитного излучения в ультрафиолетовом, видимом и ближнем инфракрасном диапазонах.
Фотохромизм, или тенебресценция — явление обратимого изменения окраски вещества под действием видимого света, ультрафиолета. Воздействие света вызывает в фотохромном веществе атомарные перестройки, изменение заселённости электронных уровней. Параллельно с изменением цвета вещество может менять показатель преломления, растворимость, реакционную способность, электропроводимость, другие химико-физические характеристики. Фотохромизм присущ ограниченному числу органических и неорганических, природных и синтетических соединений.
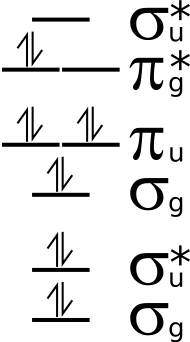
Сингле́тный кислоро́д — общее название для двух метастабильных состояний молекулярного кислорода (O2) с более высокой энергией, чем в основном, триплетном состоянии. Энергетическая разница между самой низкой энергией O2 в синглетном состоянии и наименьшей энергией триплетного состояния составляет около 11400 кельвин (Te (a1Δg ← X3Σg−) = 7918,1 см−1), или 0,98 эВ. Открыт Х. Каутским.

Тонкая структура — явление в атомной физике, описывающее расщепление спектральных линий атома.
Карбены — соединения двухвалентного углерода. Это нестабильные высокореакционноспособные соединения с шестью валентными электронами и общей формулой R1R2C: (два заместителя и электронная пара). Существует два состояния карбенов: синглетное и триплетное. Большинство карбенов существуют очень короткое время, хотя также известны и стабильные карбены. Зафиксировать карбены можно в аргоновой матрице при очень низких температурах. Названия карбенов являются производными от названия соответствующего валентно-насыщенного соединения с заменой окончаний «-ан», «-ен», «-ин» на «-илиден», «-енилиден», «-инилиден» соответственно. Применяется также заместительная номенклатура, например, дифенилкарбен, а для частицы CH2: сохранили название «метилен».
Спектра́льный терм - состояние атома, молекулы или иона, в котором определены их полный орбитальный момент и мультиплетность. Иногда под словом терм понимают собственно энергию данного уровня. Переходы между термами определяют спектры испускания и поглощения электромагнитного излучения.
Моле́кула водоро́да — простейшая молекула, состоящая из двух атомов водорода. В её состав входят два ядра атомов водорода и два электрона. Вследствие взаимодействия между электронами и ядрами образуется ковалентная химическая связь. Кроме вторичной изотопной модификации H2, имеет разновидности, в которых один или оба атома протия заменены другими изотопами водорода — дейтерием или тритием: HD, HT, D2, DT, T2. Симметричность или несимметричность молекулы имеет значение при её вращении.
SERF-магнитометр (Магнитометр свободный от спин-обменного уширения) был создан в 2002 г. в Принстонском университете, США. Магнитометр измеряет исключительно малые, не превышающие 0.2 мГс, магнитные поля, чувствительность магнитометра равна (10−15 Тл Гц−½). В магнитометре используются атомы калия, имеющие плотность 1014см−3, помещенныe в стеклянную ячейку (колба объёмом 0.3 см³), наполненную гелием 4Не под давлением в несколько атм и 30 торр азота N2. Чувствительность SERF-магнитометра сравнима с чувствительностью СКВИД-магнитометра. Устройство представляет собой оптический прибор, в котором детектируется изменение поглощения лазерного излучения при прохождении через атомный пар.
NV-центр или азото-замещённая вакансия в алмазе — это один из многочисленных точечных дефектов алмаза: нарушение строения кристаллической решётки алмаза, возникающее при удалении атома углерода из узла решётки и связывании образовавшейся вакансии с атомом азота.
Обменное взаимодействие — взаимодействие тождественных частиц в квантовой механике, приводящее к зависимости значения энергии системы частиц от её полного спина. Представляет собой чисто квантовый эффект, исчезающий при предельном переходе к классической механике.
Сцинтилля́ция — люминесценция малой продолжительности возникающая в результате взаимодействия сплошной среды-сцинтиллятора с ионизирующим излучением.

Пра́вило Ка́ши — эмпирическое правило в фотохимии, согласно которому для органических молекул в конденсированной фазе излучение фотона (люминесценция) всегда происходит с низшего возбуждённого уровня данной мультиплетности. Названо в честь американского спектроскописта и химика Майкла Каши, который предложил это правило в 1950 году.

Триплетное состояние — это квантовое состояние объекта, такого как электрон, атом или молекула, квантовая точка, имеющего полный спин S = 1. Оно имеет три разрешённых значения проекции спина вдоль заданной оси mS = −1, 0 или +1, что дало название «триплет».