
Руте́ний — химический элемент 8-й группы, пятого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 44.

Азо́тная кислота́ (химическая формула — HNO3; лат. Acidum nitricum, azoticum) — сильная химическая неорганическая кислота, отвечающая высшей степени окисления азота (+5).
Перехо́дные мета́ллы (перехо́дные элеме́нты) — элементы побочных подгрупп Периодической системы химических элементов Д. И. Менделеева, в атомах которых появляются электроны на d- и f-орбиталях. В общем виде электронное строение переходных элементов можно представить следующим образом:  . На ns-орбитали содержится один или два электрона, остальные валентные электроны находятся на
. На ns-орбитали содержится один или два электрона, остальные валентные электроны находятся на  -орбитали. Поскольку число валентных электронов заметно меньше числа орбиталей, то простые вещества, образованные переходными элементами, являются металлами.
-орбитали. Поскольку число валентных электронов заметно меньше числа орбиталей, то простые вещества, образованные переходными элементами, являются металлами.
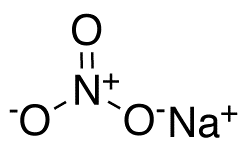
Нитра́т на́трия (азотноки́слый на́трий, натриевая селитра, чилийская селитра, натронная селитра) — натриевая соль азотной кислоты с формулой NaNO3. Бесцветные прозрачные кристаллы с ромбоэдрической или тригональной кристаллической решеткой без запаха. Вкус — резкий солёный. Применяется очень широко и является незаменимым в промышленности соединением.

Металлы платиновой группы — коллективное обозначение шести переходных металлических элементов, имеющих схожие физические и химические свойства, и, как правило, встречающихся в одних и тех же месторождениях. В связи с этим имеют схожую историю открытия и изучения, добычу, производство и применение. Металлы платиновой группы являются благородными и драгоценными металлами. В природе главные источники МПГ — ликвационные медно-никелевые руды и малосульфидные собственно платинометальные, реже отмечаются в колчеданно-полиметаллических и др. Иногда металлы платиновой группы подразделяют на две триады: рутений, родий и палладий — лёгкие платиновые металлы, а платина, иридий и осмий — тяжёлые платиновые металлы.

Катализатор Адамса (диоксид платины) — катализатор для восстановления и гидрогенолиза в органическом синтезе. Известен как гидрат диоксида платины, представляет собой тёмно-коричневый порошок. Сам по себе диоксид не является катализатором, но он переходит в активную форму после взаимодействия с водородом. Образующаяся платиновая чернь является истинным катализатором. PtO2 сам по себе — сине-чёрные кристаллы, не растворимые в воде.
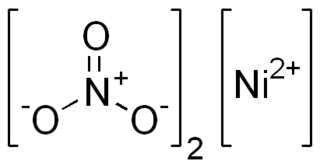
Нитра́т ни́келя(II) — неорганическое соединение, соль металла никеля и азотной кислоты с формулой Ni(NO3)2, светло-зелёные кристаллы, хорошо растворяется в воде. Образует кристаллогидраты.
Палладийпентагаллий — бинарное неорганическое соединение палладия и галлия с формулой Ga5Pd, кристаллы.
Пентапалладийдигаллий — бинарное неорганическое соединение палладия и галлия с формулой Ga2Pd5, кристаллы.
Дихлородикарбонилплатина — неорганическое соединение, хлорпроизводное карбонильного комплекса платины с формулой Pt(CO)2Cl2, светло-желтые кристаллы, реагирует с водой.
Платинатрииттрий — бинарное неорганическое соединение платины и иттрия с формулой PtY3, кристаллы.
Танталат родия — неорганическое соединение, соль родия и танталовой кислоты с формулой RhTaO4, кристаллы.
Диселенид рутения — бинарное неорганическое соединение рутения и селена с формулой RuSe2, серо-чёрные кристаллы.
Дирутенийгольмий — бинарное неорганическое соединение гольмия и рутения с формулой HoRu2, кристаллы.
Фосфид дирутения — бинарное неорганическое соединение рутения и фосфора с формулой Ru2P, кристаллы.
Фосфид рутения — бинарное неорганическое соединение рутения и фосфора с формулой RuP, кристаллы.
Дирутенийиттрий — бинарное неорганическое соединение иттрия и рутения с формулой YRu2, кристаллы.
Дирутенийтрииттрий — бинарное неорганическое соединение иттрия и рутения с формулой Y3Ru2, кристаллы.

Георгий Борисович Шульпин — российский учёный, ведущий научный сотрудник Института химической физики (ИХФ) им. Н. Н. Семёнова РАН. Доктор химических наук.
Восстановительное элиминирование — это один из типов реакций, встречающихся в металлорганической химии. Оно заключается в отщеплении органического субстрата от атома металла с одновременным уменьшением его формальной степени окисления на -2. Восстановительное элиминирование часто является частью каталитических циклов наряду с обратной реакцией окислительного присоединения.








