Зако́н Авога́дро — закон, согласно которому в равных объёмах различных газов, взятых при одинаковых температурах и давлениях, содержится одно и то же количество молекул. В виде гипотезы был сформулирован в 1811 году Амедео Авогадро, профессором физики в Турине. Гипотеза была подтверждена многочисленными экспериментальными исследованиями и поэтому стала называться законом Авогадро, став впоследствии количественной основой современной химии (стехиометрии). Закон Авогадро точно выполняется для идеального газа, а для реальных газов он является тем более точным, чем газ более разреженный.
Сте́пени свобо́ды — характеристики движения механической системы. Число степеней свободы определяет минимальное количество независимых переменных, необходимых для полного описания состояния механической системы. Строгое теоретико-механическое определение: число степеней свободы механической системы есть размерность пространства её состояний с учётом наложенных связей.
Моля́рный объём Vm — отношение объёма вещества к его количеству, численно равен объёму одного моля вещества. Термин «молярный объём» может быть применён к простым веществам, химическим соединениям и смесям. В общем случае он зависит от температуры, давления и агрегатного состояния вещества. Молярный объём также можно получить делением молярной массы M вещества на его плотность ρ: таким образом, Vm = V/n = M/ρ. Молярный объём характеризует плотность упаковки молекул в данном веществе. Для простых веществ иногда используется термин атомный объём.
Моль — единица измерения количества вещества в Международной системе единиц (СИ), одна из семи основных единиц СИ.

Газ, или газообра́зное состоя́ние — одно из четырёх основных агрегатных состояний вещества, характеризующееся очень слабыми связями между составляющими его частицами, а также их большой подвижностью. Частицы газа почти свободно и хаотически движутся в промежутках между столкновениями, во время которых происходит резкое изменение характера их движения.

Теплопрово́дность — способность материальных тел проводить тепловую энергию от более нагретых частей тела к менее нагретым частям тела путём хаотического движения частиц тела. Такой теплообмен может происходить в любых телах с неоднородным распределением температур, но механизм переноса теплоты будет зависеть от агрегатного состояния вещества.
Идеа́льный газ — теоретическая модель, широко применяемая для описания свойств и поведения реальных газов при умеренных давлениях и температурах. В этой модели, во-первых, предполагается, что составляющие газ частицы не взаимодействуют друг с другом, то есть их размеры пренебрежимо малы, поэтому в объёме, занятом идеальным газом, нет взаимных неупругих столкновений частиц. Частицы идеального газа претерпевают столкновения только со стенками сосуда. Второе предположение: между частицами газа нет дальнодействующего взаимодействия, например, электростатического или гравитационного. Дополнительное условие упругих столкновений между молекулами и стенками сосуда в рамках молекулярно-кинетической теории приводит к термодинамике идеального газа.
Постоя́нная Бо́льцмана ( или
или  ) — физическая постоянная, определяющая связь между температурой и энергией. Названа в честь австрийского физика Людвига Больцмана, внёсшего большой вклад в статистическую физику, в которой эта постоянная играет ключевую роль. Её значение в Международной системе единиц СИ согласно изменениям определений основных единиц СИ точно равно
) — физическая постоянная, определяющая связь между температурой и энергией. Названа в честь австрийского физика Людвига Больцмана, внёсшего большой вклад в статистическую физику, в которой эта постоянная играет ключевую роль. Её значение в Международной системе единиц СИ согласно изменениям определений основных единиц СИ точно равно
- k = 1,380 649 · 10−23 Дж/К.
Адиабати́ческий, или адиаба́тный проце́сс — термодинамический процесс в макроскопической системе, при котором система не обменивается теплотой с окружающим пространством. Серьёзное исследование адиабатических процессов началось в XVIII веке. В целом термин «адиабатический» в разных областях науки всегда подразумевает сохранение неизменным какого-то параметра. Так в квантовой химии, электронно-адиабатический процесс — это процесс, в котором не изменяется квантовое число электронного состояния. Например, молекула всегда остаётся в первом возбуждённом состоянии вне зависимости от изменения положения атомных ядер. Соответственно неадиабатическим называется процесс, в котором происходит изменение какого-то важного параметра.
Уравне́ние состоя́ния идеа́льного га́за — формула, устанавливающая зависимость между давлением, молярным объёмом и абсолютной температурой идеального газа. Уравнение имеет вид:
 ,
,
Универса́льная га́зовая постоя́нная — константа, численно равная работе расширения одного моля идеального газа в изобарном процессе при увеличении температуры на 1 К. Равна произведению постоянной Больцмана на число Авогадро. Обозначается латинской буквой R.
Закон Дюлонга — Пти — эмпирический закон, согласно которому молярная теплоёмкость твёрдых тел при комнатной температуре близка к 3R:

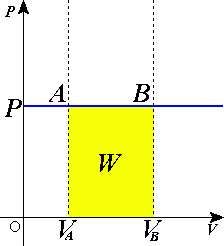
Изобари́ческий или изоба́рный проце́сс — термодинамический процесс, происходящий в системе при постоянных давлении и массе газа.
Моля́рная теплоёмкость — отношение теплоёмкости к количеству вещества, теплоёмкость одного моля вещества.
Теорема о равнораспределении кинетической энергии по степеням свободы, закон равнораспределения, теорема о равнораспределении — связывает температуру системы с её средней энергией в классической статистической механике. В первоначальном виде теорема утверждала, что при тепловом равновесии энергия разделена одинаково между её различными формами, например, средняя кинетическая энергия поступательного движения молекулы должна равняться средней кинетической энергии её вращательного движения.
Изохо́рный, или изохори́ческий проце́сс — термодинамический изопроцесс, который происходит при постоянном объёме. Для осуществления изохорного процесса в газе или жидкости достаточно нагревать или охлаждать вещество в сосуде неизменного объёма.
Сжимаемость — свойство вещества изменять свой объём под действием всестороннего равномерного внешнего давления. Сжимаемость характеризуется коэффициентом сжимаемости, который определяется формулой

















